Un nuevo estudio tuvo como objetivo comprender cómo nuestros cuerpos reconocen y responden a diferentes formas de enantiómeros de opioides. Dirigida por el Dr. Xiaohui Wang del Instituto de Química Aplicada de Changchun de la Academia de Ciencias de China, la investigación se publicó en la revista National Science Review. .
Ya en la década de 1950 se observó que la eficacia de los narcóticos opiáceos depende en gran medida de su estereoquímica. Las formas activas son los isómeros (-), mientras que los isómeros (+) no tienen ningún efecto analgésico. La morfina, un potente analgésico derivado de la adormidera, se presenta naturalmente en forma de isómero (-). Sin embargo, la (+)-morfina sintética tiene una actividad mínima y no alivia el dolor. Esto muestra que el receptor opioide μ (MOR) responde selectivamente a los enantiómeros de la morfina.
El Dr. Wang afirma:"Esta ha sido una pregunta desconcertante en neurociencia y farmacología durante el último medio siglo:¿Por qué la (-)-morfina natural alivia el dolor mientras que la (+)-morfina no?"
Los avances recientes en biología estructural han permitido a los científicos examinar estructuras de alta resolución de MOR, lo que permite estudiar su estereoselectividad a nivel atómico. Además, las simulaciones de dinámica molecular han mejorado significativamente nuestra capacidad para analizar la termodinámica y la cinética de las interacciones receptor-ligando.
El Dr. Wang añade:"El desarrollo de nuevas tecnologías nos ha dado un impulso adicional para comprender cómo MOR reconoce y responde a diferentes formas de enantiómeros de morfina".
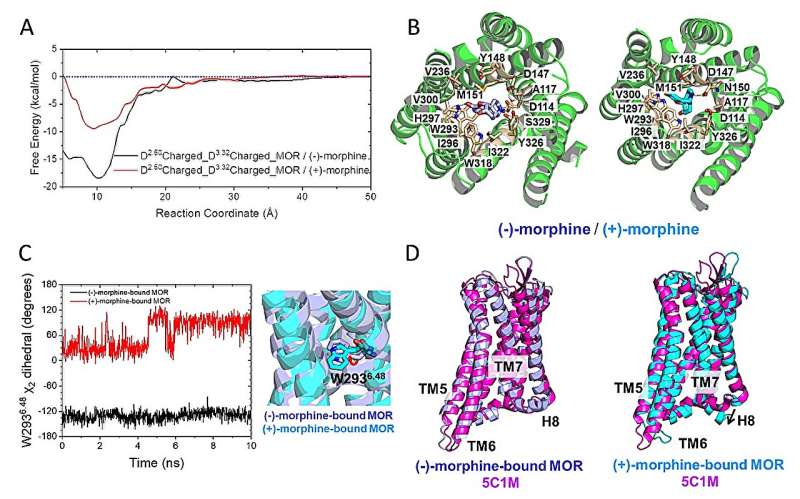
En este estudio, los investigadores emplearon simulaciones por computadora para explorar los mecanismos termodinámicos y cinéticos del reconocimiento estereoselectivo de morfina por MOR mediante simulaciones MD de todos los átomos. Descubrieron que la unión de (-)-morfina estabiliza MOR en su estado activado, exhibiendo un pozo de energía profundo, lo que resulta en un alivio del dolor.
Por el contrario, la (+)-morfina no logra mantener la activación de MOR. El estudio también identificó regiones específicas de MOR que sufren cambios cuando se unen a (-)-morfina.
"La selectividad en el reconocimiento molecular va más allá de las afinidades de unión y se extiende al ámbito del tiempo de residencia", dice el Dr. Wang. En este estudio, el análisis de la cinética arroja luz sobre la capacidad de reconocimiento quiral de MOR, tal como se refleja en el tiempo de residencia.
En particular, la (-)-morfina demostró un tiempo de residencia más prolongado que la (+)-morfina en MOR, por un notable factor de 8.000. Estos resultados cinéticos están en línea con la evidencia experimental que demuestra que la (-)-morfina funciona como un agonista de MOR, mientras que la (+)-morfina muestra una afinidad mínima por MOR.
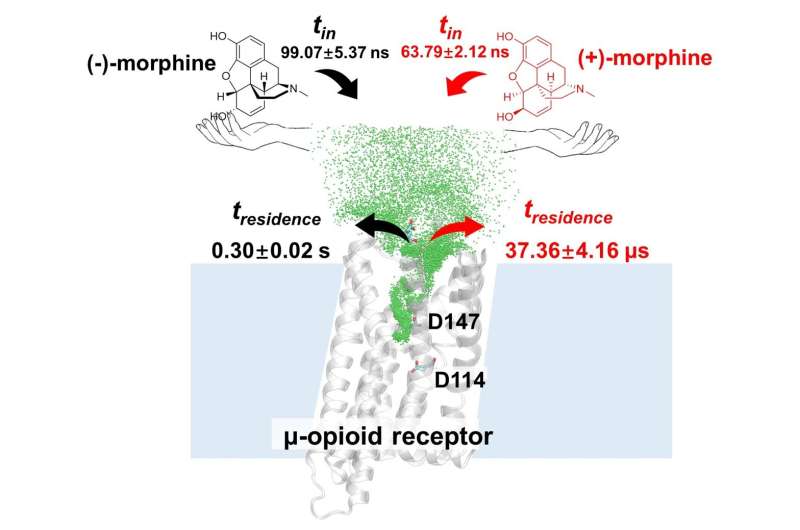
Al dilucidar la termodinámica y la cinética detrás del reconocimiento estereoselectivo de enantiómeros de morfina por parte de MOR, este estudio ofrece información valiosa sobre el funcionamiento fundamental del sistema opioide. El conocimiento adquirido a partir de esta investigación puede contribuir potencialmente al desarrollo de analgésicos más eficaces y específicos con efectos secundarios reducidos.
El Dr. Wang y su equipo opinan que sus descubrimientos sientan las bases para estudios más profundos sobre el MOR y sus interacciones con varias moléculas quirales. Esta investigación tiene el potencial de abrir nuevos caminos en los campos de la neurociencia y la farmacología.
Al profundizar en cómo MOR interactúa con estas moléculas, el equipo anticipa descubrir nuevos conocimientos sobre el comportamiento de los receptores, lo que podría conducir a avances en el desarrollo de fármacos, particularmente en el manejo del dolor y el tratamiento de la adicción. Estas exploraciones son cruciales para comprender los matices de las interacciones receptor-ligando y, en última instancia, podrían contribuir a estrategias terapéuticas más efectivas y específicas.
Más información: Yibo Wang et al, Reconocimiento estereoselectivo de enantiómeros de morfina por el receptor opioide μ, National Science Review (2024). DOI:10.1093/nsr/nwae029
Proporcionado por Science China Press