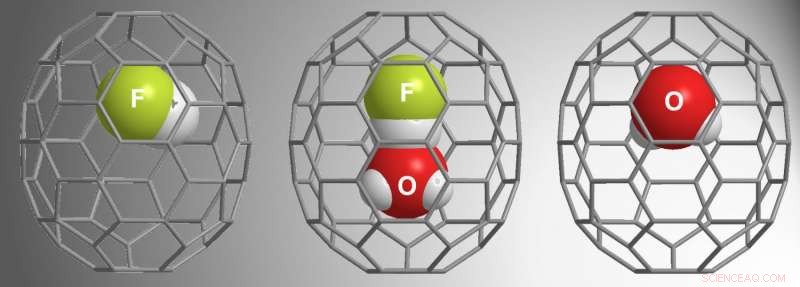
Crédito:Zhang et al.
(Phys.org) —Las clases de química para principiantes aprenden sobre los ácidos de Brønsted-Lowry. Estos ácidos se disocian en agua para formar un H + ion y un contraión cargado negativamente. Si bien esta es una lección fundamental, el mecanismo real de disolución es un poco misterioso. El h + molécula se combina con agua para formar H 3 O + , pero la cantidad de moléculas de agua necesarias para hidratar el ácido más simple, HF, es desconocido. Intentos de aislar HF y H 2 Oh, eres difícil en gran parte debido a la alta reactividad del HF y la tendencia del agua a formar enlaces de hidrógeno.
Para comprender el mecanismo fundamental detrás de la disolución ácida, Zhang y col. del Instituto de Investigación Química de la Universidad de Kyoto HF encapsulado, así como HF • H 2 O y H 2 O dentro de una C 70 fullereno. Descubrieron que para forzar a las moléculas a entrar en la cavidad de fullereno abierta, las moléculas requerían "empujar desde el exterior" en condiciones de alta presión, y "tirando desde el interior" a través de interacciones moleculares entre HF y H 2 O. Pudieron identificar cómo se producían los enlaces de hidrógeno entre estas dos moléculas. Su trabajo aparece en Avances de la ciencia .
El trabajo anterior de Zhang et al. mostró que el C 70 El fullereno podría abrirse en un proceso de tres pasos que implicaba la adición de un derivado de piridazina a los enlaces alfa o beta en el C 70 . Esto creó una apertura de anillo de 13 miembros que formó compuestos ligeramente diferentes, denotado por α-13mem y β-13mem. La deshidratación de ambos compuestos resultó en una apertura del anillo de 16 miembros. El anillo podría cerrarse nuevamente mediante hidrólisis y un proceso de dos pasos.
β-16mem fue lo suficientemente grande como para capturar H 2 Oh pero el α-16mem no lo fue. Dados estos resultados de estudios previos, para el estudio actual, Zhang y col. utilizó α-16mem para intentar encapsular HF. En lugar de, encontraron tres posibilidades diferentes dentro de los fullerenos:HF @ C 70 , (HF • H 2 JEFE 70 , y H 2 JEFE 70 .
Sus condiciones de reacción requerían alta presión (9000 atm) para "empujar" la molécula huésped hacia la cavidad α-16mem. Los estudios dependientes del tiempo mostraron que HF llenó primero la cavidad, seguido de H 2 O • HF, y luego H 2 O. En particular, la jaula abierta no atrapó a H 2 O cuando HF no estaba presente, indicando que la interacción entre H 2 O y HF impulsaron H 2 O encapsulación. Otros estudios demostraron que la HF está "tirando" de H 2 O en la cavidad mientras que el entorno de alta presión lo "empuja" hacia la cavidad.
Este proceso permitió a los autores estudiar la interacción entre H 2 O y HF en un entorno confinado utilizando 1 H NMR. El análisis de RMN mostró que el (H 2 O • HF) @C 70 fue desplazado hacia abajo de H 2 JEFE 70 y HF @ C 70 , lo que indicaba enlaces de hidrógeno. Es más, Los valores de desplazamiento y acoplamiento indicaron que el oxígeno estaba actuando como aceptor de enlaces de hidrógeno.
Usando difracción de rayos X de cristal único, Zhang y col. demostró la estructura de la (HF • H 2 JEFE 70 , e informar la primera estructura de rayos X para C doblemente encapsulado 70 . Estos análisis y estudios experimentales confirmaron que el H + ion en HF forma un enlace de hidrógeno lineal con el O en H 2 O. Además, en comparación con los cálculos teóricos de H libre 2 O y HF, Los estudios de las moléculas encapsuladas revelaron un estrecho contacto con el hidrógeno y el oxígeno que puede ser característico del H3O. + •F - .
La C 70 El derivado de fullereno proporciona un excelente nanoambiente para estudiar especies químicas aisladas, algo que no ha estado disponible para los químicos en el pasado. Este entorno aislado permitió a los autores investigar las interacciones de dos compuestos sin interferencia del entorno circundante y proporcionó información importante sobre un proceso químico ubicuo.
© 2017 Phys.org