Al comparar los patrones de expresión génica de 26 especies con diversas esperanzas de vida, los biólogos de Rochester Vera Gorbunova y Andrei Seluanov descubrieron que las características de los diferentes genes estaban controladas por redes circadianas o de pluripotencia. Crédito:Ilustración de la Universidad de Rochester / Julia Joshpe
La selección natural ha producido mamíferos que envejecen a ritmos dramáticamente diferentes. Tomemos, por ejemplo, ratas y ratones topo desnudos; los primeros pueden vivir hasta 41 años, casi diez veces más que los roedores de tamaño similar, como los ratones.
¿Qué explica una vida útil más larga? Según una nueva investigación de biólogos de la Universidad de Rochester, una pieza clave del rompecabezas radica en los mecanismos que regulan la expresión génica.
En un artículo publicado en Cell Metabolism , los investigadores, entre ellos Vera Gorbunova, profesora de biología y medicina Doris Johns Cherry; Andrei Seluanov, profesor de biología y medicina; y Jinlong Lu, investigador asociado postdoctoral en el laboratorio de Gorbunova y primer autor del artículo, investigó los genes relacionados con la esperanza de vida. Su investigación descubrió características específicas de estos genes y reveló que dos sistemas reguladores que controlan la expresión génica, las redes circadianas y de pluripotencia, son fundamentales para la longevidad. Los hallazgos tienen implicaciones tanto para comprender cómo evoluciona la longevidad como para proporcionar nuevos objetivos para combatir el envejecimiento y las enfermedades relacionadas con la edad.
Comparando genes de longevidad
Los investigadores compararon los patrones de expresión génica de 26 especies de mamíferos con una esperanza de vida máxima diversa, desde dos años (musarañas) hasta 41 años (ratas topo desnudas). Identificaron miles de genes relacionados con la vida útil máxima de una especie que estaban positiva o negativamente correlacionados con la longevidad.
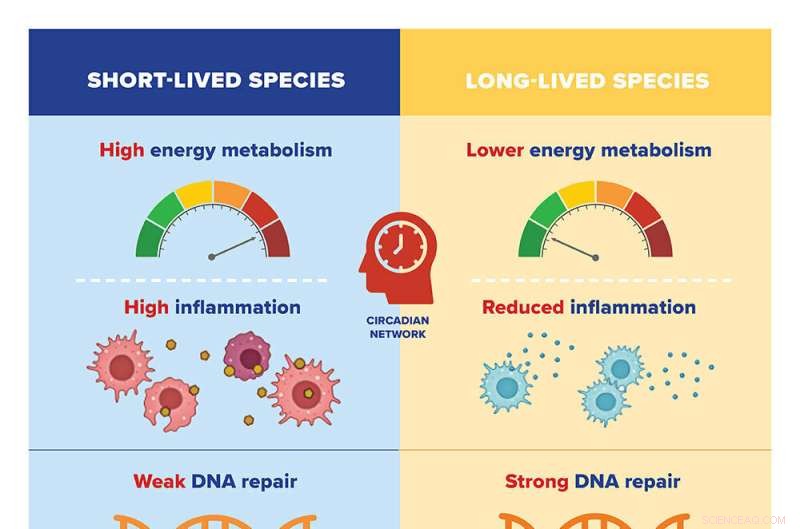
Descubrieron que las especies longevas tienden a tener una baja expresión de genes implicados en el metabolismo energético y la inflamación; y alta expresión de genes implicados en la reparación del ADN, el transporte del ARN y la organización del esqueleto celular (o microtúbulos). Investigaciones anteriores de Gorbunova y Seluanov han demostrado que características como una reparación del ADN más eficiente y una respuesta inflamatoria más débil son características de los mamíferos con una esperanza de vida prolongada.
Ocurría lo contrario con las especies de vida corta, que tendían a tener una alta expresión de genes implicados en el metabolismo energético y la inflamación y una baja expresión de genes implicados en la reparación del ADN, el transporte del ARN y la organización de los microtúbulos.
Dos pilares de la longevidad
Cuando los investigadores analizaron los mecanismos que regulan la expresión de estos genes, encontraron dos sistemas principales en juego. Los genes negativos de la esperanza de vida, los implicados en el metabolismo energético y la inflamación, están controlados por redes circadianas. Es decir, su expresión se limita a un momento particular del día, lo que puede ayudar a limitar la expresión general de los genes en especies longevas.
Esto significa que podemos ejercer al menos cierto control sobre los genes negativos de la vida útil.
"Para vivir más, tenemos que mantener horarios de sueño saludables y evitar la exposición a la luz durante la noche, ya que puede aumentar la expresión de los genes negativos de la esperanza de vida", dice Gorbunova.
Por otro lado, los genes positivos de vida útil (aquellos involucrados en la reparación del ADN, el transporte del ARN y los microtúbulos) están controlados por lo que se llama la red de pluripotencia. La red de pluripotencialidad está involucrada en la reprogramación de células somáticas (cualquier célula que no sea una célula reproductiva) en células embrionarias, que pueden rejuvenecer y regenerarse más fácilmente al reempaquetar el ADN que se desorganiza a medida que envejecemos.
"Descubrimos que la evolución ha activado la red de pluripotencialidad para lograr una vida útil más larga", dice Gorbunova.
La red de pluripotencialidad y su relación con los genes de longevidad positiva es, por lo tanto, "un hallazgo importante para comprender cómo evoluciona la longevidad", dice Seluanov. "Además, puede allanar el camino para nuevas intervenciones antienvejecimiento que activen los genes positivos clave de la vida útil. Esperaríamos que las intervenciones antienvejecimiento exitosas incluyeran el aumento de la expresión de los genes positivos de la vida útil y la disminución de la expresión de los genes negativos de la vida útil".