
Representación artística de la cicloadición 3+3. Crédito:Empa
Las síntesis químicas en líquidos y gases tienen lugar en el espacio tridimensional. Las colisiones aleatorias entre moléculas tienen que dar como resultado algo nuevo en un tiempo extremadamente corto. Pero hay otra manera:en una superficie de oro en condiciones de vacío ultraalto, las moléculas que se encuentran quietas una al lado de la otra pueden combinarse, incluso aquellas que nunca querrían reaccionar entre sí en un líquido. Los investigadores de Empa ahora han descubierto tal reacción. Lo mejor de todo es que los expertos pueden "tomar fotografías" y observar cada paso de la reacción.
En química, hay estructuras que son particularmente estables, como el llamado "anillo de benceno" que consta de seis átomos de carbono interconectados. Dichos anillos forman la base estructural del grafito y el grafeno, pero también se encuentran en muchos tintes, como el índigo para teñir jeans y en muchas drogas como la aspirina.
Cuando los químicos querían construir tales anillos de manera específica, utilizaron las llamadas reacciones de acoplamiento, que generalmente llevan el nombre de sus inventores:por ejemplo, la reacción de Diels-Alder, la reacción de Ullmann, la ciclación de Bergman o el acoplamiento de Suzuki. Ahora hay otro que aún no tiene nombre. Fue descubierto por un equipo de Empa junto con el Instituto Max Planck para la Investigación de Polímeros en Mainz. Su investigación relacionada ha sido publicada en Nature Synthesis y Nature Reviews Chemistry .
Todo en seco
Los investigadores de Empa omitieron líquidos en su síntesis química y, en su lugar, unieron los materiales de partida a una superficie de oro en un vacío ultraalto. El material de partida (diisopropil-p-terfenilo) se puede observar descansando tranquilamente en el microscopio de efecto túnel enfriado antes de que los investigadores aumenten la temperatura.
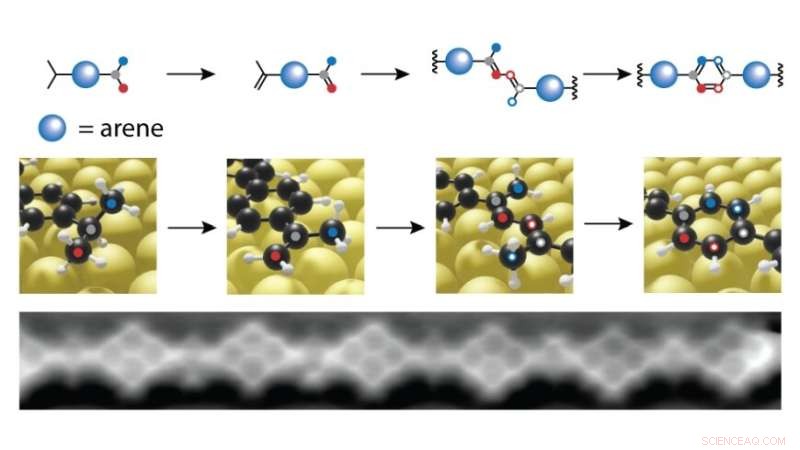
Síntesis química sobre una superficie de oro:se extrae un hidrógeno de los grupos isopropilo saturados. A 200 grados Celsius, los átomos de carbono (rojo y azul en la imagen de arriba) se combinan para formar un nuevo anillo de benceno. De esta manera, los bloques de construcción moleculares individuales se unen en una cadena de polímero, como se ve con el microscopio de fuerza atómica (abajo). Crédito:Empa
Sube la calefacción:movimiento en la pista de baile
A temperatura ambiente, todavía no sucede nada, pero a unos 200 grados centígrados, se produce una reacción sorprendente que nunca sucedería en líquidos:los dos grupos isopropilo, que normalmente están completamente inactivos desde el punto de vista químico, se combinan para formar un anillo de benceno. La razón:debido a la firme "adhesión" en la superficie de oro, primero se suelta un átomo de hidrógeno y luego se libera de la molécula. Esto crea radicales de carbono que esperan nuevos socios. Y hay muchos socios en la superficie de oro. A 200 grados centígrados, las moléculas vibran y realizan rápidas piruetas:hay mucho movimiento en la pista de baile dorada. Entonces, lo que pertenece a la unidad pronto se une.
Y de nuevo todo a cámara lenta
El emparejamiento en la superficie dorada tiene dos ventajas. En primer lugar, no hay necesidad de coerción:la reacción tiene lugar sin la mediación de ácidos bóricos o átomos de halógeno que salen volando. Es un acoplamiento que involucra solo hidrocarburos saturados. Los materiales de partida son baratos y fáciles de obtener, y no hay subproductos tóxicos.
La segunda ventaja es que los investigadores pueden observar cada paso de la reacción, otra cosa que no es posible con la química clásica "líquida". El equipo de Empa simplemente aumenta gradualmente el calentamiento de la superficie dorada. A 180 grados centígrados, las moléculas solo han conectado un brazo con sus vecinos, el segundo aún sobresale libremente en la pista de baile. Si ahora se enfría la superficie de oro dentro de un microscopio de efecto túnel, se pueden ver y "fotografiar" las moléculas justo antes de que se "casen". Esto es exactamente lo que hicieron los investigadores. Por lo tanto, el mecanismo de reacción se puede seguir en forma de "instantáneas".
Oportunidades para una 'nueva' química
Los investigadores y sus colegas esperan que surjan dos tipos de efectos del trabajo actual. En primer lugar, el "método de la instantánea" también podría ser adecuado para dilucidar mecanismos de reacción completamente diferentes. En Empa, se están desarrollando instrumentos que utilizan pulsos de láser ultracortos en un microscopio de efecto túnel para dilucidar dichas reacciones químicas paso a paso. Esto podría proporcionar información adicional sobre las reacciones químicas y pronto sacudirá muchas teorías antiguas.
Sin embargo, los resultados de la investigación "de la materia seca" también podrían ser útiles para desarrollar aún más la química "líquida". Hasta ahora, la mayoría de las reacciones documentadas en la literatura provienen de la química líquida clásica, y los investigadores de la sonda de exploración han podido recrear estos experimentos. En el futuro, ciertas reacciones también podrían diseñarse en el microscopio de efecto túnel y luego transferirse a la química líquida o gaseosa. Revelan el mecanismo de disociación de las moléculas de oxígeno en una superficie de plata