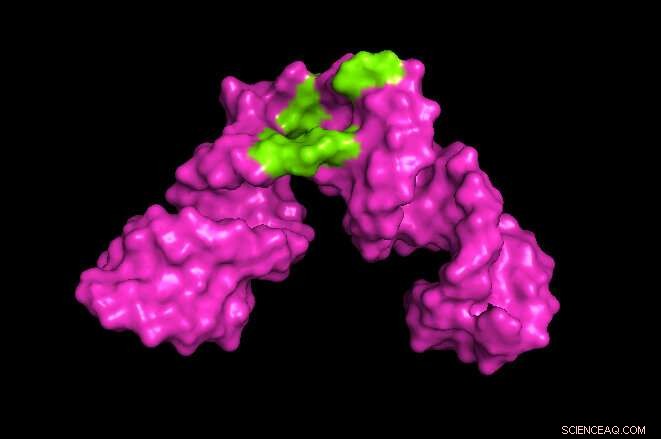
Los investigadores de la Universidad de Maryland desarrollaron un método para ampliar el alcance de la espectroscopia de resonancia magnética nuclear (RMN). En el ejemplo anterior, los investigadores pudieron crear una imagen en 3D que revelaba el sitio en un fragmento de ARN de la hepatitis donde pequeñas moléculas, como un medicamento, podían unirse (se muestra en verde). Crédito:Kwaku Dayie / Universidad de Maryland
Los científicos de la Universidad de Maryland han desarrollado un método para determinar las estructuras de grandes moléculas de ARN a alta resolución. El método supera un desafío que ha limitado el análisis 3D y la obtención de imágenes de ARN a solo moléculas pequeñas y fragmentos de ARN durante los últimos 50 años.
El nuevo método que amplía el alcance de la espectroscopia de resonancia magnética nuclear (RMN), permitirá a los investigadores comprender la forma y estructura de las moléculas de ARN y aprender cómo interactúan con otras moléculas. Los conocimientos proporcionados por esta tecnología podrían conducir a tratamientos terapéuticos dirigidos con ARN para enfermedades. El artículo de investigación sobre este trabajo fue publicado en la revista Avances de la ciencia el 7 de octubre 2020.
"El campo de la espectroscopia de resonancia magnética nuclear se ha atascado mirando cosas que son pequeñas, digamos 35 bloques de construcción de ARN o nucleótidos. Pero la mayoría de las cosas interesantes que son biológica y médicamente relevantes son mucho más importantes, 100 nucleótidos o más, "dijo Kwaku Dayie, profesor de química y bioquímica en la UMD y autor principal del artículo. "Entonces, ser capaz de romper el atasco de troncos y mirar cosas que son grandes es muy emocionante. Nos permitirá echar un vistazo a estas moléculas y ver lo que está sucediendo de una manera que no habíamos podido hacer antes ".
En espectroscopia de RMN, los científicos dirigen ondas de radio a una molécula, excitando los átomos e "iluminando" la molécula. Al medir los cambios en el campo magnético alrededor de los átomos excitados, la resonancia magnética nuclear, los científicos pueden reconstruir características como la forma, estructura y movimiento de la molécula. Los datos que esto produce se pueden usar para generar imágenes, al igual que las imágenes de resonancia magnética que se ven en la medicina.
Ordinariamente, Las señales de RMN de los muchos átomos de una molécula biológica, como el ARN, se superponen entre sí, haciendo el análisis muy difícil. Sin embargo, en los 1970s, Los científicos aprendieron a diseñar moléculas de ARN bioquímicamente para que funcionen mejor con la RMN reemplazando los átomos de hidrógeno con átomos de flúor magnéticamente activos. En moléculas relativamente pequeñas de ARN que constan de 35 nucleótidos o menos, los átomos de flúor se iluminan fácilmente cuando son golpeados por ondas de radio y permanecen excitados el tiempo suficiente para un análisis de alta resolución. Pero a medida que las moléculas de ARN se hacen más grandes, los átomos de flúor se iluminan solo brevemente, luego pierden rápidamente su señal. Esto ha impedido el análisis 3D de alta resolución de moléculas de ARN más grandes.
Trabajos anteriores de otros habían demostrado que el flúor continuaba produciendo una señal fuerte cuando estaba al lado de un átomo de carbono que contenía seis protones y siete neutrones (C-13). Entonces, Dayie y su equipo desarrollaron un método relativamente fácil para cambiar el C-12 natural en el ARN (que tiene 6 protones y 6 neutrones) a C-13 e instalar un átomo de flúor (F-19) directamente al lado.
Dayie y su equipo demostraron por primera vez que su método podía producir datos e imágenes iguales a los métodos actuales aplicándolo a piezas de ARN del VIH que contienen 30 nucleótidos. que había sido fotografiado previamente. Luego aplicaron su método a fragmentos de ARN de la hepatitis B que contienen 61 nucleótidos, casi el doble del tamaño de la espectroscopia de RMN anterior posible para el ARN.
Su método permitió a los investigadores identificar sitios en el ARN de la hepatitis B donde pequeñas moléculas se unen e interactúan con el ARN. Eso podría ser útil para comprender el efecto de posibles fármacos terapéuticos. El siguiente paso para los investigadores es analizar moléculas de ARN aún más grandes.
"Este trabajo nos permite ampliar lo que se puede enfocar, "Dijo Dayie." Nuestros cálculos nos dicen que, En teoria, podemos mirar cosas realmente grandes, como una parte del ribosoma, que es la máquina molecular que sintetiza proteínas dentro de las células ".
Al comprender la forma y estructura de una molécula, los científicos pueden comprender mejor su función y cómo interactúa con su entorno. Y lo que es más, esta tecnología permitirá a los científicos ver la estructura 3-D a medida que cambia, porque las moléculas de ARN en particular cambian de forma con frecuencia. Este conocimiento es clave para desarrollar terapias que se dirijan estrechamente a moléculas específicas de la enfermedad sin afectar las funciones celulares sanas.
"La esperanza es que si los investigadores conocen los rincones y recovecos de una molécula disfuncional, luego pueden diseñar medicamentos que llenen los rincones y recovecos para sacarlo de servicio, "Dijo Dayie." Y si podemos seguir estas moléculas a medida que cambian de forma y estructura, entonces su respuesta a posibles fármacos será un poco más predecible, y diseñar medicamentos que sean efectivos puede ser más eficiente ".