Un equipo codirigido por investigadores de Weill Cornell Medicine y el Centro del Genoma de Nueva York ha desarrollado un método avanzado para revelar cómo las mutaciones genéticas alteran el empaquetado normal del ADN. Estos cambios estructurales, que alteran los patrones de actividad genética en una célula, se conocen como cambios epigenéticos y pueden provocar enfermedades malignas.
El nuevo método, descrito en un artículo publicado en Nature , ofrece a los biólogos una poderosa herramienta que se puede aplicar en muchos campos de investigación, desde la biología celular básica hasta el estudio de cómo se originan los cánceres. Los investigadores demostraron el nuevo método usándolo para ilustrar cómo una mutación genética común ejerce sus efectos en dos cánceres de sangre raros.
"Esta nueva técnica debería permitir amplias exploraciones futuras de los vínculos entre las mutaciones y las alteraciones epigenéticas en el contexto de los cánceres y afecciones relacionadas", afirmó el autor principal del estudio, el Dr. Dan Landau, profesor de medicina en la División de Hematología y Oncología Médica de Weill. Cornell Medicine y miembro principal del cuerpo docente del Centro del Genoma de Nueva York.
El estudio fue codirigido por el Dr. Franco Izzo, investigador postdoctoral en el Laboratorio Landau durante el estudio y ahora profesor asistente en la Escuela de Medicina Icahn en Mount Sinai.
El nuevo logro es el último de una serie de innovaciones en perfiles unicelulares del grupo de investigación de Landau. Estos métodos, también llamados métodos "multiómicos unicelulares", permiten a los investigadores caracterizar mutaciones del ADN, patrones de actividad genética, proteínas de la superficie celular y otras capas de información, todo en una célula individual, utilizando la automatización para procesar muchos miles de células a la vez.
Por el contrario, los métodos más antiguos se utilizan en muestras masivas, que normalmente contienen mezclas de diferentes tipos de células, así como células mutadas y no mutadas, lo que limita en gran medida cualquier análisis.
En este caso, el equipo desarrolló un método unicelular más sensible y preciso para detectar mutaciones de interés en el ADN. Luego combinaron esto con una nueva técnica para mapear la "accesibilidad a la cromatina" de una célula (esencialmente los lugares donde el ADN está relativamente abierto y accesible para la transcripción genética) como una imagen amplia del estado epigenético de la célula.
Los investigadores denominaron estas técnicas emparejadas "Genotipado de loci específicos con accesibilidad a cromatina unicelular" o "GoT-ChA", y demostraron que podían integrar GoT-ChA con métodos unicelulares para perfilar otras capas de información como ARN y células. proteínas de superficie.
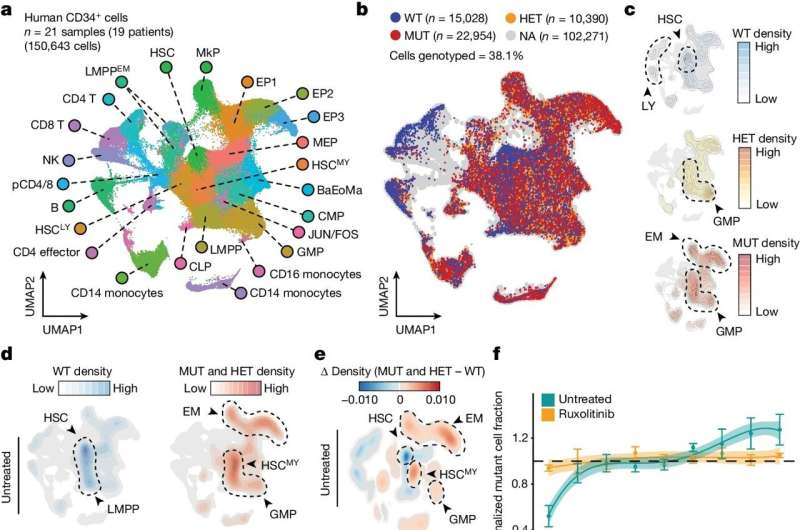
Los científicos demostraron el poder de su nuevo conjunto de herramientas usándolo para estudiar células sanguíneas extraídas de pacientes con dos cánceres sanguíneos poco comunes:policitemia vera y mielofibrosis. Estos cánceres suelen estar provocados por una mutación específica en un gen llamado JAK2, una mutación que se ha implicado en otras afecciones y que también se encuentra en muchas personas aparentemente sanas.
Ambos cánceres también presentan alteraciones del proceso normal de maduración de las células sanguíneas, lo que implica que la mutación JAK2 induce cambios epigenéticos significativos, pero las limitaciones de los métodos más antiguos significaron que estos cambios epigenéticos y otros efectos posteriores de la mutación no se comprendían bien. Con GoT-ChA, los investigadores pudieron catalogar estos efectos con gran detalle.
"Se pensaba que en la mielofibrosis, por ejemplo, la inflamación de la médula ósea estaba impulsada por el microambiente de la médula, pero descubrimos que los cambios inflamatorios en las células madre sanguíneas resultan directamente de la mutación JAK2 y también dependen del tipo de célula", dijo Landau, quien también miembro del Centro Oncológico Sandra y Edward Meyer y del Instituto Inglaterra de Medicina de Precisión en Weill Cornell Medicine.
Los resultados sugieren que nuevos fármacos inhibidores de JAK2 potentes, actualmente en desarrollo, podrían ser útiles en el tratamiento de pacientes con mielofibrosis, afirmó.
Landau señaló que GoT-ChA debería ser útil en general para estudiar condiciones en las que las mutaciones del ADN (que pueden surgir a lo largo de la vida por diversas razones) están presentes sólo en una minoría de células de un órgano y, por lo tanto, son difíciles o imposibles de estudiar con métodos tradicionales. , técnicas anteriores a la unicelular.
Los coautores del estudio, además de Izzo, fueron M.D.-Ph.D. el estudiante Robert Myers, el becario postdoctoral Saravanan Ganesan y el candidato a doctorado Levan Mekerishvili, todos del Laboratorio Landau.
Más información: Franco Izzo et al, Mapeo de genotipos a perfiles de accesibilidad de cromatina en células individuales, Naturaleza (2024). DOI:10.1038/s41586-024-07388-y
Información de la revista: Naturaleza
Proporcionado por la Universidad de Cornell