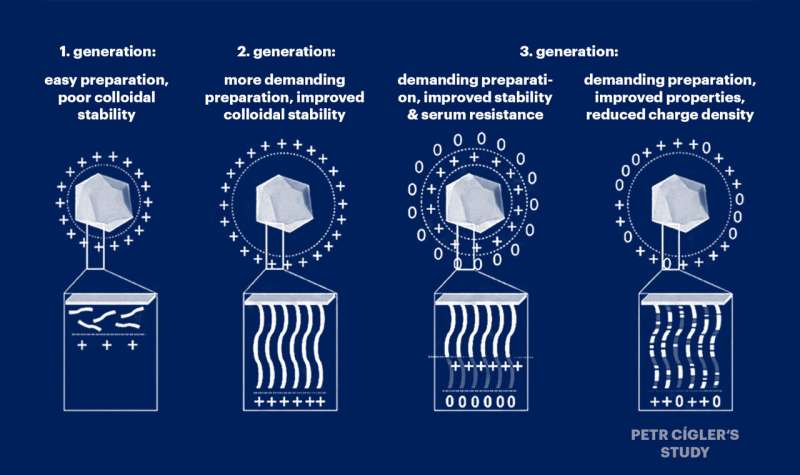
El Dr. Petr Cígler y sus colaboradores están trabajando en perfeccionar sistemas moleculares para transportar moléculas de ácido ribonucleico (ARN) al interior de las células. La cuestión de cómo administrar eficazmente ARN en un lugar designado del cuerpo para silenciar un gen que funciona mal es uno de los mayores desafíos del campo de la medicina genética en rápido desarrollo.
Ahora, investigadores del Instituto de Química Orgánica y Bioquímica de la Academia Checa de Ciencias (IOCB Praga) han dado otro paso significativo hacia la consecución de este objetivo. Han descrito en detalle la preparación de un novedoso nanomaterial vector compuesto para transportar ARN, en el que se centraron principalmente en garantizar su no toxicidad para las células. La razón es que la nocividad de los vectores de ácido nucleico conocidos hasta ahora representa un serio obstáculo para la expansión de la terapia génica.
Se ha publicado un artículo sobre el tema en Advanced Functional Materials. .
Petr Cígler y sus colegas partieron del supuesto de que la toxicidad de los vectores de ácidos nucleicos se debe a una acumulación excesiva de cargas positivas a lo largo de las cadenas de los polímeros portadores que se unen a los ácidos nucleicos. Por lo tanto, diluyeron sistemáticamente esta carga positiva con monómeros sin carga y descubrieron que su ligera dilución no perjudicaba la capacidad del sistema para transportar ácidos nucleicos.
En su minucioso estudio, también describen las circunstancias bajo las cuales se pueden preparar nuevos materiales para su uso en medicina genética. Los investigadores prestaron mucha atención a las condiciones en las que estas sustancias se unen más eficazmente a los ácidos nucleicos y en qué proporción estequiométrica.
Las células pueden regular la traducción de genes de ARNm a proteínas de varias formas. Una de ellas es silenciar un gen con la ayuda de una molécula de siRNA (pequeño ARN de interferencia). Esto bloquea la producción de la proteína diana, lo cual es especialmente útil si el gen que codifica está mutado o es defectuoso. Además, es posible intervenir si los mecanismos innatos de regulación de la traducción están alterados. En tal caso, se produce demasiada proteína en el cuerpo, lo que es perjudicial para su salud.
"La terapia génica no sólo es muy eficaz, sino que también tiene un objetivo preciso. Su mayor ventaja reside en el hecho de que se dirige con precisión a mutaciones o trastornos individuales sin peligro de equivocarse. Con el ARNip es posible atacar incluso una sola mutación". letra' de un gen", afirma Marek Kindermann, primer autor del estudio, enumerando las principales ventajas de la terapia génica. Actualmente, cinco medicamentos basados en ARNip están aprobados para su uso en todo el mundo y hay alrededor de una docena más en la "lista de espera".
El uso terapéutico del ARNip se ve obstaculizado por el hecho de que las moléculas de ARNip son inestables y, por tanto, se descomponen muy rápidamente en el cuerpo. Por lo tanto, expertos de todo el mundo están abordando el problema de cómo entregar el ARNip a un lugar designado y permitirle hacer su trabajo, que es detener o limitar la producción de una determinada proteína indeseable silenciando su gen.
Esta tarea también fue asumida por el equipo de Petr Cígler en el IOCB de Praga, junto con colegas del Instituto de Microbiología de la Academia Checa de Ciencias, dirigidos por la jefa del grupo de Nanomedicina, la Dra. Veronika Benson.
"Cada sistema de transporte está diseñado para cumplir dos objetivos básicos:en primer lugar, tiene la tarea de proteger a la molécula de la descomposición, y en segundo lugar, debe asegurar su transporte al interior de la célula para que llegue al citosol y cumpla su misión como droga allí", explica Petr Cígler.
"En nuestro estudio, analizamos con gran detalle las propiedades del sistema de transporte. Descendemos hasta el nivel de los detalles estructurales de las moléculas que interactúan con los ácidos nucleicos. Describimos las condiciones necesarias para que el ARNip se una con éxito al nanosistema de transporte y luego llega al espacio intracelular."
Los investigadores del IOCB de Praga están allanando el camino para el uso de partículas denominadas vectores no virales, que no utilizan virus para transportar el ARN. Han colocado todo el sistema de transporte, incluido el ácido nucleico, sobre la superficie de nanopartículas de diamante. Se trata de partículas portadoras marcadamente estables, que además emiten una forma especial de fluorescencia. Esto permite seguir su recorrido a través de los tejidos y controlar cómo se comportan dentro de las células.
Una complicación es que al cuerpo le resulta difícil deshacerse de los nanodiamantes, por lo que este método de terapia génica es adecuado principalmente para el tratamiento de heridas superficiales difíciles de curar. A este tipo de terapias, centradas en la curación de úlceras en las piernas de pacientes con diabetes, están destinados los nuevos nanomateriales de transporte, presentados en este y otros trabajos del equipo del Dr. Cígler y colaboradores.
Su último estudio en profundidad también fue posible gracias al proyecto AMULET, que se centra en el desarrollo de nanomateriales multiescala y reúne a ocho socios liderados por el Instituto de Química Física Jaroslav Heyrovský.
Más información: Marek Kindermann et al, Reglas de diseño para la interfaz nano-bio de nanodiamantes:implicaciones para la vectorización de ARNip, Materiales funcionales avanzados (2024). DOI:10.1002/adfm.202314088
Información de la revista: Materiales funcionales avanzados
Proporcionado por Instituto de Química Orgánica y Bioquímica del CAS