
Jennifer Roberts recolectó muestras de suelo en la región de Kongsfjorden de Svalbard, Noruega, que mostró que genes resistentes a los antibióticos se han transferido a poblaciones de microbios del suelo en una de las ubicaciones más remotas de la Tierra. Crédito:Jennifer Roberts / KU
El trabajo de un geólogo de la Universidad de Kansas en el remoto Alto Ártico de Noruega ha expuesto la asombrosa propagación mundial de microbios resistentes a los antibióticos, incluidas las "superbacterias" resistentes a múltiples fármacos, que podrían tener graves consecuencias para la salud humana en todo el mundo.
Jennifer Roberts, profesor y catedrático de geología en KU, comenzó investigando la geoquímica microbiana del deshielo del permafrost y su liberación de metano, un poderoso gas de efecto invernadero que acelera el cambio climático global.
Pero el análisis de seguimiento de las muestras de suelo que Roberts recogió en la región de Kongsfjorden de Svalbard, Noruega, también mostró que los genes resistentes a los antibióticos se han transferido a las poblaciones de microbios del suelo en una de las ubicaciones más remotas de la Tierra. Los hallazgos de Roberts y un equipo internacional de colegas del Reino Unido y China se acaban de publicar en la revista revisada por pares. Medio Ambiente Internacional .
"El estudio ofreció una buena oportunidad para analizar muestras de suelo en busca de genes de antibióticos con la hipótesis de que Svalbard era un lugar tan remoto y aislado". no encontraríamos ninguna evidencia de tales genes, ", Dijo Roberts." En contraste, encontramos bastantes, incluidos genes de superbacterias resistentes a los antibióticos, como el gen de Nueva Delhi, que surgió por primera vez en la India no hace mucho tiempo. Esto fue una sorpresa:los genes que encontramos claramente tuvieron un corto tiempo de transferencia entre su descubrimiento en la India y nuestro grupo que los detectó en el Ártico solo unos años más tarde ".
El equipo de investigación secuenció genéticamente el ADN de 40 muestras de suelo en ocho ubicaciones en Svalbard, encontrando 131 genes resistentes a los antibióticos. Un gen resistente a los antibióticos encontrado se llama blaNDM-1. Detectado inicialmente en Nueva Delhi en 2007, el gen desencadena la resistencia a los antibióticos carbapenémicos, un remedio de último recurso para una enfermedad infecciosa que de otro modo sería intratable. La propagación demostrada de blaNDM-1, en particular, es muy preocupante, llamando la atención sobre la creciente crisis de resistencia global a los antibióticos.
Los investigadores dicen que los genes resistentes a los antibióticos podrían haber tomado solo unos pocos caminos hacia el Ártico.
"Probablemente se originaron a partir de patógenos que fueron expuestos varias veces a diferentes tipos de antibióticos; así es como obtenemos estas cepas con resistencia aguda a los antibióticos". donde persisten incluso a pesar del uso de tratamientos de 'último recurso', ", Dijo Roberts." Algunos de los sitios donde encontramos la cepa genética de Nueva Delhi no están muy lejos de la base de investigación principal, por lo que existe la posibilidad de que haya desechos humanos involucrados. También observamos colonias de aves nidificantes en lugares de baja elevación, como pequeños lagos y otras fuentes de agua abierta durante el deshielo máximo, y ahí fue donde vimos las mayores concentraciones de estos genes. También los detectamos en lugares que no tenían aguas abiertas pero que tenían muchos animales pequeños como zorros, y puede trazar un vector entre un abrevadero o un lago pequeño donde hay muchas aves y pequeños mamíferos que van a beber y luego recogen los genes que estén allí ".
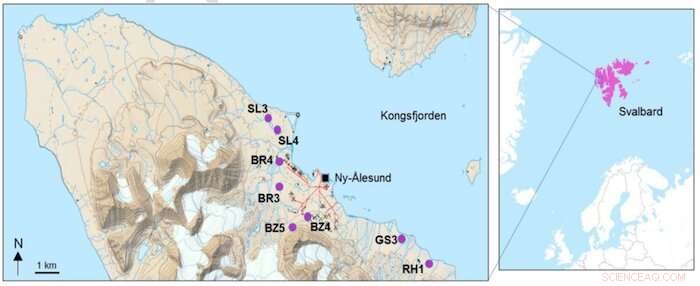
Lugares de muestreo de los ocho grupos de suelos en Kongsfjorden y la ubicación geográfica de Svalbard, Alto Ártico. Crédito:Jennifer Roberts / KU / mapa adaptado del Instituto Polar Noruego
Roberts, cuya experiencia investigadora es en hidroquímica y geoquímica microbiana, trabajó para desarrollar un punto de referencia para los genes resistentes a los antibióticos que se encuentran naturalmente en Svalbard para que el equipo pudiera distinguirlos de los genes resistentes a múltiples fármacos "extraños" transferidos al Ártico desde regiones donde se utilizan antibióticos en poblaciones humanas y animales para tratar enfermedades.
"Debido a que la migración de estos genes es motivo de gran preocupación, la siguiente pregunta es, '¿Estos genes resistentes a los antibióticos son nativos o se transfirieron?' ", Dijo." Mi función fue utilizar líneas de evidencia en nuestra investigación para ayudarnos a tener claro qué era un gen nativo que se desarrolló en el suelo y qué era traído de otras fuentes. Lo hicimos al observar los suministros nutricionales en el suelo, que son muy, muy bajo en estos suelos árticos. Luego pudimos vincular los genes resistentes a los antibióticos con lo que parece ser una nueva fuente de fosfato que llega del exterior, y la fuente más probable de fosfato son las heces. ya sea en aguas residuales humanas o, más que probable, guano de aves ".
Según Roberts, La resistencia a los antibióticos viajaba entre microbios a través de una "transferencia lateral de genes". En este proceso, los patógenos viajan al agua a través de las heces, mueren y liberan grandes cantidades de material genético libre en el agua. Este material genético no se degrada fácilmente, con el resultado de que otros organismos acaban recogiendo los genes, así como su resistencia.
"No es que tengamos algún tipo de comunidad robusta de E. coli u otro patógeno que viva en las aguas superficiales del Ártico, "Dijo Roberts." En cambio, algunos patógenos resistentes a los antibióticos se trajeron de fuentes externas, y ahora esa resistencia se ha dispersado a medida que otros organismos que ya estaban poblados en el medio ambiente recogen genes ".
Roberts dijo que el descubrimiento del equipo muestra que la resistencia a múltiples fármacos a los antibióticos ahora es de naturaleza global.
"Tenemos que recordar que tenemos antibióticos, como la penicilina, de microorganismos del suelo para empezar, ", dijo." Los microorganismos han utilizado la capacidad de resistencia para superar las inmunidades en el medio ambiente durante mucho tiempo, producir genes resistentes a los antibióticos que se consideran naturales y nativos. Pero con el uso de antibióticos fabricados para humanos y animales en todo el mundo, hemos visto una rápida evolución de genes resistentes. Encontramos genes resistentes a los antibióticos tanto nativos como evolucionados en el Ártico. La preocupación es que con la resistencia que se extiende a esta escala, es posible que nos estemos acercando a una era posterior a los antibióticos en la que ninguno de nuestros antibióticos funciona porque los patógenos que estamos tratando de combatir han recogido genes resistentes a través de la evolución o la transferencia lateral ".
Roberts dijo que los hallazgos del equipo muestran la importancia de una administración más cuidadosa del uso de antibióticos y la necesidad de un mejor tratamiento de las aguas residuales en todo el mundo.
"Nuestro uso de antibióticos por parte de humanos y animales puede tener impactos que van más allá de nosotros mismos y de nuestras comunidades locales; son globales, "Es realmente importante para nosotros comenzar a pensar en la administración del sistema de agua y el uso de antibióticos de manera global, y comenzar a reducir y controlar parte de la propagación que claramente no está controlada en este momento".