La picrotoxina, una toxina de origen vegetal que los pescadores asiáticos han utilizado tradicionalmente para paralizar y capturar peces, se ha considerado durante mucho tiempo como un posible punto de partida para nuevas terapias humanas y otros productos neuroactivos.
Sin embargo, se han logrado pocos avances debido a la inestabilidad química y la toxicidad de la picrotoxina y la dificultad de elaborar y modificar su compleja estructura. Sin embargo, los químicos de Scripps Research han encontrado una forma relativamente sencilla de crear versiones de picrotoxina con propiedades mejoradas.
En un estudio publicado en Nature Communications , los investigadores demostraron que las variantes químicas cercanas de la picrotoxina que contienen una única pequeña modificación tienen una mejor estabilidad química, son mucho más fáciles de producir y modificar y son más seguras para los humanos. Esto abre la puerta al desarrollo de nuevos medicamentos neurológicos, pesticidas más seguros e incluso tratamientos antiparasitarios.
"Sólo una pequeña alteración del producto natural le confiere propiedades que han sido difíciles de alcanzar durante décadas", afirma el autor principal del estudio, Ryan Shenvi, Ph.D., profesor del Departamento de Química de Scripps Research.
El primer autor fue Guanghu Tong, Ph.D., investigador asociado postdoctoral en el Laboratorio Shenvi durante el estudio.
La picrotoxina proviene de las semillas, a menudo llamadas semillas de "baya de pescado" debido a su uso por parte de los pescadores, de Anamirta cocculus, una planta que se encuentra en partes del sudeste asiático y la India. La toxina bloquea potentemente la actividad de los receptores neuronales que se encuentran en la mayoría de los organismos superiores.
En los mamíferos, estos se llaman GABAA receptores, y existen en todo el cerebro, en gran medida para evitar que otras neuronas se vuelvan hiperactivas. Incluso en pequeñas dosis, el bloqueo de estos receptores por parte de la picrotoxina puede causar convulsiones e interrumpir fatalmente las señales nerviosas que controlan la respiración.
Puede parecer contradictorio que los químicos recurran a los venenos para fabricar nuevos medicamentos, pero muchas toxinas vegetales, además de alcanzar objetivos deseables, ya tienen buenas propiedades similares a las de los fármacos, como llegar a sus objetivos mediante dosificación oral.
En el caso de la picrotoxina, a los químicos les gustaría modificarla para desarrollar medicamentos para trastornos psiquiátricos y neurológicos, pesticidas y medicamentos antiparasitarios seguros y eficaces, y herramientas de laboratorio para manipular el GABA con precisión A receptores. El problema ha sido que otras propiedades químicas de la picrotoxina, como su dificultad de síntesis y su tendencia a reaccionar con disolventes comunes, la han hecho extraordinariamente difícil de domesticar.
El laboratorio de Shenvi utiliza técnicas de química orgánica para superar estos desafíos y encontrar formas de mejorar los productos naturales. Durante años, él y su equipo se han centrado en moléculas que se dirigen al GABAA. receptores y, en 2020, informaron la síntesis orgánica de picrotoxina más corta jamás realizada.
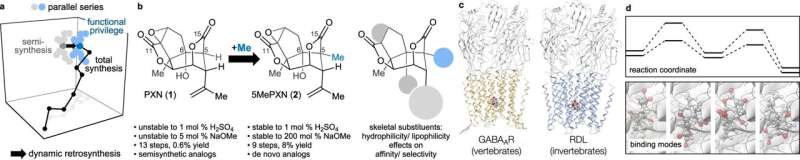
En ese estudio, descubrieron que podían sintetizar mucho más fácilmente un compuesto que era casi igual a la picrotoxina. 5La me-picrotoxina, como la llamaron, aún podría unirse al GABAA receptores y sólo se diferenciaba de su primo químico por la adición de un grupo de átomos, llamado grupo metilo, en una posición clave de la molécula. Dado este cambio estructural, el equipo de Shenvi investigó las nuevas propiedades de la picrotoxina 5Me para el nuevo estudio.
El equipo sintetizó dos conjuntos paralelos de variantes de picrotoxina y 5Me-picrotoxina, determinando cómo la ausencia o presencia del grupo metilo cambia la estabilidad de la molécula y la selectividad de unión al receptor.
Descubrieron que la versión metilada es químicamente mucho más estable, con una vida media en el torrente sanguíneo que parece ser casi el triple que la de la picrotoxina ordinaria. También descubrieron que la 5Me-picrotoxina es mucho menos propensa a reaccionar con disolventes comunes, incluidos alcoholes y ácidos. Los coautores Shuming Chen, Ph.D., profesora asistente de química en Oberlin College, y Anna Crowell, miembro de su laboratorio, explicaron esto utilizando modelos computacionales.
Otra sorpresa fue que la versión metilada tiene menor potencia contra el GABAA de mamíferos. receptores al mismo tiempo que conserva una alta potencia contra las versiones del receptor para insectos, justo lo que uno querría para un compuesto seguro para matar insectos.
"El hecho de que la picrotoxina se dirija a una familia de receptores que incluye GABAA Los receptores se conocen desde hace varias décadas, pero esta es la primera vez que hemos podido cambiar su selectividad para esos receptores", dice Tong.
Los experimentos con variantes de picrotoxina y receptores de insectos fueron realizados por investigadores colaboradores de Corteva Agriscience, desarrolladores de productos para el control de plagas. Los modelos creados para el estudio por el químico computacional de Corteva, Avery Sader, Ph.D., sugieren otras formas de modificar la 5Me-picrotoxina para hacerla más selectiva para las plagas de insectos y, por lo tanto, más segura para los humanos.
Los investigadores planean continuar sintetizando e investigando nuevas variantes de la picrotoxina 5Me por su potencial para desarrollarse en nuevos medicamentos y otros productos.
Más información: Guanghu Tong et al, La metilación de C5 confiere accesibilidad, estabilidad y selectividad a la picrotoxina, Nature Communications (2023). DOI:10.1038/s41467-023-44030-3
Proporcionado por el Instituto de Investigación Scripps