
Figura 1. Un polvo de alúmina disponible comercialmente. Crédito:Universidad de Kobe
Una colaboración de investigación internacional entre la Universidad de Kobe y la Universidad Médica de Mongolia Interior ha desarrollado un método simple, de bajo costo y relativamente respetuoso con el medio ambiente para sintetizar derivados de difenilmetanol utilizando alúmina de China. Los derivados del difenilmetanol se utilizan como materia prima en la fabricación de perfumes y productos farmacéuticos, entre otros.
Los investigadores descubrieron que la alúmina se puede reutilizar repetidamente para esta reacción si se lava con agua y se seca entre usos. Este reciclaje reduce tanto la necesidad de más alúmina como la cantidad de residuos producidos, reduciendo los costes de síntesis y el impacto sobre el medio ambiente. A medida que la conciencia ambiental global continúa aumentando, los investigadores esperan que este nuevo método de síntesis química contribuya a lograr una sociedad neutral en carbono y lograr los ODS.
Este descubrimiento fue realizado por un grupo de investigación internacional, que incluía al profesor asociado Tsuda Akihiko de la Facultad de Ciencias de la Universidad de Kobe (quien también es profesor invitado en la Universidad Médica de Mongolia Interior) e investigadores de la Universidad Médica de Mongolia Interior, incluido el profesor Chaolu Eerdun (quien obtuvo su doctorado de la Escuela de Graduados en Ciencias de la Universidad de Kobe) y el profesor Liang Fengying.
Se presentó una solicitud de patente para este método en China en abril de 2021, con una solicitud de reivindicación de prioridad realizada en septiembre del mismo año. Posteriormente, los resultados de esta investigación se publicaron en línea en la revista académica ChemistryOpen el 18 de mayo de 2022.
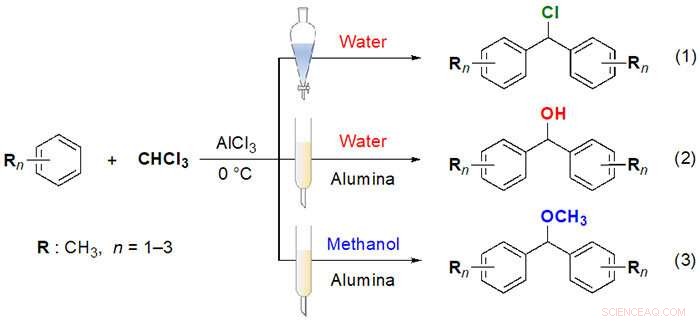
Figura 2. El nuevo método sintético para producir derivados de difenilmetanol desarrollado en este estudio:Conversión de producto utilizando un catalizador de alúmina. Crédito:Universidad de Kobe
Alúmina (Al2 O3 ) es un óxido de aluminio utilizado principalmente como materia prima para la producción de aluminio (Figura 1). Sin embargo, también se utiliza como catalizador en el campo de la química sintética orgánica. Se utiliza principalmente para reacciones que requieren condiciones duras (como alta temperatura o alta presión). Sin embargo, la alúmina no es un catalizador de uso común por varias razones, una de las cuales es que solo se puede usar para una pequeña variedad de reacciones químicas. La alúmina también se utiliza para adsorber impurezas en el campo de la síntesis orgánica y como sustancia de fase estacionaria en la cromatografía. Sin embargo, cuestiones como su elevado coste como materia prima y la gran cantidad de residuos no combustibles que genera, hacen que exista una tendencia a su sustitución por sustitutos. En estas circunstancias, el profesor Tsuda dirigió un grupo de investigación en la Universidad de Mongolia Interior (China) que logró desarrollar un método nuevo y sostenible de síntesis orgánica utilizando alúmina, que China produce en grandes cantidades.
El profesor Tsuda y el equipo de la Universidad Médica de Mongolia Interior descubrieron una forma sencilla, económica y respetuosa con el medio ambiente de sintetizar derivados de difenilmetanol (que son materiales de partida en la producción de fragancias y productos farmacéuticos) utilizando alúmina china como catalizador y adsorbente (Figura 2 ). Utilizando cloruro de aluminio (AlCl3 ) como catalizador, los solventes orgánicos genéricos tolueno, xileno y trimetilbenceno se hicieron reaccionar con cloroformo. Si la sustancia resultante se trata posteriormente con agua, se obtiene principalmente un producto de cloración. Sin embargo, los investigadores descubrieron que si la misma sustancia resultante se deposita sobre alúmina que contiene agua, se pueden obtener derivados del difenilmetanol. También encontraron que si la sustancia resultante se deposita sobre alúmina que contiene metanol, se obtiene un sustituto del metanol. Se cree que cuando la sustancia se adsorbe en la alúmina, reacciona con el agua o el alcohol que contiene para producir el producto final respectivo.
Además, el grupo de investigación descubrió que se podía obtener un producto de alta pureza incluso si estaba adsorbido por alúmina que se había utilizado previamente como catalizador o era un subproducto impuro. Usando el método mencionado anteriormente, es posible sintetizar selectivamente tres productos diferentes.

Figura 3. Elaboración del producto formado tras la alquilación de Friedel-Crafts mediada por AlCl3 con alúmina e inicialización de la alúmina utilizada. Crédito:Universidad de Kobe
Sin embargo, la alúmina comercial es comparativamente cara, lo que dificultaría la implementación de reacciones como esta que requieren grandes cantidades a escala industrial. Con esto en mente, los investigadores intentaron reutilizar la alúmina después de enjuagarla con agua y dejarla secar, y descubrieron que conservaba sus propiedades catalíticas y adsorbentes (Figura 3). Este proceso de reciclaje se puede realizar repetidamente, lo que reduce en gran medida el costo de los materiales y la cantidad de desechos. Para los experimentos de síntesis en el laboratorio, la cantidad de alúmina utilizada fue del orden de unos pocos gramos a decenas de gramos. Es una reacción segura, de alto rendimiento y que requiere poco tiempo para completarse (varias horas), por lo que esta aplicación de la alúmina a nivel académico podría expandirse a diversos campos de la industria química. Se espera que pueda proporcionar a la sociedad un método de síntesis orgánica práctico y sostenible.
At 0°C, aluminum chloride (1.1 g, 8 mmol) was added to a mixture of chloroform (30 mL, 0.37 mol) and an aromatic substrate such as p-xylene (1mL, 8mmol), and then stirred for six hours. After this, the resulting sample solution was dropped into a commercially available alumina column (water content ~1 wt%) and subjected to column chromatography with a dry chloroform/ethyl acetate (1:1) eluent. This chromatography revealed that a 94% yield of diphenylmethanol derivatives can be produced using this method. Refinement processes such as recrystallization can be performed as required to obtain a highly pure end product.
As for the mechanism behind this, it is thought that the chloroform and the aromatic substrate undergo an aluminum chloride-mediated Friedel-Crafts reaction. The resulting reactant and aluminum chloride are adsorbed by the alumina and are subsequently hydrolyzed by the water molecules in the alumina, leading to the formation of the end product. After removing the end product from the alumina, the alumina can be recycled by first washing away the adsorbed compounds, salts and solvents remaining in the alumina and then drying it. Consequently, the alumina can be reused as a catalyst for this reaction again and again.
The novel catalytic, adsorbent and recyclable properties of alumina discovered through this research have potential applications to the organic synthesis of compounds other than diphenylmethanol derivatives. The goal is to greatly expand this reaction's range of applications to develop a more general synthesis method that can be used to produce various useful chemicals.
Amidst rising global environmental awareness, it is hoped that the new chemical reaction developed in this study will become a novel method of synthesizing chemical products which will contribute towards recycling efforts, carbon neutrality and the SDGs. It is predicted to bring about fresh innovation in the organic synthesis and organic chemical industries. It is hoped that continued development of this method through the international research collaboration with China, the world's number one producer of alumina, will result in highly practical large-scale implementation. Converting CO2 to formic acid using an alumina-supported, iron-based compound