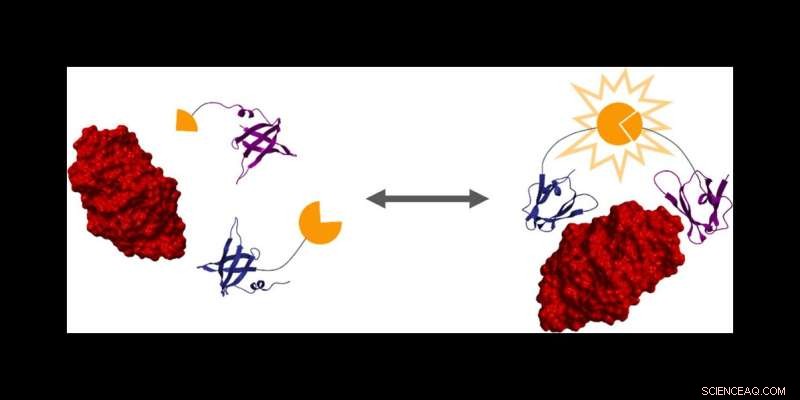
Dos proteínas aglutinantes (azul y púrpura) están diseñadas para unirse a una proteína objetivo particular (roja), como la lisozima. Solo en presencia de la proteína objetivo, las dos mitades de la enzima luciferasa dividida (amarilla) se unen para crear una señal bioluminiscente. Al analizar esta interacción, los investigadores están desarrollando modelos matemáticos que pueden predecir y controlar la diferenciación. Crédito:Nikki McArthur y Carlos Cruz-Terán
Las células están constantemente tomando decisiones que conducen a la diferenciación. Por ejemplo, las células de un embrión toman una serie de decisiones que determinan si se convertirán en neuronas en algunos casos y en células musculares en otros. ¿Cómo toman las células estas decisiones?
Investigadores de la Universidad Texas A&M y la Universidad Estatal de Carolina del Norte están determinando cómo las células facilitan los procesos de toma de decisiones. A través de este trabajo, esperan medir con precisión las concentraciones de proteínas de señalización vital específicas dentro de los tejidos celulares. Además, utilizarán las medidas para desarrollar modelos matemáticos que puedan predecir y controlar la diferenciación celular.
Este estudio fue publicado recientemente en ACS Omega .
"Queremos comprender las decisiones de diferenciación, para poder aprovecharlas en última instancia", dijo el Dr. Gregory Reeves, profesor asociado en el Departamento de Ingeniería Química Artie McFerrin en Texas A&M. "Somos herramientas de ingeniería para comprender la diferenciación celular y describir los procesos a través de ecuaciones. Para realizar estas tareas, necesitamos comprender las concentraciones de las proteínas en los tejidos vivos".
Sin embargo, determinar las concentraciones de proteínas clave de señalización puede ser extremadamente difícil. Para combatir este problema, Reeves colaboró con investigadores de la Universidad Estatal de Carolina del Norte que utilizaron un marco experimental y analítico para desarrollar ensayos de mezcla y lectura. Los ensayos de mezcla y lectura significan que los reactivos críticos se colocan en combinación con una célula lisada, lo que permite la detección de luminiscencia si la proteína objetivo está presente.
Luego, los investigadores utilizaron una técnica de ingeniería de proteínas para crear dos proteínas que se unen fuertemente a una proteína objetivo, en este caso, la lisozima. Estos dos aglutinantes de proteínas se fusionan con dos mitades de luciferasa, una enzima que crea bioluminiscencia, como se vería en una luciérnaga.
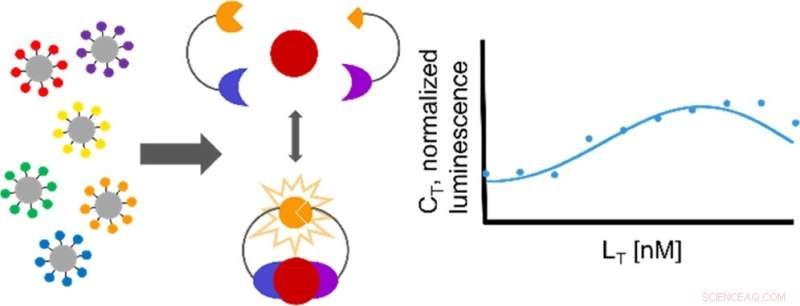
Gráficamente abstracto. Crédito:ACS Omega (2022). DOI:10.1021/acsomega.2c02319
"Cuando la proteína objetivo se une a los dos aglutinantes de proteínas diseñados, une las dos mitades de la luciferasa para crear bioluminiscencia, que podemos usar para tomar medidas", dijo Reeves.
Los investigadores del laboratorio de Reeves analizaron un modelo matemático de este método para predecir la cantidad de bioluminiscencia resultante de los eventos de unión, lo que les permitió determinar la sensibilidad del ensayo. Esto, a su vez, ayudará a los investigadores a obtener una comprensión más profunda de cómo y por qué las células toman decisiones de diferenciación.
Los impactos más amplios de este estudio incluyen el uso de esta técnica para detectar la presencia de proteínas objetivo, como anticuerpos o marcadores de cáncer regulados al alza, en un lisado celular.
"Otras aplicaciones, que usaremos en mi laboratorio, incluyen permitirnos medir limpiamente algunas proteínas que no se podían medir previamente en tejidos vivos", dijo Reeves.
Los investigadores también esperan seguir aplicando estos métodos a otras clases de moléculas que son difíciles de detectar en tejidos vivos, como el ARNm.
Este trabajo es en colaboración con la autora principal Nikki McArthur, junto con el Dr. Balaji Rao, el Dr. Carlos Cruz-Teran y Apoorva Thatavarty del Departamento de Ingeniería Química y Biomolecular de la Universidad Estatal de Carolina del Norte. La proteína controlada tanto por la luz como por la temperatura puede informar las vías de señalización celular