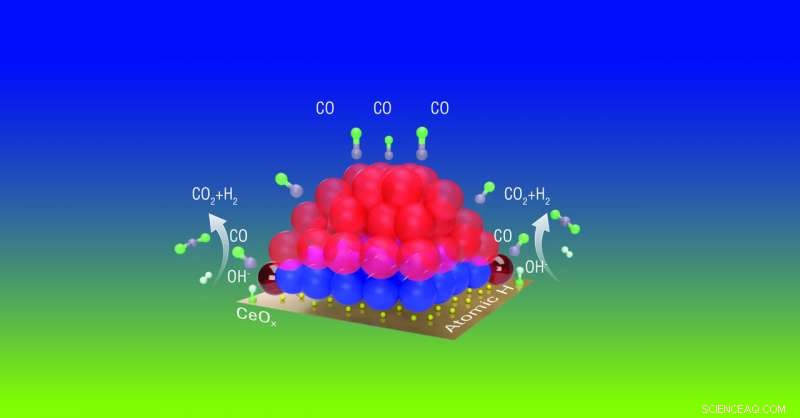
Los científicos que estudian un catalizador de reacción de cambio de gas de agua hecho de átomos de platino (rojo y azul) en un óxido de cerio (C mi O X ) descubrió que solo algunos átomos de platino alrededor de la periferia de la nanopartícula (rojo oscuro brillante) se activan para participar en la reacción. Estos átomos de platino activados transfieren oxígeno de los grupos OH (originalmente de las moléculas de agua) al monóxido de carbono (CO), transformándolo en CO 2 , dejando que el H se combine con el hidrógeno atómico para formar H 2 . Comprender esta dinámica puede ayudar a los científicos a diseñar catalizadores que requieran menos átomos de platino. Crédito:Laboratorio Nacional Brookhaven
Científicos del Laboratorio Nacional Brookhaven del Departamento de Energía de EE. UU. Universidad de Stony Brook (SBU), y otras instituciones colaboradoras han descubierto dinámicas, Detalles a nivel atómico de cómo funciona un importante catalizador a base de platino en la reacción de cambio de gas de agua. Esta reacción transforma el monóxido de carbono (CO) y el agua (H 2 O) en dióxido de carbono (CO 2 ) y gas hidrógeno (H 2 ):Un paso importante en la producción y purificación de hidrógeno para múltiples aplicaciones, incluido el uso como combustible limpio en vehículos de pila de combustible, y en la producción de hidrocarburos.
Pero debido a que el platino es raro y caro, Los científicos han estado buscando formas de crear catalizadores que utilicen menos de este metal precioso. Comprender exactamente lo que hace el platino es un paso esencial.
El nuevo estudio, publicado en Comunicaciones de la naturaleza , identifica los átomos involucrados en el sitio activo del catalizador, resolver informes anteriores contradictorios sobre cómo funciona el catalizador. Los experimentos proporcionan evidencia definitiva de que solo ciertos átomos de platino juegan un papel importante en la conversión química.
"Parte del desafío es que el catalizador en sí tiene una estructura compleja, "explicó el autor principal, Yuanyuan Li, un científico investigador en el Departamento de Ciencia de Materiales e Ingeniería Química de SBU que tiene una cita como invitado en la División de Química de Brookhaven Lab y trabaja bajo la dirección de Anatoly Frenkel, designado conjuntamente por Brookhaven / SBU.
"El catalizador está hecho de nanopartículas de platino (grupos de átomos de platino) asentadas sobre una superficie de óxido de cerio (ceria). Algunos de esos átomos de platino están en la superficie de la nanopartícula, algunos están en el núcleo; algunos están en la interfaz con ceria, y algunos de ellos están en el perímetro (los bordes exteriores) de esa interfaz, "Dijo Li." Esas posiciones y cómo colocas las partículas en la superficie pueden influir en qué átomos interactuarán con el soporte o con las moléculas de gas, porque algunos están expuestos y otros no ".
Experimentos anteriores habían producido resultados contradictorios sobre si las reacciones ocurren en las nanopartículas o en átomos de platino aislados individuales, y si los sitios activos están cargados positiva o negativamente o son neutrales. Los detalles de cómo el soporte de ceria interactúa con el platino para activarlo para la actividad catalítica tampoco estaban claros.
"Queríamos abordar estas preguntas, ", dijo Li." Para identificar el sitio activo y determinar lo que realmente está sucediendo en este sitio, es mejor si podemos investigar este tipo de catalizador a nivel atómico, "ella anotó.
El equipo, que incluía científicos del Centro de Nanomateriales Funcionales (CFN) de Brookhaven y otras instituciones en los EE. UU. y Suecia, utilizó una variedad de técnicas para hacer precisamente eso. Estudiaron el catalizador en condiciones de reacción y, inesperadamente, capturó un efecto peculiar que se produjo cuando los catalizadores alcanzaron su estado activo en condiciones de reacción.
"Los átomos de platino en el perímetro de las partículas estaban 'bailando' dentro y fuera de foco en un experimento de microscopía electrónica llevado a cabo por nuestros colaboradores, mientras que el resto de los átomos eran mucho más estables, ", Dijo Frenkel. Tal comportamiento dinámico no se observó cuando algunos de los reactivos (CO o agua) se eliminaron de la corriente de moléculas en reacción.
"Descubrimos que solo los átomos de platino en el perímetro de la interfaz entre las nanopartículas y el soporte de ceria proporcionan la actividad catalítica, "Dijo Li." Las propiedades dinámicas en estos sitios perimetrales permiten que el CO obtenga oxígeno del agua para que pueda convertirse en CO 2 , y el agua (H 2 O) pierde oxígeno para convertirse en hidrógeno ".
Ahora que los científicos saben qué átomos de platino juegan un papel activo en el catalizador, pueden diseñar catalizadores que contengan solo esos átomos de platino activos.

El autor principal, Yuanyuan Li, un científico investigador en el Departamento de Ciencia de Materiales e Ingeniería Química de la Universidad de Stony Brook que tiene una cita como invitado en la División de Química del Laboratorio de Brookhaven, realiza un análisis de una muestra utilizando un espectrómetro de infrarrojos. Crédito:Laboratorio Nacional Brookhaven
"Podríamos suponer que todos los átomos de platino de la superficie están funcionando, pero no lo son, "Dijo Li." No los necesitamos a todos, solo los activos. Esto podría ayudarnos a hacer que el catalizador sea menos costoso al eliminar los átomos que no están involucrados en la reacción. Creemos que este mecanismo puede generalizarse a otros sistemas y reacciones catalíticas, " ella añadió.
Detalles experimentales
Las "instantáneas" de microscopía electrónica en el CFN y en el Instituto Nacional de Estándares y Tecnología revelaron la naturaleza dinámica de los átomos de platino del perímetro. "En algunas imágenes, el sitio del perímetro está ahí, puedes verlo, pero en algunas imágenes no está ahí. Esto es evidencia de que estos átomos son muy dinámicos, con alta movilidad, "Dijo Li.
Los estudios de espectroscopía infrarroja (IR) en la División de Química de Brookhaven revelaron que la apariencia de los sitios del perímetro coincidía con "vacantes de oxígeno", una especie de defecto en la superficie del óxido de cerio. Estos estudios también mostraron que el CO tendía a migrar a través de la superficie de las nanopartículas de platino hacia los átomos del perímetro. y que los grupos hidroxi (OH) permanecieron en el soporte de ceria cerca de los átomos de platino del perímetro.
"Así que parece que los átomos de platino del perímetro traen los dos reactivos, CO y OH (de las moléculas de agua) juntos, "Dijo Li.
Los estudios de espectroscopía de fotoelectrones de rayos X en Química revelaron que los átomos de platino del perímetro también se activaron, cambiaron de un estado no metálico a uno metálico que podría capturar átomos de oxígeno de los grupos OH y entregar ese oxígeno al CO ". los sitios permiten que tenga lugar la reacción, "Dijo Li.
Un conjunto final de experimentos —estudios de espectroscopía de absorción de rayos X realizados en la Fuente de Fotones Avanzada (APS) en el Laboratorio Nacional Argonne del DOE — mostró los cambios estructurales dinámicos del catalizador.
"Vemos que la estructura está cambiando bajo las condiciones de reacción, "Dijo Li.
Esos estudios también revelaron un enlace inusualmente largo entre los átomos de platino y el oxígeno en el soporte de ceria. sugiriendo que algo invisible a los rayos X ocupaba espacio entre los dos.
"Creemos que hay algo de hidrógeno atómico entre la nanopartícula y el soporte. Los rayos X no pueden ver átomos ligeros como el hidrógeno. En condiciones de reacción, esos hidrógenos atómicos se recombinarán para formar H 2 , " ella añadió.
Las características estructurales y los detalles de cómo los cambios dinámicos están conectados con la reactividad ayudarán a los científicos a comprender el mecanismo de trabajo de este catalizador en particular y potencialmente diseñar otros con mejor actividad a menor costo. Las mismas técnicas también se pueden aplicar a estudios de otros catalizadores.