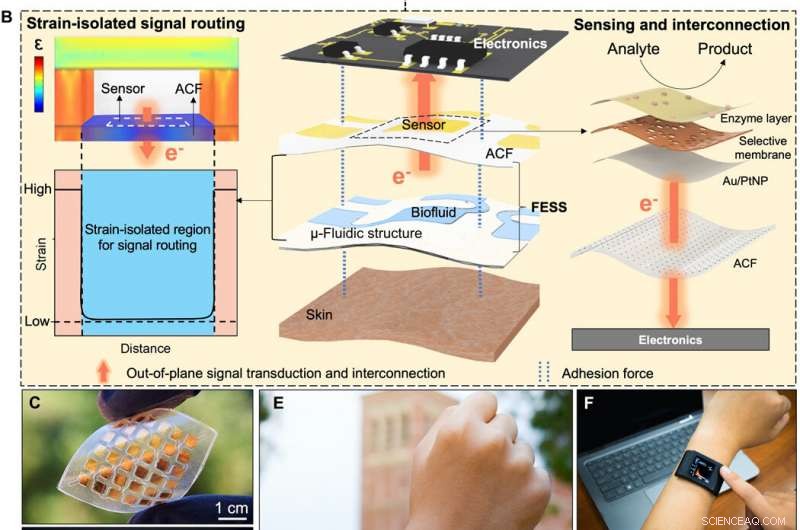
Justificación del diseño FESS, implementación, y aplicación. (A) Esquema de la vía de entrega de información de biomarcadores habilitada por el FESS, ilustrando el muestreo, sintiendo y enrutamiento de información de biomarcadores recuperada epidérmicamente para leer la electrónica a través de una única entidad. (B) Justificación del diseño de la FESS. (C) Implementación representativa del FESS, demostrando flexibilidad y sin interconexión en el plano. (D) Familia representativa de dispositivos FESS, que contiene 1 × 2, 3 × 3, y conjuntos de electrodos de 6 × 6. (E) Reloj inteligente desarrollado a medida y habilitado para FESS para el monitoreo de biomarcadores. (F y G) Despliegue del reloj inteligente habilitado para FESS en configuraciones estacionarias (F) y de ejercicio de alta intensidad (G). (Crédito de la foto:Peterson Nguyen, Kaili Chiu, Yichao Zhao, Universidad de California, Los Ángeles.) Crédito: Avances de la ciencia , doi:10.1126 / sciadv.aaz0007
En un nuevo estudio publicado en Avances de la ciencia , Yichao Zhao y un equipo de investigación en bioelectrónica integrada y materiales e ingeniería en los EE. UU. Diseñaron un dispositivo desechable, sistema de detección electroquímico autónomo (FESS). El FESS les permitió realizar una estrategia de diseño a nivel de sistema para abordar los desafíos de los biosensores portátiles en presencia de movimiento y permitir una integración perfecta con la electrónica de consumo. El equipo desarrolló un reloj inteligente habilitado para FESS, con muestreo de sudor, detección electroquímica y visualización o transmisión de datos, dentro de una plataforma portátil autónoma. El equipo utilizó el reloj inteligente FESS para monitorear los perfiles de los metabolitos del sudor entre individuos en entornos sedentarios y de ejercicio muy intensivo.
La infraestructura de Internet de las cosas (IOT) se puede utilizar en dispositivos electrónicos de consumo portátiles para transformar la medicina personalizada y de precisión mediante la recopilación de datos fisiológicamente relevantes con una mínima intervención del usuario. Los científicos suelen utilizar sensores físicos en plataformas portátiles comerciales para rastrear la actividad física y los signos vitales de un usuario. Sin embargo, para obtener información sobre la química dinámica del cuerpo, Los investigadores requieren superficies de detección electroquímica para apuntar a las moléculas de biomarcadores dentro de los fluidos corporales recuperados de forma no invasiva, como el sudor. Para lograr esto, Es fundamental diseñar con precisión la ruta de entrega de información desde la piel hasta una unidad de lectura. Para detección electroquímica, la vía de entrega de información debe muestrear y entregar el biofluido rico en biomarcadores a la superficie del sensor en una estructura de microfluidos, seguido de la transducción de señales a través de elementos interconectados a la electrónica de lectura. La señal debe mantenerse a lo largo de esta vía en presencia de tensión inducida por el movimiento.
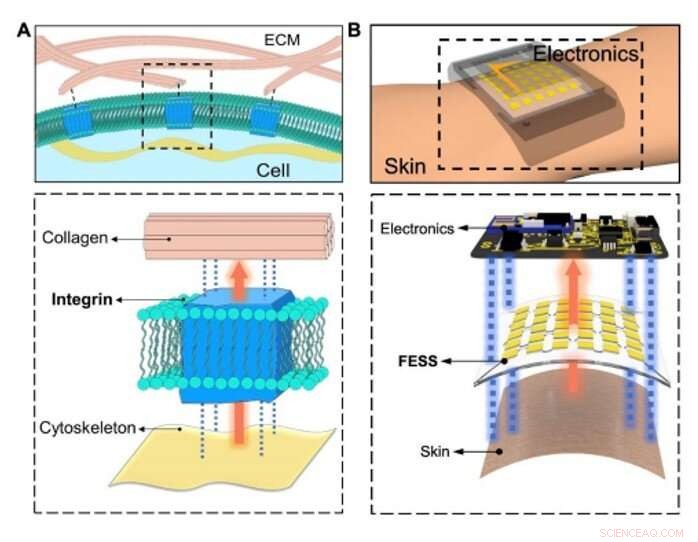
Detección e interconexión de señales in situ bioinspiradas. (A) Ilustración conceptual del intercambio de información fisiológica entre matrices intracelulares / extracelulares facilitado por moléculas adhesivas celulares (integrina) a través de la detección, interconexión de señales fuera del plano, y adhesión de doble cara. (B) Detección in situ, interconexión de señales fuera del plano, y adhesión de doble cara habilitada por FESS, como una sola entidad, colocado entre la piel y la electrónica. Crédito:Science Advances, doi:10.1126 / sciadv.aaz0007
En este trabajo, Zhao y col. desarrolló el sistema de detección electroquímica independiente (FESS) y lo adhirió simultáneamente a la piel y a la electrónica utilizando fuerzas de adhesión de doble cara sin conectores rígidos. El FESS muestreó y dirigió biofluidos recuperados epidérmicamente para detección electroquímica, seguido de enrutamiento para leer la electrónica a través de una vía aislada de deformación. Integraron el FESS dentro de un reloj inteligente personalizado para la inducción del sudor, muestreo, detección electroquímica, procesamiento de señales y visualización o transmisión de datos. Los resultados mostraron una transducción de señales de alta fidelidad y un contacto mecánico robusto con la piel humana sin restringir el movimiento del usuario. El sistema de detección independiente se puede vincular con los dispositivos electrónicos portátiles del futuro para generar conjuntos de datos de alta fidelidad relacionados con la salud y el bienestar basados en las actividades diarias de los usuarios.
Para crear una vía biológica eficiente, Zhao y col. integrina seleccionada:una molécula adhesiva celular que permitió eficazmente el intercambio de información fisiológica entre matrices intracelulares y extracelulares. El dispositivo FESS implementó funcionalidades similares a las de la integrina a través de una región aislada de cepa en una estructura de microfluidos. Diseñaron FESS como conductor vertical, Adhesivo de doble cara y sistema de película fina bioanalítica microfluídica flexible compuesto por múltiples películas apiladas verticalmente. Estas películas incluían una película conductora anisotrópica adhesiva (ACF), una película de matriz de electrodos de metal noble, una película bioquímica, una película de microfluidos y una película adhesiva para la piel. Pegaron el sistema completo de película delgada en la electrónica de lectura sin conectores y con una mínima resistencia de contacto para transformar potencialmente cualquier contacto eléctrico en un sensor químico o biológico. El equipo desarrolló una prueba de principio, reloj inteligente autónomo con detección de biomarcadores con FESS para monitorear los perfiles de metabolitos del sudor de individuos en entornos sedentarios frente a entornos de mucho ejercicio.

Simulación de deformación FESS y caracterización de interconexión de señales de deformación aislada. (A) Ilustración de la interconexión de señales fuera del plano del FESS frente a la interconexión de señales en el plano convencional. Las implementaciones convencionales están limitadas al enrutamiento de señales a través de regiones muy tensas, mientras que el FESS diseñado permite el enrutamiento a través de regiones de deformación casi nula. (B) Perfil de deformación (ε) simulado por COMSOL de un FESS representativo en presencia de una fuerza de corte aplicada externamente, ilustrando una deformación cercana a cero en la parte inferior del microcanal (es decir, interfaz sustrato-biofluido). (C) Vista ampliada correspondiente del perfil de deformación para un "píxel". (D) Distribución de la deformación a lo largo de la línea discontinua en (C). (E) Caracterización eléctrica de interconexión fuera del plano de FESS realizada bajo diferentes ángulos de flexión localizados (para una matriz de 6 × 6 electrodos de Au). (F) Resistencias de interconexión del FESS-FPCB doblado (RFESS + RFPCB), para diferentes ángulos de flexión localizados (normalizados con respecto a RFPCB sin flexión, RFPCB, 0). Las barras de error indican el error estándar de las mediciones en los seis electrodos dentro de cada columna. (G) Medidas de resistencia de los electrodos FESS bajo diferentes ángulos de flexión (n =36), en relación con la resistencia de la placa de contacto FPCB (RFPCB, 0). (H a J) Ensayos de pelado de 180 ° que caracterizan la adhesión de la interconexión entre el PCB y el FESS con diferentes estructuras de soporte:base microfluídica – ACF (H), canal de microfluidos – ACF (I), y una matriz representativa de canales de microfluidos:ACF (J). (Crédito de la foto:Peterson Nguyen, Universidad de California, Los Ángeles.) Crédito: Avances de la ciencia , doi:10.1126 / sciadv.aaz0007
En esta configuración, La conductividad vertical de ACF facilitó las interconexiones de señales fuera del plano para evitar efectos de tensión inducidos por movimientos corporales no deseados en las rutas de las señales. El equipo caracterizó la propiedad de adhesión mecánica de FESS para garantizar que las fuerzas de adhesión entre el FESS y la electrónica fueran más altas que las de FESS y la piel seca o con sudoración activa. El equipo probó la fuerza requerida para despegar la capa de ACF del FESS en una placa de circuito impreso y los resultados mostraron una fuerte interconexión basada en FESS con la electrónica. adecuado para aplicaciones corporales.
Zhao y col. luego probó la capacidad de transducción de señales del FESS. Modelaron electrodos de metales nobles en el ACF para lograr la transducción de señales bioquímicas a eléctricas, seguido de la deposición de películas bioquímicas para analizar dianas biomoleculares de interés. Probaron la actividad electroquímica del ACF con patrón metálico para dos superficies de electrodos de uso común en Au modificado con nanopartículas de oro (Au) y platino (Pt) sin modificar. Los métodos electroanalíticos investigados en el trabajo proporcionaron lecturas de biomarcadores de muestra a respuesta para obtener información en tiempo real sobre las alteraciones en la biocomposición del sudor.

Prueba de la medición de resistencia de las interconexiones basadas en ACF después de una deformación mecánica. Crédito:Science Advances, doi:10.1126 / sciadv.aaz0007
En los siguientes experimentos, el equipo de investigación demostró la capacidad de FESS para monitorear biomarcadores durante las actividades diarias del usuario. Para lograr esto, integraron FESS en un reloj inteligente desarrollado a medida como un modelo de dispositivo IOT que contiene un circuito analógico / digital, Transceptor Bluetooth y una pantalla de cristal líquido (LCD) para funcionalidades a nivel del sistema, incluido el procesamiento de señales y comandos de usuario, pantalla y comunicación de datos inalámbrica. El reloj inteligente basado en FESS funcionó de manera similar a un potenciostato. Los científicos adhirieron el reloj inteligente completo a la piel sin envoltorios externos o accesorios para la detección de biomarcadores inalámbricos como una unidad autónoma. La pantalla LCD mostró lecturas en tiempo real y el perfil temporal de las mediciones de biomarcadores, mientras que el receptor Bluetooth transmitió las lecturas a una aplicación móvil desarrollada a medida para cargar los datos en un servidor en la nube para su posterior análisis.
El equipo adhirió el reloj inteligente basado en FESS en el antebrazo de un sujeto para mostrar su función como un sistema portátil para monitorear biomarcadores. El sujeto podría controlar de forma inalámbrica el dispositivo para tomar en tiempo real, mediciones de biomarcadores basados en el sudor en relación con la rutina diaria del usuario. El usuario monitoreó sus niveles de glucosa en el sudor antes o después de consumir una variedad de comidas y la lectura del reloj inteligente indicó niveles elevados de glucosa en el sudor después de la ingesta de alimentos. en consonancia con las tendencias anteriores. El reloj inteligente también proporcionó información al usuario sobre las lecturas de lactato en el sudor mientras corría en un campo, los resultados fueron consistentes a pesar de la participación de movimientos corporales basados en alta frecuencia y alta aceleración.
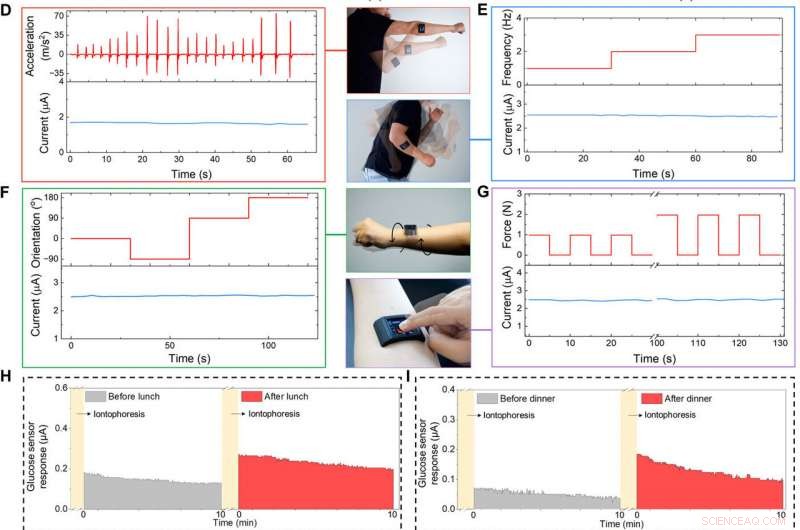
Reloj inteligente con FESS integrado y desarrollado a medida para aplicación en el cuerpo. (A) Ilustración del reloj inteligente habilitado para FESS (que contiene FESS, Pantalla LCD, TARJETA DE CIRCUITO IMPRESO, y unidades de batería alojadas dentro de una carcasa impresa en 3D). (B y C) Caracterización ex situ de la respuesta del sistema sensor de glucosa FESS-PCB ante vibración vortical (electrodo FESS:6 mm2, altura del canal de microfluidos:170 μm, y volumen:4 µl). Los perfiles de aceleración vibratoria se presentan en la mitad superior, y las respuestas del sensor se capturan en la mitad inferior cuando se prueban en PBS (B) y glucosa 100 µM en PBS (C). (D a G) Caracterización de la fidelidad de la señal en el cuerpo de un sistema de detección de lactato FESS-PCB con un sujeto que realiza boxeo de sombra (D), balanceo del brazo (E), torsión de muñeca (F), y dispositivo presionando (G). La aceleración frecuencia, orientación, y los perfiles de fuerza se presentan en la mitad superior, y las respuestas de los sensores se capturan en la mitad inferior. (H a J) Monitoreo de los perfiles de metabolitos de los sujetos a través de varios eventos diarios y en diferentes entornos. La glucosa en el sudor inducida iontoforéticamente se midió antes y después del almuerzo (H) y la cena (I). (J) Mediciones de lactato en el sudor durante el ejercicio (a la derecha se muestra un perfil representativo de aceleración inducida por el movimiento). (Crédito de la foto:Peterson Nguyen, Kaili Chiu, y Yichao Zhao, Universidad de California, Los Ángeles.) Crédito: Avances de la ciencia , doi:10.1126 / sciadv.aaz0007
De este modo, Yichao Zhao y sus colegas examinaron la ruta de entrega de información de biomarcadores y reconocieron regiones de tensión casi cero dentro de un módulo de detección de microfluidos para diseñar una ruta de cepa aislada para preservar la fidelidad de los datos de biomarcadores. El sistema de película delgada que formó la entidad FESS independiente fue bioinspirado por funcionalidades similares a las integrinas para la transducción de señales y la interconexión de señales a través de la adhesión de doble cara. El FESS unió de manera eficiente la piel y la electrónica de lectura para recolectar información de biomarcadores. El equipo combinó el sistema FESS a la perfección con un reloj inteligente desarrollado a medida como un biosensor portátil para monitorear las lecturas de biomarcadores en tiempo real a lo largo de la rutina diaria del usuario. Para comercializar el prototipo desarrollado en este trabajo, Zhao y col. proponer ensayos clínicos futuros para mapear lecturas de biomarcadores basados en el sudor y obtener información sobre el estado fisiológico de los usuarios. Las ventajas de este trabajo, incluida su facilidad de integración con dispositivos electrónicos portátiles y lecturas de alta fidelidad, se pueden emplear para realizar investigaciones clínicas a gran escala.
© 2020 Science X Network