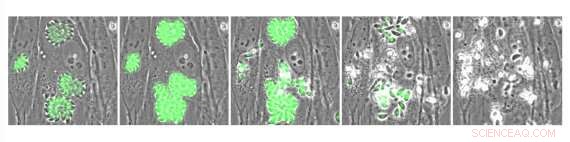
Parásitos intracelulares de Toxoplasma que expresan el indicador de calcio codificado genéticamente GCaMP. Los parásitos se trataron con A23187, un compuesto que provoca la entrada de calcio y estimula la salida del parásito. Crédito:Instituto Whitehead de Investigación Biomédica
Los parásitos Apicomplexan infectan a cientos de millones de personas en todo el mundo cada año. Varias especies de parásitos apicomplexanos del género Plasmodium causan malaria, mientras que otra especie apicomplexana, Toxoplasma gondii (T. gondii), causa toxoplasmosis, una enfermedad con síntomas similares a los de la gripe que puede ser letal para las personas con sistemas inmunitarios debilitados. A pesar de su impacto, la biología de estos parásitos causantes de enfermedades no se comprende muy bien y las opciones de tratamiento para la infección son limitadas.
Un enfoque potencial para tratar la infección podrían ser los medicamentos que interrumpen la señalización del calcio de los parásitos. de los que dependen para propagarse de una célula a otra en sus anfitriones. Los parásitos necesitan una entrada de calcio para salir de una célula huésped infectada, un proceso llamado salida, y moverse a través del cuerpo del huésped e invadir otras células. En trabajos anteriores, un investigador del laboratorio del miembro del Instituto Whitehead, Sebastian Lourido, Saima Sidik, había probado una gran colección de moléculas e identificado una llamada potenciador 1 (ENH1), que perturbó los niveles de calcio de los parásitos e impidió la salida, como un prometedor plomo antiparasitario. Sin embargo, los experimentos originales no determinaron cómo actúa ENH1. En investigación publicada en la revista Biología química ACS el 29 de junio Alice Herneisen, un estudiante de posgrado en el laboratorio de Lourido, y Lourido, quien también es profesor asistente de biología en el Instituto de Tecnología de Massachusetts, utilizó un enfoque llamado perfil de proteoma térmico para descubrir cómo ENH1 previene la salida de los parásitos T. gondii. Identificaron el objetivo principal de ENH1 como una molécula dependiente de calcio llamada CDPK1 que los parásitos usan para prepararse para la salida. moviéndose entre celdas, e invasión de células huésped. ENH1 se une a CDPK1 y evita que funcione.
"Los avances de las últimas décadas han facilitado mucho el descubrimiento de la actividad potencialmente terapéutica de una molécula, pero el siguiente paso para descubrir cómo funciona la molécula a menudo sigue siendo un desafío, "Dice Lourido." Al aplicar nuevos enfoques expansivos, estamos empezando a construir una imagen más holística de la biología celular de los parásitos ".
Es importante comprender la biología responsable de los posibles efectos observados de un medicamento porque la mayoría de los medicamentos requieren modificaciones antes de que estén listos para el uso humano; es posible que deban hacerse menos tóxicos. más potente, o más susceptible al medio ambiente del cuerpo humano, y este tipo de modificaciones no se pueden realizar hasta que se comprendan la molécula y su actividad.
Herneisen decidió utilizar un enfoque relativamente nuevo en parásitos, perfilado térmico del proteoma, para descubrir los objetivos de ENH1:las moléculas a las que se une, conduciendo a sus efectos terapéuticos. El enfoque funciona graficando cómo cada una de las proteínas dentro del parásito reacciona a los cambios de calor con y sin exposición a ENH1. Una ventaja de este enfoque es que es imparcial, lo que significa que en lugar de que los investigadores elijan objetivos probables por adelantado para probar, investigan tantas moléculas como sea posible, lo que puede dar lugar a hallazgos inesperados. Por ejemplo, Lourido ha estado investigando CDPK1 en otros contextos durante muchos años, y basándose en la comprensión previa de su laboratorio de su función, no habría esperado que fuera un objetivo principal de ENH1; tales sorpresas pueden dirigir la investigación en nuevas y emocionantes direcciones.
Aunque CDPK1 es el principal objetivo de ENH1, las investigaciones no descubrieron el objetivo que permite que ENH1 cause oscilaciones en los niveles de calcio de los parásitos. Encontrar este objetivo perdido es uno de los próximos objetivos del laboratorio.
"El hecho de que ENH1 afecte a múltiples aspectos de la señalización del calcio puede ser lo que lo convierte en un agente antiparasitario tan eficaz, ", Dice Herneisen." Está jugando con los parásitos en varios niveles ".
La traducción de la investigación para pruebas clínicas está muy lejos, pero hay múltiples indicadores de que esta es una dirección prometedora para la investigación. La señalización del calcio no solo es clave para el ciclo de vida de los parásitos y la capacidad de propagarse dentro de un huésped, pero las moléculas y los mecanismos que utilizan los parásitos para modular los niveles de calcio son muy diferentes a los que se encuentran en los mamíferos. Esto significa que es poco probable que un fármaco que interrumpa la señalización del calcio de los parásitos interfiera con la señalización del calcio en pacientes humanos. por lo que podría ser mortal para los parásitos sin dañar las células de los pacientes.