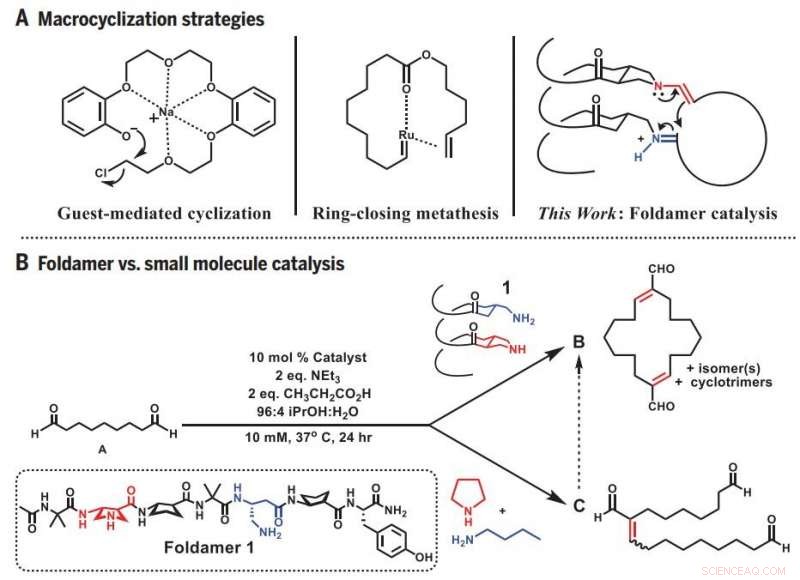
Estrategias de macrociclización. (A) Enfoques anteriores y enfoque plegable de la macrociclización. (B) Reactividad divergente:Foldamer versus catálisis de moléculas pequeñas. eq., equivalente (s). Crédito: Ciencias (2019) DOI:10.1126 / science.aax7344
Inspirándose en la naturaleza, Los químicos de la Universidad de Wisconsin-Madison han descubierto una forma eficiente de luchar durante mucho tiempo, Serpentean moléculas para formar grandes anillos, anillos que forman la columna vertebral de muchos productos farmacéuticos pero que son difíciles de producir en el laboratorio.
El trabajo puede representar un progreso preliminar hacia el desciframiento de cómo las enzimas, perfeccionado por la evolución, producir compuestos naturales de manera tan eficiente. Más inmediatamente, el nuevo método podría ayudar a los investigadores a sintetizar fármacos que tienen grandes cadenas principales de anillos, como los de la hepatitis. La investigación aparece en la edición del 19 de diciembre de la revista Ciencias .
La naturaleza prefiere el desorden de un largo, molécula flexible del orden de un anillo rígido, lo que hace que sea notoriamente difícil para los químicos lograr que se formen anillos grandes en el laboratorio. "Si las moléculas lineales se alargan lo suficiente, es como si los extremos ya no supieran que están conectados, y es tan probable que se unan con otras moléculas como que se unan, "dice el profesor de química de la UW-Madison Sam Gellman, el autor principal del informe.
Sin embargo, las enzimas biológicas pueden unir fácilmente estos extremos y formar anillos de todos los tamaños. Logran esta hazaña gracias a su complejo, Formas tridimensionales que actúan como una cerradura especializada:la molécula lineal encaja en su lugar como una llave de la manera correcta para que se produzca una reacción organizada.
Tanto para estudiar cómo funcionan las enzimas como para imitar sus habilidades, El equipo de Gellman se volvió mucho más pequeño, moléculas tridimensionales similares a proteínas llamadas foldameros que su laboratorio ha ayudado a desarrollar.
Debido a que el foldador tiene una forma tridimensional que puede agarrarse a los extremos de la molécula precursora flexible, aumenta enormemente las probabilidades de que los extremos se encuentren entre sí. Al mismo tiempo, el foldamero cataliza la reacción correcta que une los extremos en un anillo cerrado. El resultado es una síntesis sencilla y predecible de un desafío, y útil, forma molecular.
"Como químicos, Vemos cuán extraordinariamente efectivas son las enzimas para realizar reacciones que son difíciles de lograr en un matraz, pero no entendemos realmente cómo funcionan, ", dice Gellman." Si aprendemos cómo funcionan estos pequeños catalizadores de foldadores, es posible que podamos construir catalizadores que sean efectivos para muchas reacciones diferentes. Por último, tal vez podamos iniciar nuestro camino hacia los foldameros que tienen una actividad verdaderamente similar a la de las enzimas ".
El estudiante de posgrado y autor principal, Zebediah Girvin, comenzó la investigación probando las habilidades de un plegadora en forma de espiral. Girvin intentó usar el foldamero para doblar una molécula lineal que contenía nueve átomos de carbono para que formara un anillo. Pero en lugar de un anillo del tamaño esperado, Girvin obtuvo uno dos veces más grande:el resultado de dos moléculas precursoras que primero se unen y luego cierran el círculo.
"Esta es una situación común en la ciencia. Intentas algo y no sale como esperabas, ", dice Gellman." El desafío es reconocer cuándo el resultado sorprendente es tan interesante como el objetivo original, o incluso más interesante ".
Guiado por esta serendipia, Girvin comenzó a probar qué tan bien el plegador podía producir los anillos más grandes que parecía preferir crear. Descubrió que podía fabricar fácilmente anillos formados por 12 a 22 átomos de carbono cuando los sitios reactivos del foldador, donde ocurre el cierre del anillo, estaban alineados uno con el otro en un lado. Esta orientación acercó los dos extremos de diversas moléculas lineales lo suficiente como para fusionarse.
Como prueba de concepto para la nueva técnica, Girvin sintetizó el producto natural robustol desde cero. Derivado de las hojas del sedoso roble australiano, El robustol pesa con un fuerte anillo de 22 átomos.
El equipo de Gellman está muy entusiasmado con el potencial de los foldameros para catalizar otras reacciones útiles y posiblemente ayudar a desentrañar misterios de larga data sobre cómo las enzimas, virtuosos químicos de la naturaleza, Produce las moléculas necesarias para la vida simplemente colocando los bloques de construcción de aminoácidos en la forma correcta. Mientras que esas respuestas están a años de distancia, la técnica de cierre de anillo que han descubierto podría tener un uso más inmediato sintetizando candidatos a fármacos. El vaniprevir, fármaco contra la hepatitis C, que se utiliza en Japón y en ensayos de última etapa en los EE. UU., contiene solo este tipo de anillo grande.
El verdadero potencial de los foldamers se deriva de su diversidad. Los químicos pueden producir una variedad casi infinita de foldamers en el laboratorio porque tienen acceso a más componentes básicos que los que se encuentran en las proteínas naturales. Esto podría permitir a los químicos construir catalizadores más útiles, lo que llevó a Gellman a patentar ciertos foldadores y fundar la empresa Longevity Biotech para explorar sus usos terapéuticos.
Avanzando, esa gran cantidad de opciones permitirá a los investigadores organizar estos catalizadores en formas que probablemente sean útiles de formas inesperadas. Solo más investigación lo dirá.
"Aún no sabemos realmente de lo que son capaces estos catalizadores, ", dice Girvin." Se necesitarán años para descubrir su potencial, y es importante que proyectemos una red amplia y mantengamos la mente abierta sobre lo que podemos lograr con estas nuevas herramientas ".