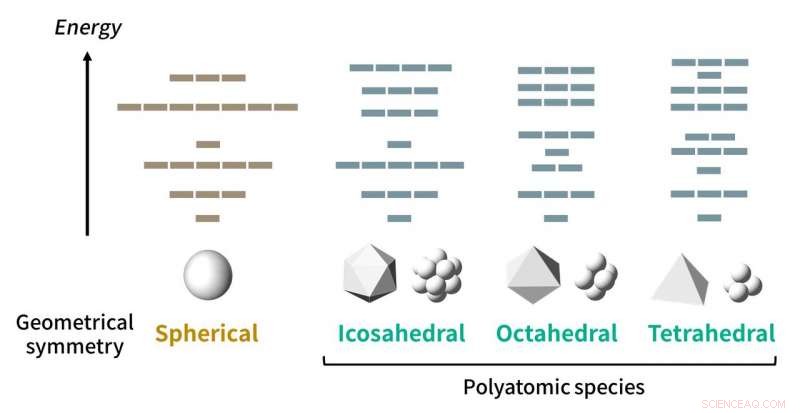
El modelo propuesto tiene en cuenta los patrones orbitales que obedecen a ciertas reglas para muchos tipos de simetrías. Aunque una esfera tiene la simetría geométrica más alta, no hay ninguna especie poliatómica real con simetría esférica. Crédito:Tecnología de Tokio
La tabla periódica de elementos fue propuesta en 1869, y a partir de entonces se convirtió en una de las piedras angulares de las ciencias naturales. Esta tabla fue diseñada para contener todos los elementos que se encuentran en la naturaleza en un diseño especial que los agrupa en filas y columnas según una de sus características más importantes, el número de electrones. Los científicos han utilizado la tabla periódica durante décadas para predecir las características de los elementos entonces desconocidos, que se agregaron a la tabla con el tiempo.
¿Podría existir una tabla periódica para las moléculas? Aunque algunos investigadores han pensado en esta posibilidad y han propuesto reglas periódicas para predecir la existencia de determinadas moléculas, estas predicciones eran válidas solo para grupos de átomos con una simetría cuasi esférica, debido a las limitaciones de su propia teoría. Sin embargo, hay muchos grupos de átomos con otras formas y otros tipos de simetrías que deberían tenerse en cuenta con un modelo mejor. Por lo tanto, un equipo de investigación de Tokyo Tech, incluido el Dr. Takamasa Tsukamoto, Dr. Naoki Haruta, Prof. Kimihisa Yamamoto y colegas, propuso un nuevo enfoque para construir una tabla periódica de moléculas con múltiples tipos de simetrías.
Su enfoque se basa en una aguda observación del comportamiento de los electrones de valencia de los átomos que forman grupos moleculares. Los electrones de valencia se pueden considerar como electrones "libres" en átomos con un orbital más externo, y así pueden interactuar con los electrones de otros átomos para formar compuestos. Cuando varios átomos forman un grupo con una forma simétrica, sus electrones de valencia tienden a ocupar orbitales moleculares específicos llamados "orbitales superatómicos, "en el que se comportan casi exactamente como si fueran los electrones de un átomo enorme.
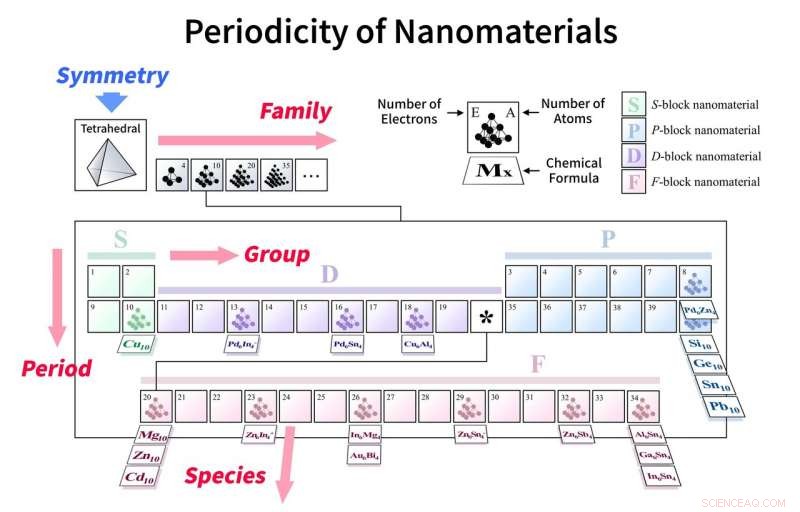
En el marco propuesto, habría conjuntos de tablas para cada tipo de simetría organizados según cuatro parámetros:grupos y períodos (número de electrones), familias (número de átomos constituyentes), y especie (tipo de elementos constitutivos). Crédito:Tecnología de Tokio
Al considerar este hecho y analizar los efectos de las simetrías estructurales para los conglomerados (Fig.1), los investigadores propusieron "modelos orbitales adaptados a la simetría (SAO), "que están de acuerdo con múltiples moléculas conocidas, así como con cálculos de mecánica cuántica de última generación. Las nuevas tablas periódicas, que se crearía para cada tipo de simetría, en realidad sería de cuatro dimensiones, como se muestra en la Fig.2, porque las moléculas se organizarían de acuerdo con cuatro parámetros:grupos y períodos (según sus electrones de "valencia", similar a la tabla periódica normal), especies (basadas en los elementos constitutivos), y familias (basadas en el número de átomos).
El enfoque SAO es muy prometedor en el campo del diseño de materiales. "Las técnicas de síntesis modernas nos permiten producir muchos materiales innovadores basados en el modelo SAO, como materiales magnéticos ligeros, ", afirma el profesor Yamamoto. El camino a seguir para los científicos consiste en ampliar aún más estas tablas a grupos moleculares con otras formas y simetrías y predecir moléculas estables que aún no se han desarrollado". Entre las infinitas combinaciones de elementos constitutivos, la tabla periódica propuesta será una contribución significativa al descubrimiento de nuevos materiales funcionales, "concluye el Prof. Yamamoto.