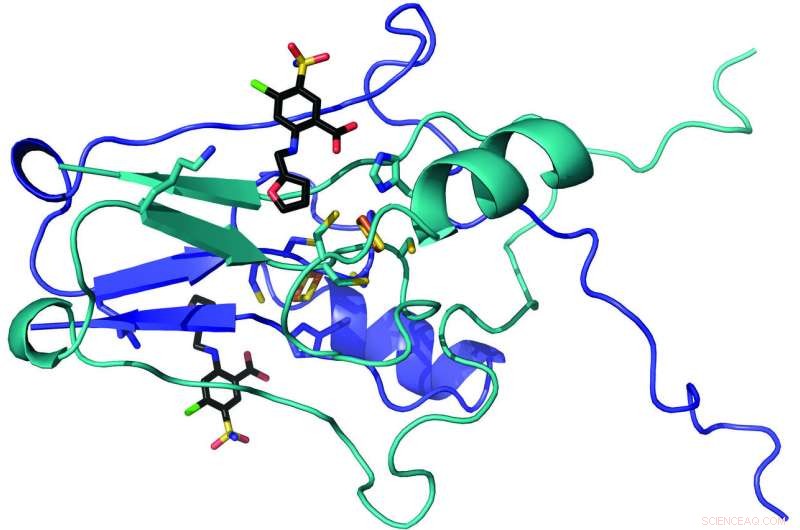
Un equipo de investigadores de WVU, incluido Werner Geldenhuys, John Hollander y Aaron Robart — han cartografiado la estructura cristalina de una proteína llamada "mitoNEET" y han identificado cómo un fármaco se adhiere a ella. Debido a que investigaciones anteriores han implicado a mitoNEET en la diabetes, accidente cerebrovascular y enfermedad cardíaca, Los hallazgos de los investigadores pueden informar el desarrollo de nuevos tratamientos para esas condiciones difíciles de abordar. Crédito:Universidad de Virginia Occidental
Los medicamentos se adhieren a las proteínas de nuestro cuerpo de la misma manera que las naves espaciales se acoplan a la Estación Espacial Internacional. Describir ese proceso en detalle puede revelar mucho sobre cómo funcionan los medicamentos y qué forma deben tomar los nuevos medicamentos.
Investigadores de la Universidad de West Virginia han trazado un mapa de la estructura cristalina de una proteína que reside en nuestras células y han determinado, por primera vez, cómo se adhiere un fármaco a ella. Los hallazgos aparecen en Química de las comunicaciones , una revista de investigación sobre la naturaleza.
El estudio, financiado por el Instituto de Ciencias Clínicas y Traslacionales de West Virginia, se centró en una proteína llamada "mitoNEET". MitoNEET habita la membrana externa de nuestras mitocondrias, que actúan como plantas de energía que energizan nuestras células.
"MitoNEET es un nuevo objetivo terapéutico para las enfermedades de base metabólica y posiblemente podría conducir a tratamientos modificadores de la enfermedad de Alzheimer y accidente cerebrovascular, "dijo Werner Geldenhuys, profesor asociado de la Facultad de Farmacia y Facultad de Medicina. Él y sus colegas, incluido Aaron Robart, profesor asistente en la Facultad de Medicina de WVU, John Hollander, decano asistente de programas profesionales en la Facultad de Medicina de WVU, y Timothy Long, un profesor asociado de la Facultad de Farmacia de la Universidad Marshall — llevó a cabo el proyecto.
"Esta proteína se ha relacionado con muchas enfermedades que son muy difíciles de abordar:cosas como la diabetes, carrera, enfermedad del corazón, ", Dijo Robart." En realidad, todavía no sabemos qué hace la proteína, pero cuelga cerca de la central eléctrica de la celda, y todas estas enfermedades tienen un tema de flujo de energía ".
Para explorar el papel que juega mitoNEET en nuestros procesos energéticos, los investigadores aislaron mitoNEET tanto de la sobreexpresión bacteriana como de modelos animales. Luego, sintetizaron 11 moléculas similares a la furosemida, un diurético común que se vende bajo la marca LASIX, y les expusieron el mitoNEET.
Después de que las moléculas se unieron al mitoNEET, los investigadores construyeron mapas átomo por átomo de los emparejamientos. Controlaron de forma remota la fuente de fotones avanzada del Laboratorio Nacional Argonne, que bombardea las muestras con Rayos X de alta energía:para revelar con precisión cómo se unieron las moléculas.
El equipo descubrió que las moléculas se acoplaban a un grupo de átomos de hierro y azufre que formaban parte de la proteína. Raisa Nuñez, un estudiante que participa en el Programa de Aprendizaje de Investigación, recopilado datos estructurales preliminares. "Esto pone de relieve que los descubrimientos científicos importantes pueden producirse en cualquier nivel profesional, "Dijo Robart.
"Estos hallazgos son importantes, ya que nos permiten seguir comprendiendo el papel que desempeñan las mitocondrias y la bioenergética en muchos estados patológicos". "Dijo Hollander." La modulación de la función mitocondrial a través de terapias dirigidas puede ser una vía crítica para el descubrimiento de fármacos ".
Comprender la función celular de mitoNEET podría mejorar el rendimiento de los fármacos que actúan alterando la actividad de la proteína. Por ejemplo, agregar un grupo de oxígeno adicional a la estructura molecular de un fármaco podría reforzar drásticamente su vínculo con mitoNEET y eliminar la unión no intencional a otras proteínas celulares.
¿Cuál es el resultado potencial para los pacientes que toman el medicamento? Mejor alivio de los síntomas.
"El éxito de este proyecto realmente ilustra cómo los enfoques que se consideran ciencia básica pueden proporcionar una visión considerable de los problemas clínicos, "dijo Michael Schaller, quien preside el Departamento de Bioquímica de la Facultad de Medicina. "También demuestra el poder de abordar los problemas como equipos formados por miembros con experiencia muy diferente".