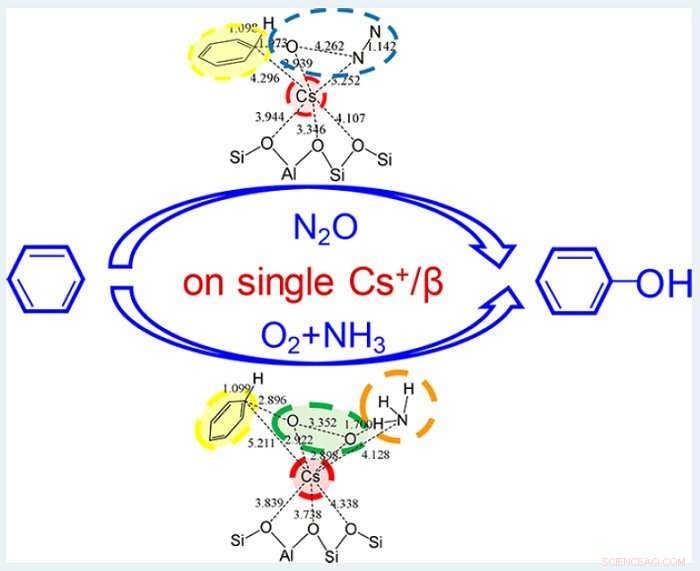
Resumen gráfico del artículo. Crédito: Catálisis ACS
Investigadores de la Universidad de Electrocomunicación, El informe de Tokio sobre una plataforma catalítica de un solo sitio con alta selectividad para la síntesis de fenol en un solo paso en un artículo apareció en Catálisis ACS .
El proceso de cumeno es un proceso industrial de tres pasos que consume mucha energía (uno de los pasos es explosivo) que se utiliza para producir fenol (C 6 H 5 OH), un producto químico utilizado como precursor de muchos materiales de importancia industrial, incluyendo polímeros, medicamentos y herbicidas. Sería muy deseable encontrar una forma eficiente y menos dañina para el medio ambiente de producir fenol, y la mejor opción sería sintetizarlo directamente a partir de benceno, O 2 y N 2 O en un proceso catalítico de un solo paso. Idealmente, esto sería una reacción de flujo en fase gaseosa en un catalizador sólido, lo que haría que la reacción fuera eficiente y daría como resultado una reducción del consumo de recursos y productos fáciles de separar.
Yasuhiro Iwasawa y colegas de la Universidad de Electrocomunicación, Tokio informaron de la oxidación selectiva de benceno a fenol utilizando grandes metales alcalinos como sitios activos incorporados en los poros de la zeolita. Los resultados desafían la sabiduría convencional sobre los procesos catalíticos, por lo que los iones de metales alcalinos y alcalinos no pueden activar el benceno, O 2 y N 2 O cuando absorben por separado. Las reacciones, que se caracterizaron mediante una combinación de técnicas de sincrotrón, mostrar una conversión y una selectividad muy altas, en particular para los iones Rb y Cs adsorbidos en un tipo de zeolita llamada β-zeolita.
Se estudiaron dos caminos de reacción:en el primero, el benceno reacciona con N 2 Oh en el segundo, con O 2 en presencia de NH 3 . Se utilizaron cálculos de la teoría funcional de la densidad para comprender el mecanismo subyacente a ambas reacciones catalíticas. En el primer caso, la reacción comienza con la adsorción de benceno y N 2 O; en el siguiente paso, el enlace O-N en N 2 O disocia, se forma un enlace O-C en el benceno y el átomo de H unido al átomo de C se mueve hacia el O, de modo que se forma fenol y el N2 se desorbe. En la segunda reacción, que tiene un rendimiento menos llamativo que el primero, benceno, O 2 y NH 3 co-adsorber; la disociación de O 2 es activado por NH 3 y, como en el caso anterior, se forma un enlace O-C en benceno, y el átomo de H en el átomo de C migra al átomo de O, formando fenol. Debido a que la reacción ocurre en un solo sitio iónico, se necesita una gran plataforma de reacción, lo que explica por qué Cs y Rb, que ambos tienen grandes diámetros, funcionan mejor que otros iones de metales alcalinos y alcalinos. La regulación de su estructura de confinamiento y coordinación local por la estructura de poros de la β-zeolita también juega un papel importante.
Los autores optimizaron las condiciones de reacción y fabricación del catalizador, modificar los precursores de metales, fuentes de zeolitas y temperatura de reacción para tratar de lograr un rendimiento lo suficientemente bueno como para hacer que el proceso sea atractivo para aplicaciones industriales.
En tono rimbombante, las barreras de activación son lo suficientemente pequeñas como para que las reacciones puedan desarrollarse a baja temperatura. Como concluyen los autores, "Los presentes hallazgos presentan un nuevo enfoque para diseñar una catálisis de activación selectiva de C-H eficiente en condiciones suaves".