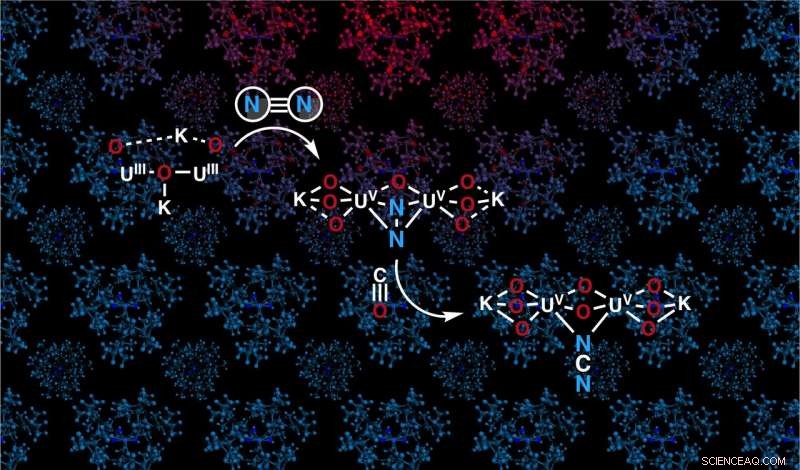
El compuesto de uranio con puentes oxo captura el dinitrógeno y convierte el dinitrógeno y el monóxido de carbono en cianamida. Crédito:Marta Falcone / Marinella Mazzanti / EPFL
Abundante en la atmósfera, el nitrógeno rara vez se utiliza en la producción industrial de productos químicos. El proceso más importante que utiliza nitrógeno es la síntesis de amoniaco utilizado para la preparación de fertilizantes agrícolas.
El uso de nitrógeno como materia prima ("materia prima") para uso industrial se logra mediante una reacción conocida como fijación de nitrógeno. En esta reacción, nitrógeno molecular (o dinitrógeno — N 2 ) se divide en dos átomos de nitrógeno que se pueden conectar a otros elementos como hidrógeno o carbono, permitiendo que el nitrógeno se almacene como amoníaco o se convierta directamente en compuestos de mayor valor.
Pero el amoníaco no es fácil de producir a nivel industrial; el proceso principal, llamado Haber-Bosch, utiliza un catalizador a base de hierro a temperaturas de alrededor de 450 grados C y presiones de 300 bar, casi 300 veces la presión al nivel del mar. Para que el proceso sea más rentable, Los químicos se han centrado en el desarrollo de nuevos sistemas que pueden transformar el nitrógeno en compuestos útiles utilizando condiciones suaves de baja energía.
En 2017, el laboratorio de Marinella Mazzanti en EPFL pudo convertir nitrógeno molecular en amoníaco en condiciones ambientales sintetizando un compuesto que contiene dos iones de uranio (III) y tres centros de potasio unidos por un grupo nitruro.
Ahora, el grupo, en colaboración con otros grupos EPFL, ha demostrado que al reemplazar el puente de nitruro en el sistema de uranio por un puente oxo, aún pueden unirse al dinitrógeno. Además, el dinitrógeno unido se puede escindir fácilmente en condiciones ambientales por el monóxido de carbono para producir cianamida, un compuesto que se usa ampliamente en la agricultura, productos farmacéuticos, y varios compuestos orgánicos.
La reactividad del complejo de dinitrógeno con puentes oxo fue notablemente diferente en comparación con el complejo de nitruro anterior y los pocos otros complejos de nitrógeno conocidos en el campo. Los estudios computacionales permitieron a los científicos relacionar estas diferencias en reactividad con la unión en el puente uranio-oxo / -nitruro.
"Estos hallazgos proporcionan información importante sobre la relación entre la estructura y la reactividad que debería extenderse a los materiales de nitruro y óxido, "dice Marinella Mazzanti." Además, la implementación de estos compuestos en sistemas catalíticos podría conducir en última instancia a un acceso de menor costo a los fertilizantes ".