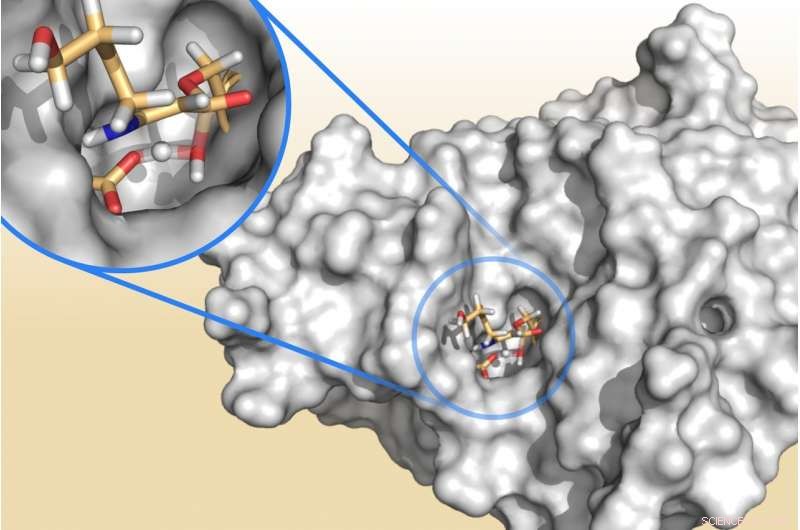
Una enzima bacteriana que libera fragmentos de ácido clavulánico, un "bloqueador de resistencia" diseñado para superar las infecciones resistentes a los antibióticos. La destrucción del ácido clavulánico permite que la enzima proteja a las bacterias de los efectos de los antibióticos. Crédito:Marc van der Kamp
A través de simulaciones por computadora, Los científicos pueden predecir si las bacterias pueden detenerse con terapias antibacterianas populares o no, un avance que ayudará a seleccionar y desarrollar tratamientos efectivos para las infecciones bacterianas.
La creciente resistencia a los antibióticos es una de las amenazas para la salud mundial más graves a las que nos enfrentamos. Existe una necesidad urgente de desarrollar nuevos antibióticos que sean rentables, ya que se estima que para 2050, 10 millones de vidas por año estarán en riesgo de infecciones resistentes a los antibióticos. En un intento por ayudar a abordar este desafío, Investigadores de la Universidad de Bristol han desarrollado simulaciones por computadora que podrían ser clave para avanzar en la actual "carrera armamentista" con las bacterias.
Los investigadores se centraron en las enzimas de las bacterias que pueden dividir la estructura de los antibióticos de tipo penicilina. conduciendo a la resistencia. Para restaurar la eficacia de estos antibióticos, Se han desarrollado moléculas de "bloqueo de resistencia" para bloquear la actividad de estas enzimas. Al tratar a los pacientes con las combinaciones adecuadas de antibióticos y bloqueadores de resistencia, los médicos pueden tomar la delantera en la batalla. Desafortunadamente, las bacterias pueden producir muchas enzimas diferentes capaces de destruir las penicilinas, y los bloqueadores de resistencia disponibles funcionan solo contra algunos de ellos.
Nuevos hallazgos, publicado en Bioquímica , muestran que ahora es posible usar simulaciones por computadora para predecir si estos bloqueadores de resistencia serán efectivos o no. Se espera que esta información ayude a los científicos a desarrollar bloqueadores de resistencia mejorados, que puede restaurar la acción de los antibióticos populares contra una gama más amplia de bacterias resistentes.
Usando una técnica de simulación por computadora llamada QM / MM (simulaciones de mecánica cuántica / mecánica molecular), el equipo de investigación de Bristol pudo obtener una visión a nivel molecular de cómo reaccionan las enzimas de resistencia con los bloqueadores de resistencia.
Los investigadores se centraron específicamente en el ácido clavulánico, un medicamento que previene la destrucción de antibióticos comunes similares a la penicilina. El ácido clavulánico se usa comúnmente en combinación con el antibiótico amoxicilina para tratar el oído, infecciones de los senos nasales y del tracto urinario (co-amoxiclav). Algunas de esas infecciones bacterianas, sin embargo, se están volviendo mucho más difíciles de tratar porque el ácido clavulánico no actúa eficazmente contra las enzimas que producen.
Las simulaciones QM / MM interrogaron cómo el ácido clavulánico interactúa con estas enzimas bacterianas y revelaron el paso más importante para determinar si la enzima se bloquea de manera efectiva. Una enzima que no se puede detener libera una molécula descompuesta de ácido clavulánico y continúa descomponiendo el antibiótico con el que se administra. resultando en resistencia a los antibióticos. Si la degradación del ácido clavulánico tarda mucho tiempo, luego, la enzima se 'obstruye' y no puede descomponer el antibiótico, que luego puede matar la bacteria y eliminar la infección.
Dr. Marc van der Kamp, de la Escuela de Bioquímica de la Universidad de Bristol, dijo:
"Estamos emocionados de ver cómo nuestras simulaciones por computadora se pueden usar en el futuro para probar enzimas de bacterias y predecir cuándo será efectivo un inhibidor de bloqueo de resistencia.
Esperamos que esto identifique cómo podemos bloquear mejor estas enzimas bacterianas, de modo que los antibióticos se puedan utilizar eficazmente para el tratamiento de infecciones resistentes a los fármacos.
Nuestras simulaciones también pueden ser una herramienta valiosa para ayudar a elegir qué combinaciones de medicamentos son las mejores para tratar un brote de infección en particular. permitiéndonos estar mejor equipados en esta 'carrera armamentista' con bacterias ".