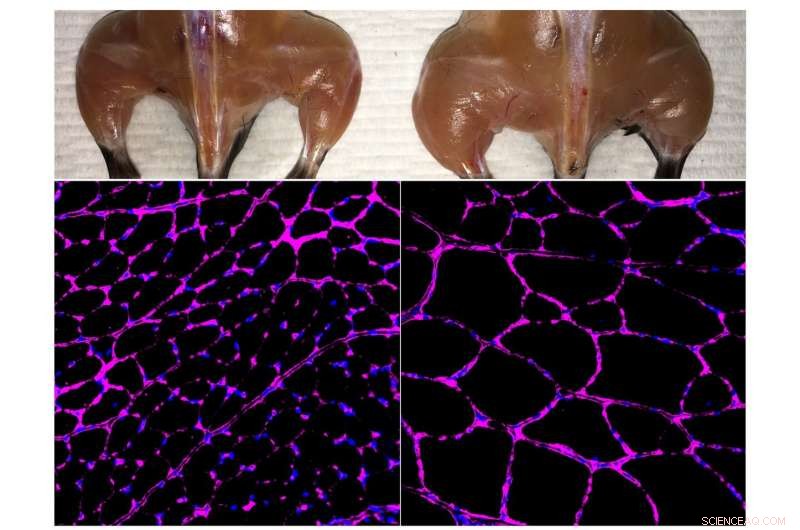
El avanzado sistema de activación de genes epigenéticos basado en Cas9 in vivo del laboratorio de Belmonte mejora la masa del músculo esquelético (arriba) y el crecimiento del tamaño de las fibras (abajo) en un ratón tratado (derecha) en comparación con un control independiente (izquierda). Las imágenes de microscopía fluorescente en la parte inferior muestran tinción púrpura de la glicoproteína laminina en las fibras del músculo tibial anterior. Crédito:Instituto Salk
Los científicos de Salk han creado una nueva versión de la tecnología de edición del genoma CRISPR / Cas9 que les permite activar genes sin crear rupturas en el ADN. potencialmente eludir un obstáculo importante para el uso de tecnologías de edición de genes para tratar enfermedades humanas.
La mayoría de los sistemas CRISPR / Cas9 funcionan creando "rupturas de doble hebra" (DSB) en las regiones del genoma destinadas a la edición o eliminación, pero muchos investigadores se oponen a crear tales rupturas en el ADN de los seres humanos vivos. Como prueba de concepto, el grupo Salk utilizó su nuevo enfoque para tratar varias enfermedades, incluida la diabetes, enfermedad renal aguda, y distrofia muscular, en modelos de ratón.
"Aunque muchos estudios han demostrado que CRISPR / Cas9 se puede aplicar como una herramienta poderosa para la terapia génica, Existe una creciente preocupación con respecto a las mutaciones no deseadas generadas por las roturas de doble hebra a través de esta tecnología, "dice Juan Carlos Izpisua Belmonte, profesor del Laboratorio de Expresión Genética de Salk y autor principal del nuevo artículo, publicado en Celda el 7 de diciembre 2017. "Pudimos sortear esa preocupación".
En el sistema CRISPR / Cas9 original, la enzima Cas9 se acopla con ARN guía que la dirigen al lugar correcto en el genoma para crear DSB. Recientemente, algunos investigadores han comenzado a utilizar una forma "muerta" de Cas9 (dCas9), que aún puede apuntar a lugares específicos del genoma, pero ya no corta el ADN. En lugar de, dCas9 se ha combinado con dominios de activación transcripcional (interruptores moleculares) que activan genes específicos. Pero la proteína resultante, dCas9 unida a los interruptores activadores, es demasiado grande y voluminosa para caber en el vehículo que se usa típicamente para administrar este tipo de terapias a las células de los organismos vivos. a saber, virus adenoasociados (AAV). La falta de un sistema de administración eficiente hace que sea muy difícil utilizar esta herramienta en aplicaciones clínicas.
El equipo de Izpisua Belmonte combinó Cas9 / dCas9 con una gama de conmutadores activadores diferentes para descubrir una combinación que funcionó incluso cuando las proteínas no estaban fusionadas entre sí. En otras palabras, Cas9 o dCas9 se empaquetaron en un AAV, y los interruptores y los ARN guía se empaquetaron en otro. También optimizaron los ARN guía para asegurarse de que todas las piezas terminaran en el lugar deseado del genoma. y que el gen diana estaba fuertemente activado.
"Todos los componentes trabajan juntos en el organismo para influir en los genes endógenos, "dice Hsin-Kai (Ken) Liao, investigador de plantilla en el laboratorio de Izpisua Belmonte y coautor del nuevo artículo. De este modo, la tecnología opera epigenéticamente, lo que significa que influye en la actividad genética sin cambiar la secuencia de ADN.
Para probar el método, los investigadores utilizaron modelos de ratón de lesión renal aguda, diabetes tipo 1 y una forma de distrofia muscular. En cada caso, diseñaron su sistema CRISPR / Cas9 para impulsar la expresión de un gen endógeno que podría potencialmente revertir los síntomas de la enfermedad. En el caso de enfermedad renal, activaron dos genes que se sabe que están involucrados en la función renal, y observó no solo niveles aumentados de las proteínas asociadas con esos genes, pero mejoró la función renal después de una lesión aguda. Para la diabetes tipo 1, tenían como objetivo impulsar la actividad de genes que pudieran generar células productoras de insulina. Una vez más, el tratamiento funcionó, la reducción de los niveles de glucosa en sangre en un modelo de ratón con diabetes. Para la distrofia muscular, los investigadores expresaron genes que previamente se había demostrado que revierten los síntomas de la enfermedad, incluyendo un gen particularmente grande que no se puede administrar fácilmente a través de terapias génicas tradicionales mediadas por virus.
"Estábamos muy emocionados cuando vimos los resultados en ratones, "agrega Fumiyuki Hatanaka, investigador asociado en el laboratorio y coautor del artículo. "Podemos inducir la activación de genes y al mismo tiempo ver cambios fisiológicos".
El equipo de Izpisua Belmonte ahora está trabajando para mejorar la especificidad de su sistema y aplicarlo a más tipos de células y órganos para tratar una gama más amplia de enfermedades humanas. así como para rejuvenecer órganos específicos y revertir el proceso de envejecimiento y las condiciones relacionadas con la edad como la pérdida de audición y la degeneración macular. Se necesitarán más pruebas de seguridad antes de los ensayos en humanos, ellos dicen.