Crédito:Universidad de Zhejiang
Las terapias macromoleculares sin fármacos pueden inducir la apoptosis celular al agrupar receptores de superficie celular que no se internalizan. Estos muestran una enorme promesa en el tratamiento de tumores, particularmente en términos de toxicidades no específicas en comparación con medicamentos de bajo peso molecular. Sin embargo, la mayoría de las terapias macromoleculares sin fármacos informadas implican una forma de administración en "dos pasos" y hay escasez de investigación in vivo.
El 23 de diciembre de 2021, el equipo de investigación dirigido por el Prof. Du Yongzhong en la Facultad de Ciencias Farmacéuticas de la Universidad de Zhejiang, publicó un artículo titulado "Macromoléculas 'libres de drogas' controladas espaciotemporalmente por luz a través de nanopartículas de conversión ascendente para una terapia tumoral precisa" en el diario Nano hoy .
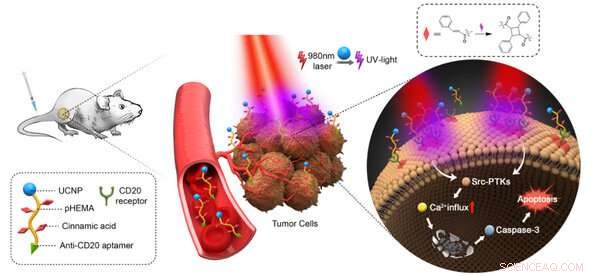
El equipo de Du sintetizó macromoléculas "libres de drogas" controladas por luz que consisten en nanopartículas de conversión ascendente, aptámeros, polímeros solubles en agua y grupos cinamato (CA). Estas macromoléculas se acumularon primero en gran medida en los sitios tumorales mediados por aptámeros y se localizaron con precisión en los receptores en la superficie de las membranas de las células tumorales. Las nanopartículas de conversión ascendente convirtieron la luz del infrarrojo cercano en luz ultravioleta e indujeron el entrecruzamiento de los grupos CA, lo que resultó en la agrupación de los receptores CD20 y la apoptosis celular. No se produjo apoptosis en los sitios libres de luz. Por lo tanto, los tumores podrían tratarse con precisión de manera segura y eficiente. Esta estrategia fue confirmada por administración in situ e intravenosa en animales modelo tumorales.
"Esta terapia macromolecular sin fármaco sintetizada in situ y controlada por conversión ascendente del infrarrojo cercano amplía el repertorio de fármacos macromoleculares y abre una nueva vía para la terapia tumoral", dijo Du. Estrategia antitumoral precisa lograda a través de nanopartículas dopadas con lantánidos fotoconmutables