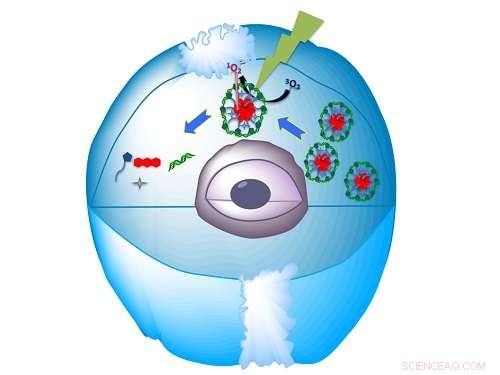
El nanomaterial biocompatible autoensamblado entrega el miARN a la célula y luego lo libera cuando lo golpea la luz. Crédito:KAUST
Los investigadores de la Universidad de Ciencia y Tecnología King Abdullah (KAUST) de Arabia Saudita han desarrollado un diminuto sistema de administración terapéutica que puede controlar la capacidad del cuerpo para fabricar proteínas.
Los genes contienen las instrucciones para fabricar las proteínas que componen nuestro cuerpo. La información genética se traduce en las proteínas necesarias para construir células vivas mediante un proceso de transcripción en el que el código genético del ADN se copia en una molécula grande conocida como ARN mensajero (ARNm).
Este proceso de transcripción se puede alterar mediante la introducción de cadenas dobles cortas de ARN, referido como ARN interferente pequeño (ARNip), que se une al ARNm e inhibe la expresión de genes particulares. Aprovechar esta interferencia de ARN para aplicaciones terapéuticas es difícil y requiere un material que pueda proteger el ARNip mientras viaja a través del torrente sanguíneo. ayudándola a penetrar la membrana externa de la célula y llevarla a su ubicación objetivo.
"La entrega de ARN es muy complicada, ya que las células pueden digerirlo fácilmente. Se necesitan mejores vehículos para que se pueda administrar más ARN con el fin de editar genes". "dice Niveen Khashab del Laboratorio de Materiales Híbridos Inteligentes de KAUST.
Khashab y sus colegas ahora han demostrado nanoestructuras biocompatibles para entregar ARNip y silenciar genes de manera eficiente1. Combinaron la macromolécula histidina-capped-9, 10-dialcoxi-antraceno (HDA) y ARNip en agua. Observaron el autoensamblaje de nanopartículas esféricas cuando el agua era ligeramente ácida, pero no cuando era de pH neutro.
Khashab explica que estas nanoesferas son creadas por la interacción electrostática entre el HDA cargado positivamente y el ARN cargado negativamente, y luego los dos brazos largos del supramolecular HDA envuelven el ARNip para protegerlo.
"Nuestro enlazador orgánico puede interactuar con materiales genéticos mediante enlaces de hidrógeno y formar un vehículo de entrega, "explica Khashab." El enfoque es escalable y crea cantidades reproducibles de ARN encapsulado; también es biocompatible y seguro ".
Las nanopartículas también podrían activarse con luz visible. Cuando se irradia con radiación verde en presencia de un compuesto fluorescente ácido, conocido como eosina, la esfera se desmonta y libera el ARNip.
El equipo demostró la eficacia de la nanopartícula para la administración de fármacos en el linfoma de células B 2, una molécula de ARNm que crea proteínas para regular la muerte celular. Demostraron que sus nanoestructuras mejoran la eficacia del silenciamiento de genes y conducen a una eliminación de genes de más del 90 por ciento después de la exposición a la luz visible.
"El siguiente paso es modificar el diseño para entregar otras moléculas de carga, como proteínas, y mejorar la respuesta de la luz a longitudes de onda más altas en el infrarrojo cercano, "dice Khashab.