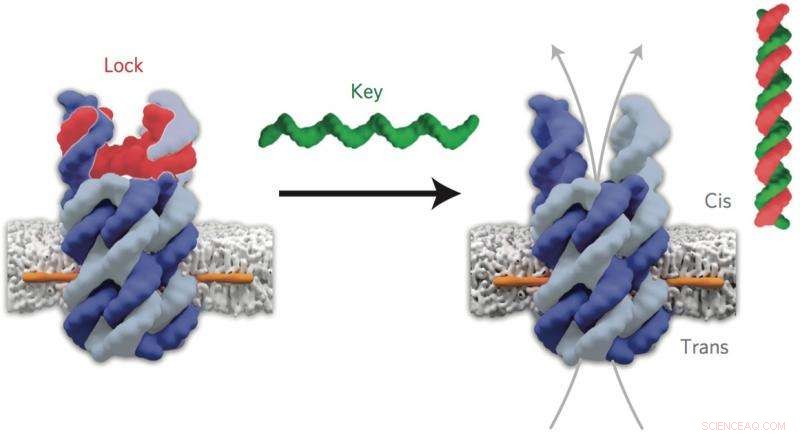
El ADN 'candado' (rojo) del nanoporo cerrado se une al ADN 'clave' (verde) para abrir el canal. Crédito:Jonathan Burns et al. Nanotecnología de la naturaleza, DOI 10.1038 / nnano.2015.279
El ADN se ha utilizado como un 'bloque de construcción molecular' para construir poros sintéticos bioinspirados que mejorarán la forma en que se administran los medicamentos y ayudarán a avanzar en el campo de la biología sintética. según científicos de UCL y Nanion Technologies.
El estudio, publicado hoy en Nanotecnología de la naturaleza y financiado por el Consejo de Investigación en Biotecnología y Ciencias Biológicas (BBSRC), Leverhulme Trust y UCL Chemistry, muestra cómo se puede utilizar el ADN para construir poros estables y predecibles que tienen una forma y una carga definidas para controlar qué moléculas pueden pasar a través del poro y cuándo.
Autor principal, Dr. Stefan Howorka (Química UCL), dijo:"Los poros biológicos naturales hechos de proteínas son esenciales para transportar carga dentro y fuera de las células biológicas, pero son difíciles de diseñar desde cero. El ADN ofrece una estrategia completamente nueva para construir poros sintéticos altamente específicos que podemos abrir y cerrar a pedido. Hemos diseñado nuestros poros para que actúen como puertas:la puerta se abre solo cuando se le proporciona la llave correcta. Al convertir estos poros en portadores de medicamentos, creemos que permitirá una orientación mucho más precisa de la terapéutica ".
Muchas terapias, incluidos los medicamentos contra el cáncer, se pueden transportar por el cuerpo en pequeños transportadores llamados vesículas que se dirigen a diferentes tejidos utilizando marcadores biológicos. Previamente, la liberación de los fármacos desde el interior de las vesículas se desencadenó con paredes de vesículas con fugas inducidas por la temperatura o con canales de péptidos insertados, que son menos rígidos y predecibles que el ADN.
Usando bloques de construcción de ADN, el equipo diseñó poros con estructuras predeterminadas y propiedades definidas que se anclaron con precisión en las paredes, o membranas, de las vesículas.
"Nuestros poros toman la forma de un barril abierto hecho de seis duelas de ADN. Diseñamos una compuerta molecular para cerrar una entrada pero luego reabrir el canal cuando una molécula específica se une. Se unieron anclajes con alta afinidad de membrana para atar el agua -poros solubles en la membrana aceitosa, "explicó el primer autor, Dr. Jonathan Burns (Química UCL).
Utilizando técnicas de electrofisiología, los investigadores verificaron que el poro se extendía verticalmente por la superficie de la membrana y era estable con un ancho interno de 2 nm, que es un tamaño apropiado para que pasen pequeñas moléculas de fármacos.
El mecanismo de bloqueo y liberación de la puerta se probó con técnicas de electrofisiología y con fluoróforos. que son de tamaño equivalente a moléculas pequeñas. Como el poro del ADN tenía una carga neta negativa, los fluoróforos con una carga neta negativa se movían con más facilidad que los que tenían una carga neta positiva, mostrando selectividad por la que podría salir la carga. Quitar la cerradura con una llave coincidente aumentó el tráfico 140 veces en comparación con una llave no coincidente.
La coautora Astrid Seifert, que trabaja con el Dr. Niels Fertig en Nanion Technologies, dijo:"Pudimos analizar con precisión el rendimiento de cada uno de los poros que creamos. Primero insertamos poros en membranas y luego probamos la respuesta biofísica de cada canal usando microchips avanzados. No solo hemos desarrollado una nueva forma de diseñar altamente poros específicos, sino también un método automatizado para probar sus propiedades in situ, lo cual será importante para probar los poros que se utilizarán para la administración de fármacos dirigida en el futuro ".
Los investigadores planean probar los poros sintéticos en una variedad de escenarios, incluida la liberación de medicamentos contra el cáncer a las células y el desarrollo de poros que liberan biomoléculas farmacéuticamente activas.
Dr Howorka agregado, "Nuestro enfoque es un gran paso adelante en la construcción y el uso de estructuras biológicas sintéticas y promete una nueva era en el diseño de poros y la biología sintética. Hemos demostrado un control tan preciso sobre el comportamiento de los poros, tanto en términos de selectividad como de capacidad de respuesta, creemos que el método allana el camino para una amplia gama de aplicaciones, desde la administración de fármacos hasta la nanosensibilidad ".