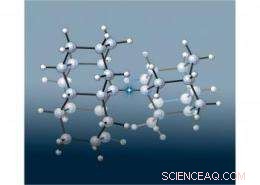
Un equipo de científicos europeos y de SLAC unió dos diminutas estructuras de "diamondoides" parecidas a un diamante para crear el enlace carbono-carbono más largo (resaltado en esta imagen por la estrella) jamás visto en un alcano. una clase de moléculas compuestas únicamente por carbono e hidrógeno conectadas por enlaces covalentes simples. Lo que fue sorprendente sin embargo, era que la molécula era mucho más estable de lo esperado, ya que los enlaces más largos suelen ser más débiles. Los investigadores determinaron que las fuerzas de atracción entre las diamondoides mejoraban la estabilidad de esta molécula. Imagen de Peter R. Schreiner, Universidad Justus-Liebig, Alemania.
(PhysOrg.com) - La fuerza de un enlace químico entre átomos es la base fundamental para la estabilidad y reactividad de una molécula. Ajustar la fuerza y la accesibilidad del enlace puede cambiar drásticamente las propiedades de una molécula. Por ejemplo, La fuerza de un enlace está directamente relacionada con su longitud:estirar un enlace más allá de su longitud normal lo debilita.
Pero una nueva investigación realizada por un equipo de dos universidades europeas y el SLAC National Accelerator Laboratory muestra que las fuerzas atractivas entre otras partes de una molécula pueden hacer que un enlace estirado que une dos átomos de carbono sea mucho más estable de lo esperado. Este resultado debería conducir a mejoras en la forma en que los científicos diseñan nuevas moléculas, materiales y catalizadores.
“Proporcionamos una comprensión de por qué las moléculas con enlaces excepcionalmente largos no necesariamente tienen que ser inestables, "Dijo Jeremy Dahl, un científico del Instituto Stanford de Ciencia de Materiales y Energía (SIMES), un instituto dirigido conjuntamente por SLAC y la Universidad de Stanford. Los colaboradores fueron Peter R. Schreiner de la Universidad Justus-Liebig en Alemania y Andrey A. Fokin del Instituto Politécnico de Kiev en Ucrania. Los resultados se publican hoy en Naturaleza .
Aunque es aplicable a todo tipo de moléculas, la nueva investigación involucra alcanos, una clase de moléculas compuestas solo por átomos de carbono e hidrógeno conectados por enlaces covalentes simples, y diamondoides, que son diamantes del tamaño de una molécula iniciados por los investigadores de SIMES. Etano El propano y el octano son alcanos familiares que tienen una columna vertebral de dos, tres y ocho átomos de carbono, respectivamente, todos unidos por enlaces simples. Los átomos de carbono en las diamondoides extremadamente rígidas están dispuestos en la misma forma tetraédrica que el diamante.
En su nueva investigación, los científicos unieron pares de diamondoides para crear tres nuevos alcanos que tenían un enlace carbono-carbono ultralargo en el medio. Para acomodar las voluminosas diamondoides, el enlace central tenía que extenderse mucho más allá de la longitud normal del enlace carbono-carbono de 1,54 angstroms. (Angstrom, o Å, es una décima de nanómetro.) Una de las nuevas moléculas tenía el enlace carbono-carbono más largo jamás medido en un alcano:1,704 Å.
Asombrosamente, estas nuevas moléculas de doble diamondoide resultaron ser mucho más estables de lo esperado. Investigaciones anteriores de otros grupos habían demostrado que un alcano con un enlace carbono-carbono de 1,65 Å sobrevivía menos de una hora a 167 ° C (333 ° F). A diferencia de, el enlace central carbono-carbono en dos de las nuevas moléculas de diamondoides unidas se rompió solo después de calentarse por encima de los 300 ° C (572 ° F). El tercero, con el enlace carbono-carbono de 1.704Å, duró hasta que se calentó a 220 ° C (428 ° F).
"Basado solo en la longitud del enlace carbono-carbono, Esperaba que estas moléculas diamondoides fueran mucho menos estables de lo que demostraron ser, ”Dijo Schreiner. "Algo más tenía que estar sucediendo para mantener unidas estas nuevas moléculas".
¿Qué marcó la diferencia? Estructura de cristal de rayos X, resonancia magnética nuclear, y estudios termogravimétricos realizados por los colegas europeos de Dahl mostraron que incluso cuando los lazos se estiraron, las fuerzas de atracción entre las dos diamondoides las estaban acercando. Estas fuerzas de atracción generalmente se ven entre moléculas separadas, donde se denominan fuerzas de van der Waals en honor al físico holandés que las describió por primera vez en 1873. “Los científicos generalmente no consideran las atracciones de van der Waals cuando analizan la estabilidad de una sola molécula, pero ahora parece que deberían hacerlo, —Dijo Dahl.
Los hallazgos de la investigación del grupo fueron respaldados por cálculos sofisticados que permitieron a los científicos encender y apagar las fuerzas atractivas cuando evaluaron la estabilidad de las nuevas moléculas.
Schreiner agregó que este hallazgo puede explicar por qué el análisis convencional predice que los alcanos ramificados, que contienen grandes grupos de átomos unidos a la columna vertebral del alcano, son mucho menos estables de lo que realmente son. y por qué los diamondoides tienen puntos de fusión mucho más altos de lo esperado.
Estos resultados son los últimos de varios hallazgos de investigación interesantes y aplicaciones para diamondoides desde que Dahl y su colega Robert Carlson desarrollaron una forma de aislar cantidades significativas de ellos del petróleo crudo en 2003.
Entre sus interesantes propiedades, los diamondoides emiten electrones de manera extremadamente eficiente. En un trabajo publicado en Science en 2007, Los científicos de SIMES Zhi-Xun Shen, Wanli Yang y Nick Melosh, además de Dahl, Carlson y el Grupo Schreiner:demostraron que las diamondoides emiten fácilmente electrones en un rango de energía muy estrecho, una propiedad que podría mejorar las capacidades de obtención de imágenes de varios tipos de microscopios electrónicos, así como el patrón de haz de electrones utilizado para fabricar chips de computadora.
Las diamondoides también son altamente personalizables, lo que significa que se pueden producir y modificar diferentes variedades para cumplir con diferentes especificaciones:cristales tridimensionales para aplicaciones que requieren un material en polvo, películas bidimensionales para recubrir otros materiales, y posiblemente incluso nanocables unidimensionales para transferir carga o luz.
“Estos últimos resultados muestran que la fabricación de moléculas en nuevas formas y tamaños puede conducir a descubrimientos sorprendentes, —Dijo Dahl.