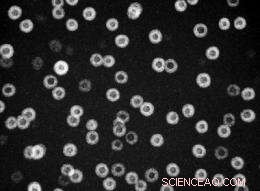
Cuando el aluminio se alea con las proporciones adecuadas de escandio y litio a través de una simple serie de tratamientos térmicos, Se forman inclusiones de nanopartículas en la matriz de aluminio (fondo oscuro) cuyos núcleos, hecho de aluminio, escandio, y litio (ojeras), varían en diámetro y cuyas conchas, hecho de aluminio y litio (anillos brillantes), varían en espesor. Pero sus diámetros generales son notablemente uniformes. Crédito:Laboratorio Nacional Lawrence Berkeley
Mucho antes de que supieran que lo estaban haciendo, desde el primer motor de avión de los hermanos Wright, los metalúrgicos estaban incorporando nanopartículas en aluminio para hacer un fuerte, duro, aleación resistente al calor. El proceso se llama precipitación en estado sólido, en el cual, después de que la masa fundida se haya enfriado rápidamente, los átomos de los metales de aleación migran a través de una matriz sólida y se juntan en partículas dispersas medidas en mil millonésimas de metro, sólo unos pocos átomos de ancho.
La clave de la resistencia de estas aleaciones endurecidas por precipitación es el tamaño, forma, y uniformidad de las nanopartículas y cuán estables son cuando se calientan. Una aleación con una combinación de propiedades de gran éxito es una formulación particular de aluminio, escandio, y litio, cuyos precipitados son todos casi del mismo tamaño. Fue elaborado por primera vez en el Laboratorio Nacional Lawrence Berkeley del Departamento de Energía de los Estados Unidos (Berkeley Lab) en 2006 por un equipo dirigido por Velimir Radmilović y Ulrich Dahmen de la División de Ciencias de los Materiales.
Estos científicos y sus colegas ahora han combinado observaciones a escala atómica con el poderoso microscopio TEAM en el Centro Nacional de Microscopía Electrónica (NCEM) de Berkeley Lab con tomografía de sonda atómica y otras técnicas experimentales. y con cálculos teóricos, para revelar cómo las nanopartículas que consisten en núcleos ricos en escandio y rodeados por capas ricas en litio pueden dispersarse en tamaños notablemente uniformes a lo largo de una matriz de aluminio puro.
"Con el microscopio TEAM pudimos estudiar la estructura núcleo-capa de estos nanoprecipitados y cómo forman esferas que tienen casi el mismo diámetro, "dice Dahmen, el director de NCEM y autor de la Materiales de la naturaleza artículo que describe los nuevos estudios. "Y lo que es más, estas partículas no cambian de tamaño con el tiempo, como hacen la mayoría de los precipitados. Típicamente, las partículas pequeñas se hacen más pequeñas y las partículas grandes se hacen más grandes, un proceso llamado maduración o engrosamiento, que eventualmente debilita las aleaciones. Pero estos nanoprecipitados uniformes de núcleo y capa resisten el cambio ".
Evolución de una aleación
En el sistema de aluminio-escandio-litio, los investigadores encontraron que, después del derretimiento inicial, Un simple proceso de calentamiento de dos pasos crea primero los núcleos ricos en escandio y luego las capas ricas en litio de las partículas esféricas. Las esferas autolimitan su crecimiento para alcanzar las mismas dimensiones externas, produciendo un peso ligero, potencialmente resistente al calor y a la corrosión, aleación superfuerte.
"El escandio es el fortalecedor más potente del aluminio, "dice Radmilović de NCEM, quien también es profesor de metalurgia en la Universidad de Belgrado, Serbia, y un autor de la Materiales de la naturaleza papel. "Agregar menos del uno por ciento de escandio puede marcar una diferencia dramática en la resistencia mecánica, resistencia a la fractura, resistencia a la corrosión:todo tipo de propiedades ". Debido a que el escandio se difunde muy lentamente a través de la matriz de aluminio sólido, la mezcla sólida debe calentarse a una temperatura alta (antes de que se derrita) antes de que precipite el escandio.
El litio es el más liviano de todos los metales (solo el hidrógeno y el helio son más livianos) y no solo aporta ligereza a una aleación de aluminio, sino que potencialmente, fuerza también. El litio se difunde mucho más rápidamente que el escandio, a una temperatura mucho más baja.
"El problema es ese, por sí mismo, el litio puede no estar a la altura de su promesa, "dice Dahmen, colaborador de Radmilović desde hace mucho tiempo. "El truco consiste en convencer al litio de que adopte una estructura cristalina útil, a saber, L1 2 . "
El L1 2 celda unitaria se asemeja a una celda cúbica centrada en la cara, entre las estructuras cristalinas más simples y simétricas. Los átomos ocupan cada esquina de un cubo imaginario y están centrados en las seis caras del cubo; en la L1 2 estructura, los tipos de átomos de las esquinas pueden diferir de los de los centros de las caras. Para las inclusiones de aleación, es una de las estructuras más fuertes y estables porque, como explica Dahmen, "una vez que los átomos están en su lugar en L1 2 , es difícil para ellos moverse ".
Dahmen atribuye a Radmilović la "intuición" de alear tanto el escandio como el litio con aluminio, calentar y enfriar el material en una serie específica de pasos. Esa intuición se basó en la larga experiencia de Radmilović con las propiedades separadas de las aleaciones de aluminio-litio y aluminio-escandio y un profundo conocimiento de cómo era probable que interactuaran. Elaboró una receta para las proporciones de los ingredientes en la fusión inicial y cómo enfriarlos y recalentarlos.
La clave del proceso fue utilizar litio como una especie de catalizador para forzar un "estallido de nucleación" en el escandio. Después de mezclar los tres metales, Derretido, y rápidamente enfriado o apagado, El litio sirve para reducir el calentamiento necesario para convencer al escandio para que forme estructuras de núcleo densas, aunque la mezcla sólida aún debe calentarse a 450 grados Celsius (842 Fahrenheit) durante 18 horas para formar estos núcleos. hecho de aluminio, litio, y escandio. Los núcleos tienen un promedio de un poco más de nueve nanómetros de diámetro, pero no son de tamaño uniforme.
A continuación, la aleación se vuelve a calentar, esta vez a 190˚ Celsius (374˚ F) durante cuatro horas. A la temperatura más baja, el escandio está inmóvil; el litio que se mueve libremente forma una capa alrededor de los núcleos ricos en escandio, tanto como el agua en una nube se cristaliza alrededor de una mota de polvo para formar un copo de nieve. Las conchas tienen un promedio de aproximadamente 10,5 nanómetros de espesor, pero su grosor no es uniforme.
Lo que es notable aunque, es que cuando un núcleo es más grueso que el promedio, el caparazón es más delgado que el promedio, y viceversa:cuanto más pequeño es el núcleo, cuanto más rápido crece la cáscara. El tamaño del núcleo y el tamaño de la carcasa están "anticorrelacionados" y el resultado es "centrado en el tamaño". Esferas enteras todavía varían un poco, pero las diferencias son mucho menores que entre los núcleos solos o los proyectiles solos.

El L1 2 la estructura se muestra en la parte inferior izquierda, con átomos de aluminio en gris y átomos de escandio o litio de color verde rojizo. En imágenes de una nanopartícula de núcleo-capa fabricada por el microscopio TEAM de NCEM, cada punto muestra la parte superior de una columna de átomos; los tipos de átomos en cada columna se pueden calcular a partir del brillo y el contraste de los puntos. La matriz de aluminio tiene una estructura cúbica centrada en las caras en la que todos los átomos son de aluminio, mientras que en la L1 2 estructura las posiciones centradas en la cara también son de aluminio. Pero en el núcleo de la nanopartícula (arriba a la derecha), las columnas en las esquinas de la L1 2 la celda unitaria es una mezcla de aluminio, litio, y átomos de escandio, mientras que en el caparazón circundante (abajo a la derecha), las columnas de las esquinas son una mezcla de aluminio y litio. Crédito:Laboratorio Nacional Lawrence Berkeley
La estructura de los núcleos y carcasas incrustados en aluminio parece igualmente notable. El aluminio puro en sí tiene una estructura cúbica centrada en la cara, y esta estructura se repite a la perfección por el L1 2 estructura tanto de los núcleos como de las cáscaras, perfectamente unido sin dislocaciones en las interfaces entre el núcleo, cascarón, y matriz.
Dahmen dice:"Son los núcleos ricos en escandio los que convencen al litio de que adopte la útil L1 2 estructura."
Uniendo el experimento con la teoría
Usando el microscopio TEAM y una técnica de imagen especial para mirar hacia abajo en la parte superior de las filas regulares de columnas de átomos, la L1 2 la estructura se revela en grupos de cuadrados entrelazados, con cuatro columnas de átomos en las esquinas y cinco columnas de átomos en los centros alineados de las caras.
En aluminio puro, todos los puntos tienen el mismo brillo. En las conchas y núcleos sin embargo, las columnas de las esquinas y las columnas centradas en las caras difieren en contraste:las columnas centradas en las caras son de aluminio puro, pero las columnas de las esquinas están mezcladas. Al complementar las imágenes TEAM de alta resolución con datos de otras técnicas experimentales, fue posible utilizar el brillo y el contraste para calcular los tipos de átomos en cada columna.
Empleando cálculos de primeros principios, Los miembros del equipo Colin Ophus y Mark Asta pudieron modelar el efecto del litio en la precipitación de escandio en estado sólido, estimulando un repentino estallido de nucleación, y también para entender por qué, debido a las propiedades termodinámicas de los dos metales que interactúan con el aluminio y entre sí, los precipitados son tan uniformes y estables.
Radmilović dice:"Colin y Mark demostraron que el litio y el escandio se asemejan entre sí. También demostraron que al usar las columnas de aluminio como estándar, podemos calcular la intensidad del escandio y el litio por el brillo de la mancha ". En las conchas, las columnas de las esquinas contienen aluminio y aproximadamente un 10 por ciento de litio. En los núcleos las columnas de las esquinas contienen los tres metales.
Dahmen dice:"En los últimos años ha habido un rápido aumento en el uso de la 'microscopía integradora', utilizando una variedad de técnicas como imágenes de campo oscuro anulares de gran angular, contraste de fase de alta resolución, e imágenes y espectroscopia con filtrado de energía para atacar un solo problema. El microscopio TEAM, que se corrige por aberración cromática y esférica, es único en su capacidad para realizar todas estas técnicas con alta resolución. Comprender por qué las nanoinclusiones en aluminio-escandio-litio son uniformes es uno de los mejores ejemplos de la necesidad de utilizar la microscopía integradora ".
Tan buena aleación como es el aluminio-escandio-litio, su uso puede estar limitado por el costo de escandio raro, actualmente diez veces el precio del oro. Al comprender cómo la aleación logra sus características notables, los investigadores esperan plenamente que otros sistemas con precipitados núcleo-capa puedan controlarse mediante los mismos mecanismos, dando lugar a nuevos tipos de aleaciones con una gama de propiedades deseables.