
Un estudio en SLAC y Stanford identificó qué pares de átomos en una nanopartícula de catalizador son más activos en una reacción que descompone un gas de escape nocivo en los convertidores catalíticos. Las partículas más activas contenían la mayor proporción de una configuración atómica particular, una en la que había dos átomos, cada uno rodeado por siete átomos vecinos, Forme parejas para llevar a cabo los pasos de reacción. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
Reemplazar los costosos metales que descomponen los gases de escape en los convertidores catalíticos por más baratos, materiales más eficaces es una prioridad para los científicos, tanto por razones económicas como medioambientales. Se requieren catalizadores para realizar reacciones químicas que de otro modo no ocurrirían, como convertir los gases contaminantes de los gases de escape de los automóviles en compuestos limpios que pueden liberarse al medio ambiente. Para mejorarlos, los investigadores necesitan una comprensión más profunda de cómo funcionan exactamente los catalizadores.
Ahora, un equipo de la Universidad de Stanford y el Laboratorio Nacional de Aceleración SLAC del Departamento de Energía han identificado exactamente qué pares de átomos en una nanopartícula de paladio y platino, una combinación comúnmente utilizada en convertidores, son los más activos para descomponer esos gases.
También respondieron una pregunta que ha desconcertado a los investigadores de catalizadores:¿Por qué las partículas de catalizador más grandes a veces funcionan mejor que las más pequeñas? cuando esperas lo contrario? La respuesta tiene que ver con la forma en que las partículas cambian de forma durante el curso de las reacciones, creando más de esos sitios altamente activos.
Los resultados son un paso importante hacia la ingeniería de catalizadores para un mejor desempeño tanto en los procesos industriales como en los controles de emisiones. dijo Matteo Cargnello, profesor asistente de ingeniería química en Stanford que dirigió el equipo de investigación. Su informe fue publicado el 17 de junio en procedimientos de la Academia Nacional de Ciencias .
"El resultado más emocionante de este trabajo fue identificar dónde ocurre la reacción catalítica, en qué sitios atómicos se puede realizar esta química que toma un gas contaminante y lo convierte en agua y dióxido de carbono inofensivos. que es increíblemente importante e increíblemente difícil de hacer, ", Dijo Cargnello." Ahora que sabemos dónde están los sitios activos, podemos diseñar catalizadores que funcionen mejor y utilicen ingredientes menos costosos ".
Se requieren catalizadores para realizar reacciones químicas que de otro modo no ocurrirían, como convertir los gases contaminantes de los gases de escape de los automóviles en compuestos limpios que pueden liberarse al medio ambiente. En el convertidor catalítico de un automóvil, nanopartículas de metales preciosos como paladio y platino se adhieren a una superficie de cerámica. A medida que fluyen los gases de emisión, Los átomos en la superficie de las nanopartículas se adhieren a las moléculas de gas que pasan y las estimulan a reaccionar con el oxígeno para formar agua. dióxido de carbono y otros productos químicos menos dañinos. Una sola partícula cataliza miles de millones de reacciones antes de agotarse.
Los convertidores catalíticos actuales están diseñados para funcionar mejor a altas temperaturas, Cargnello dijo:razón por la cual la mayoría de las emisiones de escape nocivas provienen de vehículos que recién comienzan a calentarse. Con más motores diseñados para trabajar a temperaturas más bajas, Existe una necesidad imperiosa de identificar nuevos catalizadores que funcionen mejor a esas temperaturas, así como en barcos y camiones que es poco probable que cambien a funcionamiento eléctrico en el corto plazo.
Pero, ¿qué hace que un catalizador sea más activo que otro? La respuesta ha sido esquiva.
En este estudio, El equipo de investigación analizó las nanopartículas catalizadoras hechas de platino y paladio desde dos perspectivas, la teoría y el experimento, para ver si podían identificar estructuras atómicas específicas en su superficie que contribuyan a una mayor actividad.
Partículas más redondas con bordes irregulares
Por el lado de la teoría, El científico del personal de SLAC, Frank Abild-Pedersen, y su grupo de investigación en el Centro SUNCAT para la ciencia de la interfaz y la catálisis crearon un nuevo enfoque para modelar cómo la exposición a gases y vapor durante las reacciones químicas afecta la forma y la estructura atómica de una nanopartícula catalítica. Esto es computacionalmente muy difícil, Abild-Pedersen dijo:y estudios previos habían asumido que las partículas existían en el vacío y nunca cambiaban.
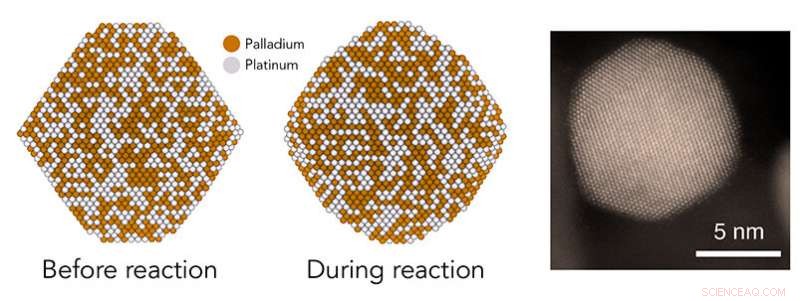
En un estudio en SLAC y Stanford, los teóricos predijeron que las nanopartículas de catalizador hechas de paladio y platino (izquierda) se volverían más redondas durante ciertas reacciones químicas (centro), creando características escalonadas con pares de átomos que son sitios catalíticos especialmente activos. Experimentos e imágenes de microscopio electrónico como la de la derecha confirmaron que este es el caso, ofreciendo una nueva comprensión de cómo funcionan los catalizadores. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
Su grupo creó formas nuevas y más simples de modelar partículas de una manera más compleja, entorno realista. Los cálculos de los investigadores postdoctorales Tej Choksi y Verena Streibel sugirieron que a medida que avanzan las reacciones, las nanopartículas de ocho lados se vuelven más redondas, y su piso, Las superficies en forma de facetas se convierten en una serie de pequeños escalones dentados.
Al crear y probar nanopartículas de diferentes tamaños, cada uno con una proporción diferente de bordes dentados a superficies planas, el equipo esperaba encontrar exactamente qué configuración estructural, e incluso qué átomos, contribuyó más a la actividad catalítica de las partículas.
Un poco de ayuda del agua
Ángel yang un doctorado estudiante en el grupo de Cargnello, hizo nanopartículas de tamaños controlados con precisión, cada una de las cuales contenía una mezcla distribuida uniformemente de átomos de paladio y platino. Para hacer esto, tuvo que desarrollar un nuevo método para hacer las partículas más grandes sembrándolas alrededor de las más pequeñas. Yang usó rayos X de la fuente de luz de radiación sincrotrón de Stanford de SLAC para confirmar la composición de las nanopartículas que hizo con la ayuda de Simon Bare de SLAC y su equipo.
Luego, Yang realizó experimentos en los que se usaron nanopartículas de diferentes tamaños para catalizar una reacción que convierte el propeno, uno de los hidrocarburos más comunes presentes en los gases de escape, en dióxido de carbono y agua.
"El agua aquí jugó un papel particularmente interesante y beneficioso, ", dijo." Normalmente envenena, o desactiva, catalizadores. Pero aquí la exposición al agua hizo que las partículas se redondearan y abriera sitios más activos ".
Los resultados confirmaron que las partículas más grandes eran más activas y que se volvían más redondas y dentadas durante las reacciones. como predijeron los estudios computacionales. Las partículas más activas contenían la mayor proporción de una configuración atómica particular, una en la que había dos átomos, cada uno rodeado por siete átomos vecinos, Forme parejas para llevar a cabo los pasos de reacción. Fueron estos "7-7 pares" los que permitieron que las partículas grandes funcionaran mejor que las más pequeñas.
Avanzando, Yang dijo:espera descubrir cómo sembrar nanopartículas con materiales mucho más baratos para reducir su costo y reducir el uso de metales preciosos raros.
Interés de la industria
La investigación fue financiada por BASF Corporation, un fabricante líder de tecnología de control de emisiones, a través de la Alianza de Investigación de California, que coordina la investigación entre los científicos de BASF y siete universidades de la costa oeste, incluido Stanford.
"Este documento aborda cuestiones fundamentales sobre los sitios activos, con la teoría y las perspectivas experimentales que se unen de una manera realmente agradable para explicar los fenómenos experimentales. Esto nunca se ha hecho antes, y por eso es bastante significativo, "dijo Yuejin Li, un científico principal senior de BASF que participó en el estudio.
"En el final, " él dijo, "Queremos tener un modelo teórico que pueda predecir qué metal o combinación de metales tendrá una actividad incluso mejor que nuestro estado actual de la técnica".