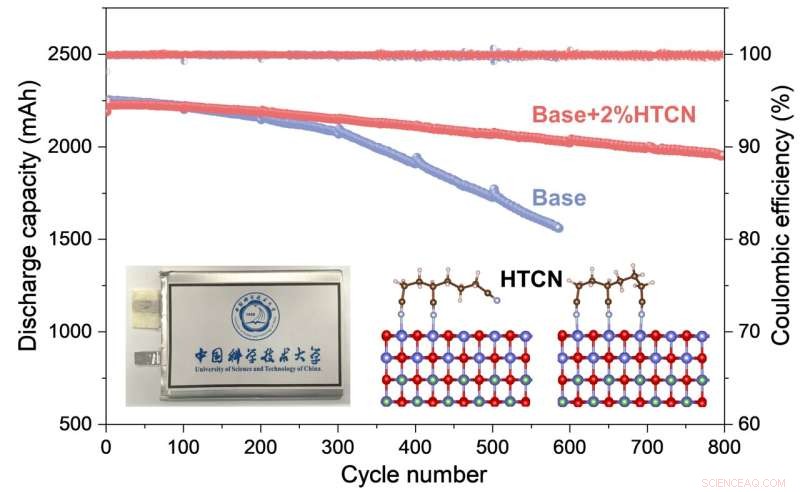
El rendimiento electroquímico y el mecanismo de trabajo del aditivo HTCN en LiCoO2 de alto voltaje cátodo para celdas de bolsa prácticas se estudian exhaustivamente. Crédito:Nano Investigación
Los nitrilos, un compuesto orgánico con un átomo de carbono unido por triple enlace a un átomo de nitrógeno, se agregan comúnmente a la fórmula de electrolitos para las baterías que utilizan un cátodo de óxido de cobalto y litio, lo que hace que dichas baterías estén mucho más cerca de alcanzar su rendimiento teórico completo. Hasta ahora, los investigadores de baterías no han entendido realmente por qué estos nitrilos funcionan de esta manera. Pero un grupo de electroquímicos ha utilizado técnicas de microscopía avanzadas para observar más de cerca lo que sucede a escala molecular e identificar lo que está sucediendo, abriendo nuevas vías para mejorar aún más el rendimiento de la batería.
El estudio fue publicado en la revista Nano Research el 22 de septiembre de 2022.
Óxido de cobalto de litio (LiCoO2 , o simplemente "LCO") es el material más utilizado para los cátodos, los electrodos positivos, en las baterías de iones de litio. Esto es especialmente cierto para las baterías utilizadas en dispositivos electrónicos portátiles gracias al alto voltaje operativo de LCO, su alta capacidad y la estabilidad de su rendimiento a largo plazo.
Pero lo que ha hecho que los cátodos LCO sean particularmente atractivos es que ofrecen más energía en una cantidad de espacio más pequeña (mayor densidad de energía), lo cual es muy útil para dispositivos de consumo más pequeños, como teléfonos, relojes inteligentes y dispositivos que tienen limitaciones de espacio aún más estrictas, como como sensores inteligentes domésticos e industriales.
Sin embargo, por el momento, los cátodos LCO solo pueden entregar aproximadamente la mitad de su capacidad específica teórica. Esto significa que lo que realmente entregan es mucho menos de lo que teóricamente deberían poder producir. Y, por lo tanto, a menudo les resulta difícil satisfacer las crecientes demandas de densidad de energía de los dispositivos electrónicos portátiles.
Una forma de sortear este obstáculo sería aumentar el voltaje de carga limitado de las baterías que usan cátodos LCO. La tensión de carga limitada describe el punto en el que se considera que una batería está completamente cargada. Más allá de este punto, la batería podría dañarse y muchos dispositivos simplemente se apagan cuando se alcanza el umbral de corte. Este umbral se establece de manera un tanto arbitraria, por lo que podría aumentarse, y tal operación de alto voltaje promete dar un impulso de densidad de energía a tales baterías.
Pero aquí surge un nuevo problema:la operación de alto voltaje puede exacerbar las reacciones químicas dañinas en la interfaz entre el cátodo y el electrolito. Esto puede provocar grietas y otros daños internos, que a su vez pueden deteriorar aún más la interfaz entre los electrodos. En última instancia, todo esto puede resultar en una disminución radical de la capacidad de la batería y un fuerte aumento de los problemas de seguridad. La temperatura de trabajo en estos dispositivos puede alcanzar los 45 ℃ debido a su propia generación de calor, lo que acorta aún más la vida útil de la batería.
Y así, desde hace algún tiempo, mezclar compuestos adicionales a la fórmula del electrolito para ajustar la actividad de reacción del electrolito (el medio que contiene iones que ayuda a establecer una corriente a través del movimiento de iones positivos y negativos a través de él) en la interfaz entre el cátodo y electrolito ha demostrado ser una estrategia muy eficaz para disminuir la actividad de reacción de electrolitos.
Hay una serie de compuestos diferentes que se utilizan como aditivos de electrolitos, pero para las baterías de iones de litio, los nitrilos son quizás los más utilizados. Los nitrilos son cualquier compuesto orgánico que tiene una sección de la molécula (un grupo funcional) formada por un átomo de carbono con triple enlace a un átomo de nitrógeno.
Sin embargo, el mecanismo de trabajo de los aditivos de nitrilo en los cátodos de alto voltaje aún no se comprende completamente, particularmente en el tipo de baterías de bolsa LCO de alto voltaje prácticas y cotidianas. (Las baterías de bolsa son un tipo de batería "blanda" sin una carcasa de metal duro y, en cambio, cuyos componentes están encerrados en una película de plástico recubierta de aluminio, que se parece un poco a una "bolsa" de chicle o tabaco suelto. Desarrollada por primera vez en 1995 y permitiendo un uso mucho más eficiente del espacio, las baterías de bolsa se han convertido desde entonces en una opción común para los fabricantes debido a esta ventaja de diseño).
Hay dos teorías principales que intentan explicar el mecanismo de los aditivos de nitrilo, pero ambas tienen deficiencias significativas en su poder explicativo.
"Los nitrilos funcionan bien, pero realmente no sabemos por qué funcionan bien, por qué ocurre esta acción estabilizadora. Lo que está sucediendo exactamente sigue siendo bastante misterioso", dijo Shuhong Jiao, electroquímico de la Universidad de Ciencia y Tecnología de China. (USTC). "Y si no sabemos por qué está funcionando lo que estamos haciendo para mejorar las baterías, esto nos impide ajustar nuestros esfuerzos para mejorar las cosas aún más".
Por lo tanto, los investigadores tomaron un aditivo de electrolito de nitrilo común, un ligando tridentado que contenía 1,3,6-hexanotricarbonitrilo (o más simplemente HTCN) para tratar de arrojar luz sobre cuál es el mecanismo de los nitrilos para estabilizar un LiCoO2 de alto voltaje. cátodo.
Mientras la batería estaba funcionando, y superando con creces a un equivalente sin los aditivos de electrolito HTCN, los investigadores utilizaron microscopía electrónica para observar más de cerca lo que estaba sucediendo, combinado con un análisis de la composición de iones y elementos del sistema. Descubrieron que el aditivo HTCN inhibía de manera muy efectiva la generación de grietas y la disolución de iones de cobalto.
Luego, usando espectroscopía de fotoelectrones de rayos X combinada con una serie de cálculos teóricos, encontraron que las moléculas de HTCN se adsorbían (pegaban) de manera eficiente en la superficie de LCO y se incrustaban en la interfaz entre el cátodo y el electrolito, que en a su vez inhibe en gran medida una reacción de oxidación en la superficie del LCO, evitando así una descomposición continua del electrolito.
En conjunto, esto equivale a una interfaz mucho más estable entre el cátodo y el electrolito, lo que suprimió significativamente la descomposición de los componentes y la formación de grietas. Es esta estructura de cátodo-electrolito estable y densa la que mejora la estabilidad de la batería a través de una gran cantidad de ciclos de carga y descarga.
Al conocer esta comprensión a nivel molecular de cómo los aditivos de nitrilo dan un impulso a tales baterías, los investigadores ahora pueden buscar otras formulaciones de aditivos de electrolitos que produzcan una estructura de interfaz similar o mejor. Los aditivos químicos mejoran la estabilidad de las baterías de iones de litio de alta densidad