Los científicos del St. Jude Children's Research Hospital han publicado su trabajo sobre SJ3149, un compuesto con amplia actividad contra muchos tipos de cáncer, particularmente la leucemia mieloide aguda (AML). SJ3149 se adhiere a la proteína caseína quinasa 1 alfa (CK1α) relacionada con el cáncer, lo que lleva a su destrucción.
El trabajo está publicado en la revista Nature Communications. .
"Hemos creado un superpegamento molecular", dijo el coautor principal Zoran Rankovic, Ph.D., Departamento de Biología Química y Terapéutica de St. Jude. "SJ3149 es el primer degradador potente y selectivo de CK1α de su clase, que muestra eficacia en modelos de cáncer tanto in vitro como in vivo".
Los pegamentos moleculares actúan secuestrando el mecanismo natural de reciclaje de proteínas de la célula. El pegamento molecular recluta la proteína objetivo en una enzima que la marca para su destrucción mediante un proceso llamado degradación proteasomal. Para muchas proteínas relacionadas con el cáncer a las que los inhibidores de moléculas pequeñas convencionales no pueden atacar bien, los pegamentos moleculares pueden ser una alternativa terapéutica viable. Esto llevó a los científicos de St. Jude a desarrollar una gran biblioteca patentada de pegamentos moleculares y a examinarla contra una variedad de líneas celulares cancerosas, encontrando un resultado inicial.
Una vez que los investigadores optimizaron el impacto identificado, la molécula SJ3149 resultante mostró mayor potencia y menos efectos fuera del objetivo que compuestos similares. SJ3149 mostró una amplia y auspiciosa actividad anticancerígena incluso para un pegamento molecular, de ahí el apodo de "superpegamento". El compuesto también parece tener un perfil similar al de una clase de medicamentos contra el cáncer aprobados, los inhibidores murinos doble minuto 2 (MDM2), lo que indica además que puede tener utilidad clínica.
Los pegamentos moleculares son un pozo prometedor para encontrar nuevas terapias porque pueden apuntar a proteínas que antes no eran farmacológicas. Sin embargo, encontrar y adaptar estas moléculas al uso clínico ha sido un desafío. Identificar y refinar dicha molécula proporciona una prueba del concepto de que el enfoque de St. Jude puede acelerar este proceso de descubrimiento.
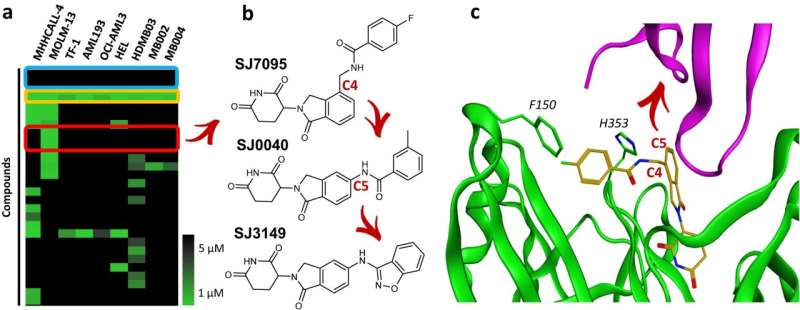
"Nuestro trabajo proporciona un modelo para realizar estudios similares para otros objetivos", dijo el coautor correspondiente Marcus Fischer, Ph.D., Departamento de Biología Química y Terapéutica de St. Jude. Los investigadores descubrieron el compuesto, lo modificaron mediante un diseño racional y probaron su eficacia. Para entender cómo el compuesto funcionó tan bien, el grupo de Fischer cristalizó el gran complejo de la proteína objetivo y SJ3149 se unió a la maquinaria celular responsable de marcar las proteínas para su degradación, un aparato de proteína ubiquitina ligasa.
"Pudimos ver que la belleza de este compuesto es que interactúa directamente con CK1α", explicó Fischer. "SJ3149 llega y conecta directamente CK1α con la enzima que la marca para la maquinaria de degradación celular, lo que explica la alta eficacia de degradación del compuesto".
Comprender cómo funcionan estos compuestos a nivel atómico puede allanar el camino para el diseño racional de pegamentos moleculares.
"Este es un ejemplo perfecto de cómo tomar materia química y generar conocimientos estructurales y mecanicistas para comprender la eficacia y la actividad celular", dijo el coautor correspondiente Jeffery Klco, MD, Ph.D., Departamento de Patología de St. Jude, médico científico. con un enfoque en ALD. "En esta etapa, todavía es sólo un compuesto líder, pero puede convertirse en otra opción potencial para tratar diferentes cánceres pediátricos, lo cual es emocionante".
La creación del complejo fue un gran esfuerzo de colaboración. El trabajo implicó diseñar, sintetizar y examinar la biblioteca de pegamentos moleculares, optimizar la química medicinal guiada por la estructura y realizar pruebas en células cancerosas derivadas de pacientes. Sólo fue posible gracias a la experiencia combinada de los laboratorios de Rankovic, Fischer y Klco, en colaboración con colaboradores internos y externos. El enfoque ahora se puede utilizar como base para futuros descubrimientos.
"La biología química ha entrado en un nuevo paradigma con los pegamentos moleculares", afirmó Rankovic. "Con este estudio, hemos establecido una línea para identificar nuevos pegamentos moleculares prometedores para tratamientos contra el cáncer".
Más información: Gisele Nishiguchi et al, Los degradadores selectivos de CK1α ejercen actividad antiproliferativa contra una amplia gama de líneas celulares de cáncer humano, Nature Communications (2024). DOI:10.1038/s41467-024-44698-1
Información de la revista: Comunicaciones sobre la naturaleza
Proporcionado por St. Jude Children's Research Hospital