Investigadores dirigidos por Satoshi Kamiguchi en el Centro RIKEN para la Ciencia de Recursos Sostenibles (CSRS) en Japón han descubierto una forma más ecológica de producir amoníaco, un compuesto esencial utilizado en fertilizantes.
El estudio, publicado en Chemical Science , describe un nuevo catalizador que funciona de manera estable a temperaturas relativamente bajas, reduciendo así la cantidad de energía y dinero necesarios para sintetizar amoníaco. Dado que el amoníaco es una forma excelente de almacenar hidrógeno de forma segura, así como un excelente combustible alternativo por derecho propio, este descubrimiento facilitará la transición de los combustibles fósiles a una economía de energía verde y neutra en carbono.
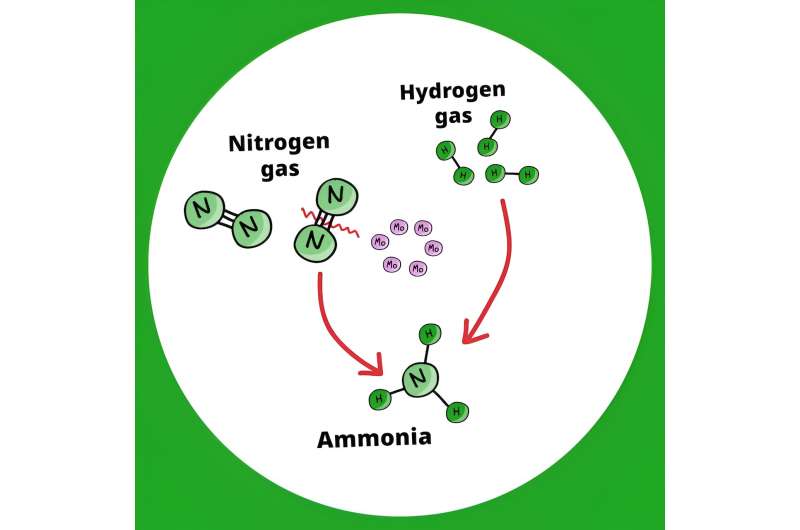
Los fertilizantes son una forma de proporcionar nitrógeno adicional a las plantas, lo que las ayuda a crecer y aumenta el rendimiento de los cultivos. El nitrógeno de los fertilizantes proviene del amoníaco, que se produce al descomponer el hidrógeno (H2 ) y nitrógeno (N2 ) moléculas y uniendo los elementos individuales en gas amoníaco (NH3 ) a través del proceso Haber-Bosch. La reacción requiere presión y temperaturas extremadamente altas, y un catalizador de hierro.
La presión y las temperaturas extremadamente altas (alrededor de 200 atm y 500 °C (932 °F)) necesarias para la reacción requieren una gran cantidad de energía. Debido a que el amoníaco se utiliza tan ampliamente en fertilizantes y otras industrias, la producción mundial consume una enorme cantidad de energía. Para ayudar a reducir la huella energética del amoníaco, los investigadores de RIKEN CSRS han desarrollado una reacción más respetuosa con el medio ambiente y la energía que puede proceder de forma estable a temperaturas mucho más bajas sin desactivarse.
El mayor obstáculo fue descomponer el gas nitrógeno porque existe un fuerte triple enlace entre los dos átomos de nitrógeno dentro de una molécula de gas nitrógeno. "El truco consistió en utilizar partículas metálicas de molibdeno ultrapequeñas preparadas a partir de un grupo de haluro metálico molecular hexanuclear, que luego se activó con gas hidrógeno", dice Kamiguchi.
Una vez activados, varios átomos de molibdeno trabajan juntos para romper los fuertes enlaces nitrógeno-nitrógeno e impulsar rápidamente la síntesis de amoníaco. Cuando se probó, este nuevo método pudo crear amoníaco a partir de gases de nitrógeno e hidrógeno de forma continua durante más de 500 horas a 200 °C (392 °F), lo que redujo en gran medida la temperatura requerida cuando se utiliza el proceso convencional Haber-Bosch.
Además de afectar a la industria de los fertilizantes, la nueva forma de producir amoníaco podría ayudar indirectamente a reducir las emisiones de carbono si se utilizara amoníaco como combustible en todo el mundo. El combustible de amoníaco se puede quemar directamente en motores de combustión interna sin emitir CO2. , pero no se ha convertido en una alternativa práctica debido al proceso Haber-Bosch de alta energía.
Una de las ventajas del nuevo método es que permitiría la producción de amoníaco con menor energía, lo que reduciría en gran medida las emisiones de carbono si se utiliza combustible de amoníaco a gran escala.
Al mismo tiempo que el amoníaco almacena nitrógeno para fertilizantes, también almacena hidrógeno. Esto lo convierte en un portador ideal de hidrógeno, que algunos consideran la fuente ideal de energía. Cuando se necesita el hidrógeno almacenado, se puede liberar del amoníaco y utilizarlo como combustible sin emitir dióxido de carbono.
"La sustitución del proceso Haber-Bosch por nuestro nuevo método debería suponer un ahorro de energía en todo el mundo", afirma Kamiguchi. "Si se utilizan combustible de amoníaco e hidrógeno en cantidades mucho mayores, reducir enormemente la energía necesaria para sintetizar el amoníaco conducirá a menores emisiones de CO2 y ayudar a prevenir un mayor calentamiento global."
Aún queda un problema. El hidrógeno necesario para producir amoníaco todavía se produce a partir de combustibles fósiles y, en las grandes cantidades necesarias, también produciría una enorme cantidad de CO2. emisiones y consumo de energía. Por lo tanto, Kamiguchi señala:"Cuando nuestro sistema catalizador se combina con H2 verde producción a partir de energías renovables, la emisión de CO2 que calienta el planeta podría reducirse aún más."
Actualmente, el equipo de investigación se centra en agregar promotores al catalizador a base de molibdeno que hará que la síntesis de amoníaco sea más eficiente.
Más información: Satoshi Kamiguchi et al, Síntesis catalítica de amoníaco en grupos de molibdeno de tamaño angstrom soportados por zeolita HY, Ciencia química (2024). DOI:10.1039/D3SC05447K
Información de la revista: Ciencias químicas
Proporcionado por RIKEN