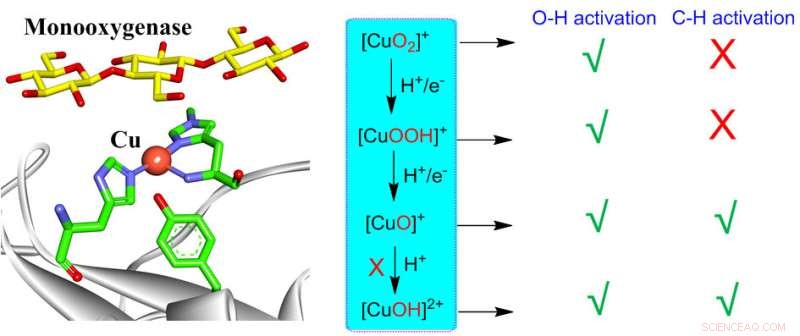
La activación de dioxígeno por cobre mononuclear en sistemas biológicos y sintéticos puede generar varios intermediarios cobre-oxígeno, incluido [CuO2 ] + , [CuOOH] + , [CuO] + , [CuOH] 2+ . Todas estas especies pueden realizar la activación de O-H, mientras que solo [CuO] + y [CuOH] 2+ son reactivos para la activación de C-H. Sin embargo, la formación de [CuOH] 2+ es altamente desfavorable en monooxigenasas, dejando [CuO] + como el único intermediario activo responsable de la activación de C-H en las monooxigenasas. Estos conocimientos pueden proporcionar una comprensión coherente de las reactividades de varias especies activas de cobre y oxígeno en sistemas biológicos y sintéticos. Crédito:Diario chino de catálisis
Las activaciones de dioxígeno constituyen uno de los problemas centrales en las metaloenzimas dependientes de cobre. Sobre O2 activación, las metaloenzimas dependientes del cobre, incluidas las metano monooxigenasas particuladas (pMMO), las polisacáridos monooxigenasas líticas (LPMO) y las enzimas binucleares de cobre PHM y DBM, pueden realizar activaciones de enlaces C-H/O-H desafiantes.
Mientras tanto, se han sintetizado complejos que contienen núcleos de cobre y oxígeno para imitar las especies activas de metaloenzimas. La activación de dioxígeno por el sitio activo de cobre mononuclear puede generar intermediarios cobre-oxígeno, incluidos Cu(II)-superoxo, Cu(II)-hidroperoxo, Cu(II)-oxilo, así como las especies de hidróxido de Cu(III).
Curiosamente, todas estas especies se han invocado como posibles intermediarios activos para las activaciones de C-H/O-H en sistemas biológicos o sintéticos. Debido a la escasa comprensión de las reactividades del complejo cobre-oxígeno, la naturaleza de las especies activas en los sistemas biológicos y sintéticos es muy controvertida.
Recientemente, un equipo de investigación dirigido por el profesor Binju Wang de la Universidad de Xiamen, China, midió las reactividades de varias especies mononucleares de cobre y oxígeno tanto en sistemas biológicos como sintéticos. El estudio muestra:
Se espera que estos conocimientos proporcionen una comprensión coherente de las reactividades de varias especies activas de cobre y oxígeno en sistemas biológicos y sintéticos.
La revisión se publicó en el Chinese Journal of Catalysis . Científicos revelan mecanismo de activación de dioxígeno