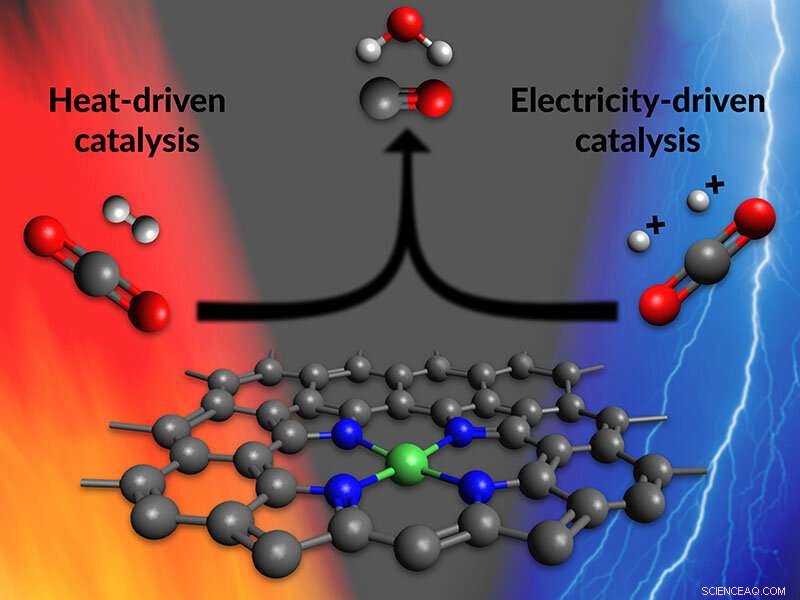
Esta ilustración muestra uno de los sitios activos de un nuevo catalizador que acelera el primer paso en la fabricación de combustibles y productos químicos útiles a partir del dióxido de carbono. Los sitios activos consisten en átomos de níquel (verde) unidos a átomos de nitrógeno (azul) y dispersos por un material de carbono (gris). Los investigadores de SLAC y Stanford descubrieron que este catalizador, llamado NiPACN, funciona en reacciones impulsadas por calor o electricidad, un paso importante para unificar la comprensión de las reacciones catalíticas en estos dos entornos de reacción muy diferentes. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
Prácticamente toda la producción de productos químicos y combustibles se basa en catalizadores, que aceleran las reacciones químicas sin consumirse en el proceso. La mayoría de estas reacciones tienen lugar en enormes recipientes de reactores y pueden requerir altas temperaturas y presiones.
Los científicos han estado trabajando en formas alternativas de impulsar estas reacciones con electricidad, en lugar de calor. Esto podría permitir eficiente, Fabricación distribuida alimentada por fuentes renovables de electricidad.
Pero los investigadores que se especializan en estos dos enfoques (calor versus electricidad) tienden a trabajar de forma independiente, desarrollando diferentes tipos de catalizadores adaptados a sus entornos de reacción específicos.
Una nueva línea de investigación apunta a cambiar eso. Científicos de la Universidad de Stanford y del Laboratorio Nacional Acelerador SLAC del Departamento de Energía informaron hoy que han creado un nuevo catalizador que funciona con calor o electricidad. Basado en átomos de níquel, el catalizador acelera una reacción para convertir el dióxido de carbono en monóxido de carbono, el primer paso para fabricar combustibles y productos químicos útiles a partir del CO 2 .
Los resultados representan un paso importante hacia la unificación de la comprensión de las reacciones catalíticas en estas dos condiciones muy diferentes con distintas fuerzas impulsoras en juego, dijo Thomas Jaramillo, profesor en SLAC y Stanford y director del Instituto SUNCAT de Ciencia de Interfaces y Catálisis, donde se llevó a cabo la investigación.
"Esta es una rareza en nuestro campo, ", dijo." El hecho de que podamos unirlo en un marco para ver el mismo material es lo que hace que este trabajo sea especial, y abre una vía completamente nueva para analizar los catalizadores de una manera mucho más amplia ".
Los resultados también explican cómo el nuevo catalizador impulsa esta reacción clave más rápido cuando se usa en un reactor electroquímico. dijo el equipo de investigación. Su informe apareció en la edición impresa de Angewandte Chemie esta semana.
Hacia un futuro de química sostenible
Encontrar formas de transformar el CO 2 en productos químicos, combustibles y otros productos, desde metanol hasta plásticos y gas natural sintético, es un enfoque importante de la investigación de SUNCAT. Si se hace a gran escala con energía renovable, podría crear incentivos de mercado para reciclar los gases de efecto invernadero. Esto requerirá una nueva generación de catalizadores y procesos para llevar a cabo estas transformaciones de manera económica y eficiente a escala industrial, y hacer esos descubrimientos requerirá nuevas ideas.
En busca de nuevas direcciones, SUNCAT formó un equipo de Ph.D. estudiantes que involucran a tres grupos de investigación en el departamento de ingeniería química de Stanford:Sindhu Nathan del grupo de la profesora Stacey Bent, cuya investigación se centra en reacciones catalíticas impulsadas por calor, y David Koshy, quien es co-asesorado por Jaramillo y el profesor Zhenan Bao y se ha centrado en las reacciones electroquímicas.
El trabajo de Nathan ha tenido como objetivo comprender las reacciones catalíticas impulsadas por calor en un aspecto fundamental, nivel atómico.
"Las reacciones impulsadas por el calor son lo que se usa comúnmente en la industria ahora, ", dijo." Y para algunas reacciones, un proceso impulsado por calor sería un desafío de implementar porque puede requerir temperaturas y presiones muy altas para que se produzca la reacción deseada ".
Conducir reacciones con electricidad podría hacer que algunas transformaciones sean más eficientes, Koshy dijo:"porque no tienes que calentar las cosas, y también puede hacer reactores y otros componentes más pequeños, más barato y modular; además, es una buena forma de aprovechar los recursos renovables ".
Los científicos que estudian estos dos tipos de reacciones trabajan en paralelo y rara vez interactúan, por lo que no tienen muchas oportunidades de obtener información mutua que pueda ayudarlos a diseñar catalizadores más efectivos.
Pero si los dos campos pudieran funcionar con el mismo catalizador, sentaría una base para unificar su comprensión de los mecanismos de reacción en ambos entornos, Dijo Jaramillo. "Teníamos razones teóricas para pensar que el mismo catalizador funcionaría en ambos conjuntos de condiciones de reacción, " él dijo, "pero esta idea no había sido probada".
Una nueva vía para el descubrimiento de catalizadores
Por sus experimentos, el equipo eligió un catalizador que Koshy sintetizó recientemente llamado NiPACN. Las partes activas del catalizador:los lugares donde agarra las moléculas que pasan, hace que reaccionen y libera los productos:consisten en átomos de níquel individuales unidos a átomos de nitrógeno que se encuentran dispersos por todo el material de carbono. La investigación de Koshy ya había determinado que NiPACN puede impulsar ciertas reacciones electroquímicas con alta eficiencia. ¿Podría hacer lo mismo en condiciones térmicas?
Para responder a esta pregunta, el equipo llevó el catalizador en polvo a la fuente de luz de radiación sincrotrón de Stanford (SSRL) de SLAC. Trabajaron con el científico de personal distinguido Simon Bare para desarrollar un pequeño reactor donde el catalizador podría acelerar una reacción entre el hidrógeno y el dióxido de carbono a altas temperaturas y presión. La configuración les permitió hacer brillar rayos X en la reacción a través de una ventana y ver cómo avanzaba la reacción.
En particular, Querían ver si las duras condiciones dentro del reactor cambiaban el catalizador, ya que facilitaba la reacción entre el hidrógeno y el CO. 2 .
"La gente podría decir, ¿Cómo sabes que la estructura atómica no cambió? ¿Haciendo de este un catalizador ligeramente diferente al que habíamos probado previamente en reacciones electroquímicas? ", dijo Koshy." Tuvimos que demostrar que los centros de reacción de níquel todavía se ven iguales cuando la reacción ha terminado ".
Eso es exactamente lo que encontraron cuando examinaron el catalizador en detalle atómico antes y después de la reacción con rayos X y microscopía electrónica de transmisión.
Avanzando, el equipo de investigación escribió, estudios como este serán fundamentales para unificar el estudio de los fenómenos catalíticos en los entornos de reacción, lo que, en última instancia, reforzará los esfuerzos para descubrir nuevos catalizadores para transformar las industrias química y de combustibles.