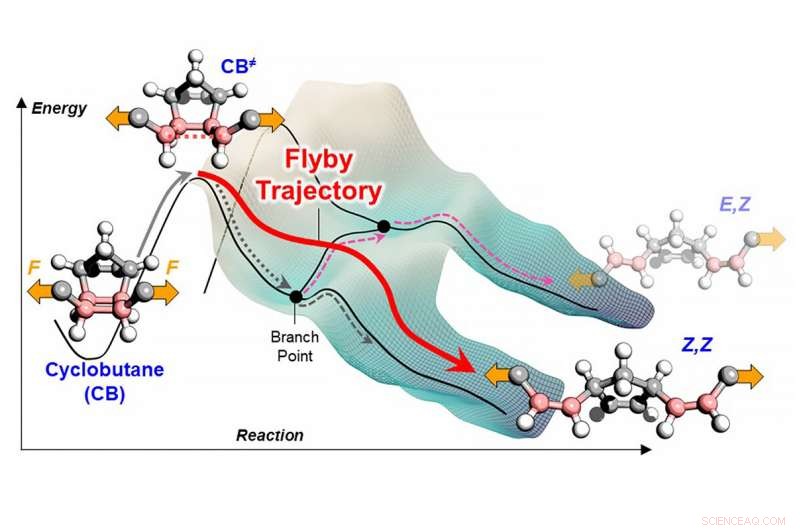
Una ilustración que muestra el movimiento de una molécula a través de una superficie de energía potencial en la forma en que los excursionistas siguen el mapa de contorno de montañas y valles a lo largo de un sendero. Cuando se aplica una fuerza mecánica, la energía aumenta y la molécula se excita, salta la barrera de energía inicial y tiene suficiente energía para continuar su "trayectoria de sobrevuelo" sobre la barrera de energía subsiguiente. Crédito:Yun Liu
Un nuevo estudio muestra que es posible utilizar la fuerza mecánica para alterar deliberadamente las reacciones químicas y aumentar la selectividad química, un gran desafío del campo.
El estudio dirigido por el investigador de Urbana-Champaign de la Universidad de Illinois, Jeffrey Moore, y el químico de la Universidad de Stanford, Todd Martinezz, demuestra cómo las fuerzas mecánicas externas alteran los movimientos atómicos para manipular los resultados de las reacciones. Los hallazgos del estudio se publican en la revista Ciencias .
"Pensamos en las reacciones químicas como moléculas que se mueven sobre una superficie de energía potencial en la forma en que los excursionistas siguen el mapa de contorno de montañas y valles a lo largo de un sendero, "dijo el autor principal Yun Liu, investigador postdoctoral en el grupo de investigación de Moore. "Una montaña a lo largo de una ruta de reacción es una barrera que debe atravesarse antes de que las moléculas puedan descender a su producto final. Por lo tanto, la altura relativa de las barreras controla qué camino probablemente elegirán las moléculas, permitiendo a los químicos hacer predicciones sobre lo que producirá una reacción química en particular, un resultado llamado selectividad ".
Los químicos han asumido tradicionalmente que el movimiento de las moléculas, conocido como "dinámica molecular", está gobernado por una superficie de energía potencial. Las moléculas se transforman mediante reacciones químicas que buscan el camino que requiere una cantidad mínima de energía. Sin embargo, La evidencia emergente muestra que las moléculas a menudo no tienen tiempo para tomar muestras de la superficie, conduciendo a desviaciones llamadas efectos dinámicos no estadísticos, dijeron los investigadores.
Se observan efectos dinámicos no estadísticos en algunas reacciones comunes como la nitración del benceno y las reacciones de deshidratación, "Dijo Liu." A pesar de estos ejemplos, Las ECM no han captado completamente la atención de los químicos porque son difíciles de medir y no se pueden controlar para cambiar los resultados de la reacción, la búsqueda esencial de la química ".
Liu desarrolló un diseño experimental utilizando una molécula de anillo marcada con un isótopo de carbono 13 con dos cadenas de polímero unidas. Liu colocó los polímeros en un recipiente de reacción y aplicó una fuerza mecánica mediante sonicación, que rasga el anillo en dos grupos separados.
"La molécula del anillo se puede convertir en uno de tres productos diferentes después de ser desgarrada, convirtiéndolo en un buen modelo para investigar ECM, "Dijo Liu." La etiqueta 13-C nos permite rastrear y medir los cambios químicos que ocurren en el anillo, haciéndolo distinto de miles de otros enlaces químicos en el polímero ".
Liu plantea la hipótesis de que con la excitación de la fuerza mecánica, los átomos se calientan a lo largo de direcciones de reacción específicas, en lugar de seguir las direcciones formadas por la superficie de energía potencial. Los investigadores llamaron a esta desviación del concepto convencional de reacciones químicas una "trayectoria de sobrevuelo".
"Utilizando el ejemplo de senderismo, la hipótesis equivale a decir que el excursionista simplemente decidió no seguir el mapa, "Dijo Liu." En cambio, el excursionista estaba lo suficientemente emocionado como para subirse a un ala delta y simplemente volar entre colinas en su descenso. Como resultado, la dirección en la que se mueven las moléculas depende de su salto inicial, en lugar de la altura de la barrera posterior ".
Liu realizó múltiples experimentos que demostraron la capacidad de sintonización de la trayectoria de sobrevuelo al aumentar la fuerza mecánica para que la reacción pueda superar cada vez más las barreras. Idealmente, los investigadores pueden convertir una reacción no selectiva en una altamente selectiva en la que los productos secundarios formados sean indetectables.
Para respaldar el hallazgo experimental, El estudiante graduado de la Universidad de Stanford, Soren Holm, recolectó 10, 000, 000 calcularon geometrías para construir un modelo teórico de la superficie de energía potencial y luego extrajeron la velocidad de las trayectorias de reacción bajo la presencia de fuerza mecánica.
"Descubrimos que las trayectorias tempranas no se ralentizan al pasar las barreras, "Dijo Liu.
En otras palabras, las barreras pasan volando en lugar de ser superadas, que debería haber ralentizado la velocidad de reacción química, dijeron los investigadores. Tiempo extraordinario, las moléculas se enfrían, y las trayectorias subsiguientes siguen la ruta de energía mínima inicialmente predicha.
"Nuestros hallazgos brindarán a los investigadores una comprensión más completa de cómo la fuerza puede alterar el curso de las reacciones químicas para aumentar la eficiencia de la producción". ", Dijo Moore." Es otra herramienta en nuestra caja de herramientas para hacer las cosas que usamos todos los días ".
La Fundación Nacional de Ciencias, la Oficina de Investigación del Ejército, la Fundación Dr. Leni Schoninger y la Deutsche Forschungsgemeinschaft apoyaron esta investigación.
Moore es el director del Instituto Beckman de Ciencia y Tecnología Avanzadas, es profesor de química y ciencias de los materiales e ingeniería y está afiliado al Centro de Estudios Avanzados, el Laboratorio de Investigación de Materiales, la Facultad de Medicina de Carle Illinois, el Instituto Carl R. Woese de Biología Genómica y el Centro de Ciencias Sociales y del Comportamiento.