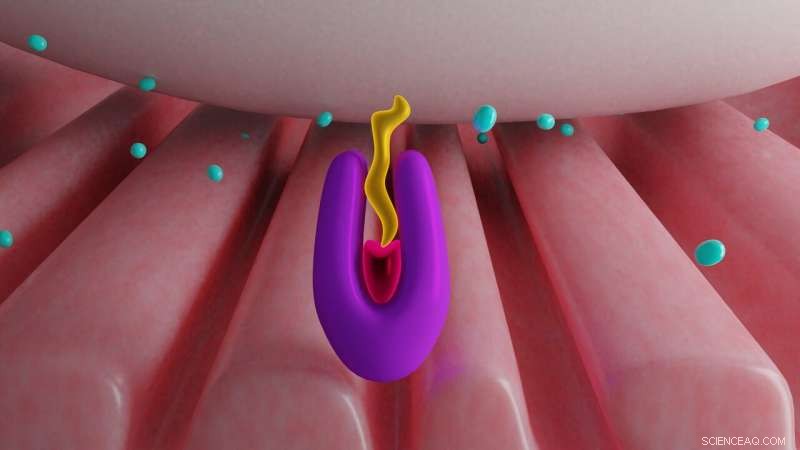
Un antídoto de acción rápida para mitigar los efectos de la intoxicación por organofosforados requiere un reactivador que pueda cruzar de manera efectiva y eficiente la barrera hematoencefálica. se unen libremente a la enzima, químicamente arrebatar el veneno y luego salir rápidamente. El Laboratorio Nacional Oak Ridge está utilizando datos de difracción de neutrones para mejorar un nuevo diseño de reactivador. Crédito:Michelle Lehman y Jill Hemman / ORNL, Departamento de Energía de EE. UU.
Elige tu veneno. Puede ser mortal por buenas razones, como proteger los cultivos de insectos dañinos o combatir la infección por parásitos como medicina, o para el mal como arma para el bioterrorismo. O, en cantidades extremadamente diluidas, se puede utilizar para realzar la belleza.
Si bien los ataques químicos dirigidos contra civiles tienden a aparecer en los titulares, los informes de intoxicación más comunes en los Estados Unidos son por exposición accidental a productos químicos domésticos como aerosoles para insectos, soluciones de limpieza o frutas o verduras mal lavadas. En todo caso, el remedio es de acción rápida, compuesto de droga que persigue veneno, y el Laboratorio Nacional de Oak Ridge está a la vanguardia en el desarrollo de una nueva generación de antídotos que salvan vidas.
Simplemente pon, "un veneno es algo que degrada gravemente su salud, o tu estado de salud, "dijo Andrey Kovalevsky, cristalógrafo y bioquímico en ORNL. Es un experto en la comprensión a nivel atómico de la función enzimática, unión a fármacos y resistencia a los fármacos. Usando neutrones y rayos X, estudia cómo funcionan las enzimas en el cuerpo y, dependiendo de los detalles, cómo inhibirlos o reactivarlos utilizando pequeñas moléculas orgánicas.
"Dependiendo del veneno y la cantidad, el efecto puede ser muy rápido (en segundos) o puede ser lento, ", agregó. El cuerpo activa sus propias defensas para contrarrestar una sustancia venenosa; sin embargo, normalmente no es suficiente. Cualquier nivel de exposición puede ser mortal. especialmente si el tipo de veneno no es conocido de inmediato por el personal de primera respuesta o el equipo médico que atiende a un paciente afectado.
Un antídoto debe actuar rápido, antes de que el veneno cause un daño irreversible, para ser efectivo y salvar vidas.
Refleja el veneno
Kovalevsky es parte de un equipo dirigido por Zoran Radić de la Universidad de California, San Diego, desarrollar una nueva familia de antídotos para venenos llamados organofosforados, que incluyen agentes nerviosos. La investigación de Radić se enfoca de manera única en la causa raíz del envenenamiento por organofosforados, yendo más allá de tratar los síntomas como con los remedios existentes.
Su atención se centra en los complejos mecanismos bioquímicos que controlan y mantienen el sistema nervioso del cuerpo. Empiezan con acetilcolina, o ACh, que es un compuesto que se encuentra en la unión de músculos y nervios y también en el cerebro. La ACh funciona como un neurotransmisor que mantiene la comunicación normal entre nervios y músculos. Pero ACh no actúa solo.
La enzima llamada acetilcolinesterasa, o AChE, es también donde los músculos y los nervios se encuentran. Su trabajo es proporcionar un control específico de los niveles de compuesto ACh degradándolo, lo que asegura que los nervios funcionen correctamente.
Cuando una persona está expuesta a un agente nervioso, o en grandes cantidades de un insecticida en aerosol, por ejemplo, el veneno pasa rápidamente de los pulmones o la piel al torrente sanguíneo y corre al sistema nervioso. Al llegar a las uniones músculo-nerviosas, el veneno abruma e inhibe el trabajo de la enzima AChE.
Como la enzima AChE está siendo atacada y no puede degradar la ACh, los niveles del compuesto ACh aumentan, interrumpir el equilibrio entre músculos y nervios. Esto causa estragos en el cuerpo.
"En lugar de ser muy poco de algo, hay demasiado de este neurotransmisor. Entonces, los receptores de los nervios están sobreexcitados, y la gente puede entrar en shock, tienen temblores y convulsiones y comienzan a sudar porque sus glándulas están trabajando demasiado, ", Explicó Kovalevsky. Al final, es probable que la persona afectada muera porque dejó de respirar.
Radić dijo que el antídoto debe reflejar la actividad del veneno sin actuar como inhibidor, también.
"Estos venenos, típicamente compuesto por moléculas neutras o sin carga, atraviesan las membranas biológicas muy rápidamente hacia la sangre y luego se distribuyen de la sangre al tejido, incluido el sistema nervioso central. Y todo esto sucede minutos después de la exposición, " él dijo.
"El veneno llega a su objetivo rápidamente, para tratar ese objetivo y recuperar la actividad de la enzima, tenemos que tener un antídoto que haga lo mismo ".
Si se hace bien, el antídoto aliviará la enzima AChE del ataque del veneno, esencialmente extirpando la molécula del veneno unida a la enzima, y permitiéndole comenzar a nivelar los neurotransmisores ACh y finalmente calmar todo el sistema nervioso. El truco consiste en asegurarse de que el antídoto esté diseñado para no quedarse demasiado tiempo o adherirse demasiado a la enzima y convertirse en parte del problema.
Al rescate
En un estudio financiado por el programa CounterACT, Oficina del Director de los Institutos Nacionales de Salud y el Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares y publicado en el Revista de química biológica , El equipo de Radić diseñó y probó medicamentos de acción rápida llamados reactivadores en tres agentes nerviosos diferentes y un pesticida con resultados iniciales positivos.
El equipo comenzó con un compuesto de fármaco existente (nombre de código RS194B), que fue desarrollado por Radić y el profesor Palmer Taylor de UC San Diego unos 15 años antes, porque ya había demostrado ser prometedor viajar a través de la barrera hematoencefálica cuando se probó en primates expuestos a intoxicación por organofosforados.
Sin embargo, los reactivadores de nuevo diseño funcionaron mejor in vitro, o fuera de un organismo vivo, que RS194B, y el equipo de investigación descubrió por qué.
A nivel atómico, RS194B no pudo alcanzar el sitio de actividad del veneno dentro de la molécula de AChE tan eficientemente como los nuevos reactivadores.
Para este estudio, El equipo utilizó análisis cristalográfico de rayos X para observar el complejo RS194B con la enzima AChE sola y luego introdujo un análogo de un agente químico nervioso llamado VX, uno de los productos químicos más mortíferos jamás fabricados. Si bien RS194B no se unió como se esperaba, el experimento fomentó ideas sobre cómo rediseñar "una especie de compuesto de élite, "Dijo Kovalevsky.
"Necesitamos mejorar la capacidad del reactivador para cruzar la barrera hematoencefálica, se unen libremente a la enzima, quitar químicamente el veneno y luego salir rápidamente, "Dijo Kovalevsky." No queremos que se quede después de la reactivación, como hacemos con muchos medicamentos estándar que normalmente inhiben una función enzimática ".
"Ese es nuestro objetivo. Es por eso que diseñar reactivadores es un esfuerzo completamente diferente y muchas reglas del diseño de fármacos convencionales no se aplican, "añadió.
Después de algunos ajustes en el diseño del fármaco, el equipo ideó un nuevo paradigma que puede cambiar por completo la forma en que los investigadores piensan sobre el diseño de un reactivador. Ejecutaron simulaciones por computadora y luego sintetizaron varios compuestos más prometedores de las opciones de diseño alteradas, que proporcionó detalles sobre sus propiedades y pistas sobre cómo podría funcionar cada compuesto.
Analizaron el impacto de cada variación de diseño de fármaco, más el RS194B original, con agentes nerviosos Sarin, Ciclosarina VX y un pesticida Paraoxon. También, el equipo incluyó 2PAM (también llamado pralidoxima), el único antídoto para el envenenamiento por organofosforados aprobado por la Administración Federal de Drogas de los Estados Unidos para su uso en adultos y niños, que sirvió como control para los experimentos.
"Queríamos que nuestros diseños de reactivadores fueran tan buenos como, o mejor que, 2PAM en estos estudios, "dijo Kovalevsky. Sin embargo, 2PAM no puede cruzar la barrera hematoencefálica. Puede viajar a otras áreas del cuerpo afectadas por venenos para actuar sobre el sistema nervioso periférico. pero no se reactiva en el sistema nervioso central.
Según los resultados iniciales del estudio, varias de las variaciones de diseño de fármacos del equipo funcionaron mejor que RS194B y 2PAM, lo que, según Kovalevsky, es un resultado muy alentador para sus novedosas ideas de diseño de reactivadores.
"Una de las distinciones de nuestro antídoto es que pueden atacar diferentes venenos organofosforados de manera más efectiva, porque sus estructuras de reactivación pueden cambiar con su protonación, "Radić dijo." A diferencia de los rayos X, la difracción de neutrones es una técnica experimental que puede informarnos sobre la posición de los protones tanto en el antídoto como en la enzima envenenada ".
Grande, cristales diminutos
Para tener una mejor idea del nuevo diseño del reactivador, el equipo utilizó cristalografía de neutrones en el reactor de isótopos de alto flujo de ORNL, una instalación para usuarios de la Oficina de Ciencias del Departamento de Energía. Kovalevsky opera el instrumento llamado IMAGINE, que utiliza técnicas de difracción de neutrones para observar la estructura de un solo cristal a escala atómica.
La estructura molecular de la proteína es compleja, lo que requiere el crecimiento de cristales individuales grandes, una fuerza de los ORNL, para la difracción de neutrones. Los neutrones son muy sensibles a elementos ligeros como el hidrógeno, y son particularmente adecuados para encontrar átomos de hidrógeno individuales en cristales de proteínas que los rayos X no pueden detectar. Los datos recopilados de IMAGINE, junto con información de un experimento de neutrones realizado en el Institut Laue-Langevin en Francia, confirmó que es posible identificar la ubicación y distribución de cada átomo de hidrógeno en la proteína.
El equipo continuará cultivando cristales más grandes para su análisis, que debería producir conjuntos de datos de mayor resolución e informar los ajustes a los prometedores, diseños de fármacos novedosos. Su investigación continua podría finalmente confirmar una nueva clase de acción rápida, antídotos que salvan vidas para el envenenamiento por organofosforados.