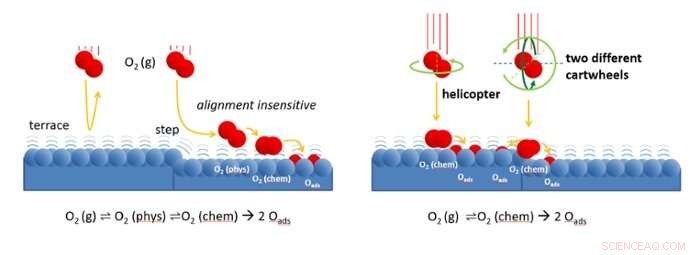
Figura a la izquierda:las moléculas de oxígeno se acercan a la superficie del catalizador a baja velocidad. Los escalones en la superficie dispersan las moléculas en un estado "fisisorbido" débilmente unido. Desde allí, las moléculas pueden encontrar fácilmente su camino hacia un sitio donde se unen químicamente y finalmente se disocian. En las terrazas atómicamente planas, la dispersión de nuevo en la fase gaseosa es mucho más probable. Debido a que el estado fisisorbido está débilmente ligado, se parece mucho a la molécula en fase gaseosa. En ambos, la molécula puede girar. Por tanto, el proceso de dispersión no depende de la alineación inicial de la molécula. Figura derecha:A alta velocidad de incidencia, El O2 se puede adsorber directamente en un estado químicamente unido. En terrazas, moléculas que los helicópteros tienen una mayor probabilidad de unirse que las que se "carthweel". Solo a pasos Las moléculas que hacen volteretas son sensibles a la alineación. Las moléculas que giran a lo largo del borde de los escalones (rotación verde oscuro) se adhieren más fácilmente al borde que las que giran contra el borde (rotación verde claro). Crédito:Universidad de Leiden
El platino es un catalizador ampliamente utilizado, pero su mecanismo preciso sigue siendo en gran parte un misterio para los científicos. Ludo Juurlink ahora ha demostrado por primera vez cómo reacciona el oxígeno en la superficie de platino. Junto con Ph.D. estudiantes Kun Cao y Richard van Lent y colegas internacionales, ha publicado sus hallazgos en PNAS .
A principios de este año, Juurlink resolvió un problema de química de 40 años, junto con Richard van Lent y el instituto DIFFER. Usando una superficie de platino curva única, demostró cómo reacciona el hidrógeno con el platino. En su investigación actual, volvió a utilizar el platino curvo, esta vez investigando la reacción con el oxígeno.
Esto ha llevado a un descubrimiento interesante. Juurlink y sus colegas observaron que el oxígeno reacciona con el platino de una manera diferente que el hidrógeno, mucho más ligero. El platino curvo volvió a ser crucial para este descubrimiento. "Debido a que la superficie de platino es curva, la estructura atómica cambia muy gradualmente a lo largo de la superficie, "explica Juurlink. Esta estructura se puede comparar a una escalera con escalones que se vuelven cada vez más estrechos hacia los bordes. En el medio, la superficie se parece más a un salón de baile ".
La reactividad del hidrógeno resultó depender de qué tan cerca estén los pasos del catalizador entre sí. Este también es el caso del oxígeno, pero por una razón fundamentalmente diferente. "Los pasos tienen un efecto diferente sobre el oxígeno que sobre el hidrógeno".
Según Juurlink, esto tiene que ver principalmente con la mayor masa de oxígeno. "Como el oxígeno es más pesado que el hidrógeno, la interacción con la superficie de platino comienza desde una distancia mayor, ", dice." La molécula de oxígeno ya siente la interacción con el platino, pero aún no puedo ver los detalles. Como resultado, la reacción tiene lugar de forma diferente a la del hidrógeno ".
Para el experimento, era necesario controlar la dirección de rotación de las moléculas de oxígeno. Esto requirió la cooperación de un colega japonés, Mitsunori Kurahashi, que construyó un dispositivo único para este propósito. "El año pasado, Tuve la oportunidad de realizar mediciones en su laboratorio durante dos semanas gracias a una beca del instituto donde trabaja Kurahashi, "dice Juurlink.
"Este es un hermoso descubrimiento fundamental, concluye Juurlink, que también puede tener un impacto en las aplicaciones existentes. La reacción del oxígeno al platino es esencial en el sector de la energía sostenible y para mejorar la calidad del aire. "Por ejemplo, la reacción tiene lugar en las pilas de combustible de hidrógeno y en los sistemas de escape de los automóviles, "dice el químico." El hecho de que ahora podamos medir cómo se desarrolla la reacción a un nivel tan detallado, plantea desafíos a los modelos teóricos que describen esta reacción química y hacen predicciones al respecto ".