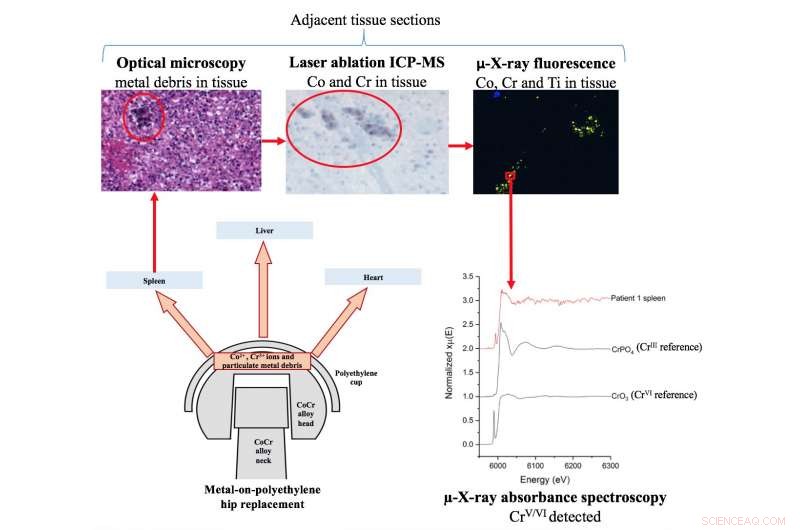
Figura 1:Resumen del estudio. Crédito:Fuente de luz de diamante
El reemplazo de cadera se considera una de las intervenciones ortopédicas más exitosas, con 75, 000 realizados cada año solo por el NHS. Sin embargo, los implantes utilizados para reemplazar las caderas contienen metales, como el cromo y el cobalto, que son potencialmente tóxicos y que pueden depositarse en los tejidos alrededor del lugar del implante debido al desgaste y la corrosión. Un equipo de investigadores utilizó espectroscopia de absorción de rayos X (XAS) en la línea de luz I18 para mostrar que estos metales también pueden encontrar su camino hacia los tejidos de los órganos. Sus resultados sugieren que las enfermedades crónicas, como la diabetes, puede crear condiciones en las que el cromo trivalente levemente tóxico (Cr III ) las partículas de las articulaciones de reemplazo se reoxidan dentro del cuerpo para formar cromo hexavalente cancerígeno (Cr VI ). Sus resultados han sido publicados en el Revista de oligoelementos en medicina y biología .
Metales en movimiento
Las operaciones de reemplazo de cadera tienen más de cien años de historia, con los primeros intentos registrados que tuvieron lugar en Alemania en 1891. El cirujano inglés pionero George McKee fue el primero en utilizar las articulaciones de cadera de metal sobre metal (MOM) de forma regular, en la década de 1950, y Sir John Charnley en Manchester Royal Infirmary fueron pioneros en la técnica moderna de reemplazo de cadera a principios de la década de 1960. Los implantes MOM se volvieron impopulares en la década de 1970 cuando las operaciones de seguimiento encontraron partículas metálicas en los tejidos alrededor del implante. Los implantes de metal sobre polietileno (MOP) son ahora el tipo más utilizado.
Aunque investigaciones anteriores han establecido que las partículas metálicas de la aleación de cobalto-cromo (CoCr) se pueden encontrar en los tejidos que rodean el implante, Se ha trabajado poco sobre los efectos sobre los tejidos sistémicos u orgánicos. Este estudio fue el primero en combinar el uso de micro fluorescencia de rayos X y micro espectroscopia de absorción de rayos X para sondear la distribución y la forma química del cobalto. cromo y titanio en muestras de tejido de órganos de pacientes que habían recibido implantes de cadera MOP.
Potencial tóxico
La aleación de CoCr se utiliza en implantes médicos porque se forma una capa de pasivación rica en óxido de cromo sobre su superficie, protegiendo el metal subyacente de la corrosión. Sin embargo, esta película protectora puede dañarse por el desgaste y la corrosión una vez que el implante está dentro del cuerpo.
El cobalto de los implantes se puede encontrar en dos formas dentro del cuerpo, siendo su estado divalente (CoII) más tóxico que el metálico (Co 0 ) estado. Los niveles elevados de cobalto en la sangre están relacionados con problemas neurológicos, cardiomiopatía e hipotiroidismo.
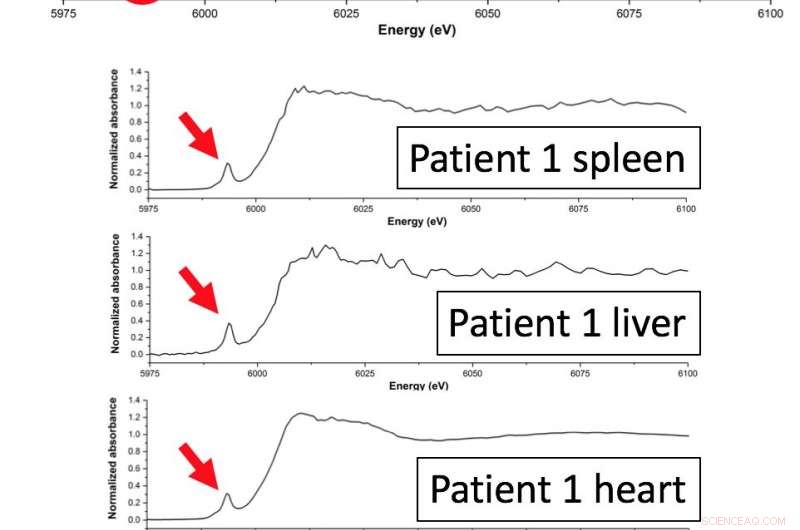
Figura 2:Gráficos de XANES que muestran que se detectó CrV / VI en 4 muestras de tejido separadas de 2 pacientes diferentes. Crédito:Fuente de luz de diamante
El cromo tiene tres estados predominantes:metálico (Cr0), trivalente (Cr III ) y hexavalente (Cr VI ). El cromo trivalente es levemente tóxico, pero los compuestos de cromo hexavalente son fuertemente cancerígenos y causan daño renal.
Un equipo de investigadores utilizó muestras de tejido del hígado, bazo y corazón de cinco pacientes que se habían sometido a una artroplastia de cadera. El trabajo preparatorio guió la elección de las áreas de tejido que se examinarán más a fondo utilizando técnicas de sincrotrón. Utilizaron micro fluorescencia de rayos X para mapear los elementos metálicos, y espectros micro XAS adquiridos en modo de fluorescencia debido a las bajas concentraciones de metales en las muestras. El uso de la parte XANES del espectro permitió a los investigadores determinar los estados metálicos presentes. Las ventajas de utilizar un sincrotrón para este trabajo incluyen la naturaleza no destructiva de las técnicas de rayos X, su sensibilidad y su capacidad para mapear grandes áreas de tejido.
Un posible vínculo con las enfermedades crónicas
Esta fue la primera visita a Diamond de la autora principal, Ilona Swiatkowska. Encontró el apoyo del personal de la línea de luz invaluable, señalando que "el científico Konstantin Ignatyev se quedó hasta la medianoche (¡el fin de semana!) para asegurarse de que pudiéramos obtener los mejores resultados posibles".
Los resultados mostraron la presencia de cromo en tres estados de oxidación diferentes:Cr 0 , Cr III y una especie más oxidada, es decir, Cr V o Cr VI . Este es el primer estudio que reporta una especie de cromo más oxidada que el Cr III en tejido humano. Si bien los investigadores no pudieron determinar con precisión qué estado altamente oxidado estaba presente, la explicación más probable es una mezcla de Cr III y Cr VI óxidos.
Dado que cualquier Cr VI liberado del implante se habría reducido en la sangre antes de llegar a cualquier órgano, Es poco probable que las partículas de Cr altamente oxidadas provengan directamente del implante. Es más probable que Cr III se volvió a oxidar a Cr VI dentro del cuerpo. Las muestras en las que se encontraron estos estados altamente oxidados procedían de dos pacientes con diabetes, y es posible que el aumento de la producción de especies reactivas de oxígeno asociadas con la diabetes (y otras enfermedades crónicas) podría haber fomentado la oxidación de Cr III desde el implante a estados de valencia superiores.
Existe evidencia limitada de un mayor riesgo de cáncer en pacientes que se han sometido a un reemplazo de cadera. Sin embargo, la mayoría de los estudios anteriores adolecen de un tiempo de seguimiento corto, que puede ser insuficiente para detectar cambios malignos. Con más pacientes más jóvenes a los que se recomienda someterse a reemplazos de articulaciones, habrá un número creciente de pacientes expuestos a materiales de implantes durante 30 años o más. Más estudios toxicológicos, incluidos los pacientes con enfermedades crónicas, son necesarios para confirmar estos hallazgos preliminares, y para determinar qué pacientes pueden tener un mayor riesgo de daño tisular y cáncer.