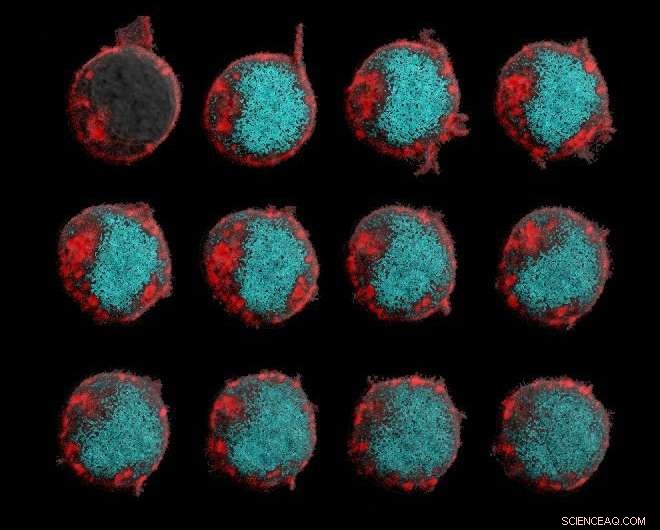
En estas imágenes de lapso de tiempo, Los receptores de antígenos quiméricos responden a una citocina soluble, desencadenando la activación de las células T. Crédito:ZeNan Chang y Michael Lorenzini
Los ingenieros y científicos de UCLA han diseñado un tipo de proteína sintética:un receptor de antígeno quimérico, o COCHE, que responde a objetivos de proteínas solubles. El avance es muy prometedor para ayudar al sistema inmunológico del cuerpo a buscar y destruir el cáncer porque podría aumentar la efectividad de las inmunoterapias contra tumores sólidos que de otra manera serían altamente resistentes a la respuesta inmunológica del cuerpo.
El estudio fue publicado en Biología química de la naturaleza .
"Hemos generado el primer ejemplo de un CAR que puede ayudar a los glóbulos blancos, específicamente a las células T, a convertir las proteínas producidas por tumores a partir de supresores, o 'tranquilizantes' para nuestro sistema inmunológico, en estimulantes que desencadenan fuertes ataques a las células tumorales, "dijo Yvonne Chen, el investigador principal del estudio, y profesor asistente de ingeniería química y biomolecular en la Escuela de Ingeniería Samueli de UCLA. "Esto podría dar lugar a nuevas aplicaciones terapéuticas, particularmente en el tratamiento de tumores sólidos ".
Los tumores sólidos (tumores que crecen como masas en el cuerpo) son difíciles de destruir porque tienen una variedad de defensas, incluida la capacidad de secretar proteínas que inhabilitan el sistema inmunológico. Superar esas defensas ha sido uno de los principales objetivos de la investigación en biología del cáncer. Un método prometedor para hacerlo es la terapia con células T modificadas con CAR. En 2017, la FDA aprobó este tipo de terapias para tratar los cánceres de la sangre, como leucemia o linfoma. Sin embargo, La terapia con células T modificadas con CAR no ha tenido tanto éxito para el tratamiento de tumores sólidos.
El sistema inmunológico busca naturalmente células enfermas o infectadas que puedan dañar el cuerpo. En la superficie de esas células hay proteínas llamadas antígenos. Mientras tanto, Las células T (glóbulos blancos que pueden destruir células anormales) tienen proteínas correspondientes, llamados receptores, que puede reconocer y unirse a antígenos específicos. Cuando se produce esa unión, desencadena una serie de procesos químicos y biofísicos que activan la célula T para neutralizar las células dañinas.
Los tumores sólidos tienen la capacidad de secretar proteínas solubles llamadas citocinas inmunosupresoras, que inactivan las células inmunes, incluidas las células T. Esto crea un microambiente que es altamente hostil a las células inmunes y protege el tumor.
Basado en ese conocimiento, los investigadores plantearon la hipótesis de que podrían superar ese mecanismo de defensa alterando la respuesta de las células T a las citocinas inmunosupresoras. En lugar de cerrar las células T diseñadas reaccionarían a las citocinas montando un ataque sobre las células tumorales.
Los científicos sabían que la señalización de CAR puede desencadenar la activación de las células T y los efectos antitumorales, por lo que los investigadores propusieron diseñar CAR en las células T para señalizar en respuesta a citocinas inmunosupresoras. Sin embargo, Los CAR normalmente responden a los antígenos presentados en la superficie de las células, no a los antígenos que flotan en el medio ambiente.
Los investigadores descubrieron cómo diseñar CAR que pudieran responder no solo a los antígenos unidos a la superficie, sino también a proteínas solubles, incluidas las citocinas inmunosupresoras. Los investigadores colocaron los CAR que desarrollaron en células T, y las células T modificadas se activaron en respuesta a antígenos solubles.
El nuevo enfoque permitió a las células T convertir el propio mecanismo de defensa del cáncer en un arma que podría intensificar el ataque del sistema inmunológico a las células tumorales.
Los investigadores también descubrieron que, para que se active una célula T, dos de los CAR en su superficie deben unirse a una sola proteína soluble. Y demostraron la versatilidad de su enfoque mediante la ingeniería de CAR que respondían a varias proteínas solubles diferentes, incluido el factor de crecimiento transformante beta, o TGF-beta, una potente citocina inmunosupresora. TGF-beta podría ser un objetivo para futuras inmunoterapias para tratar el cáncer.