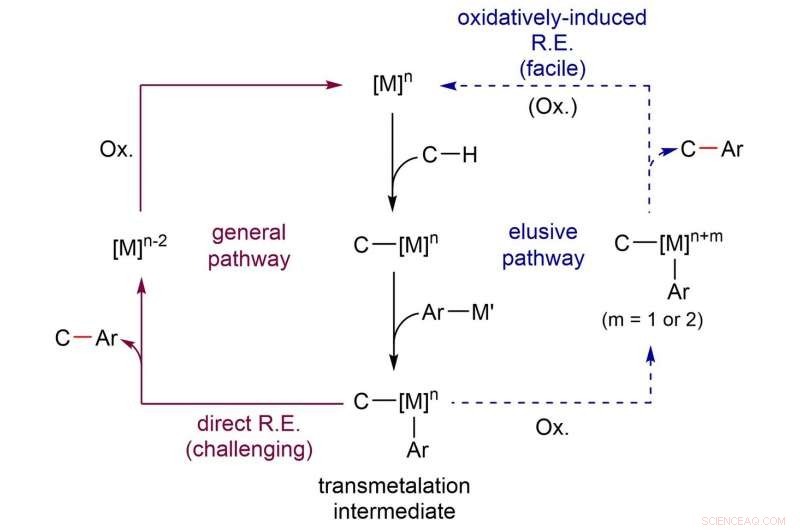
Oxidación del metal (M, iridio vía azul) conduce a una disminución de 19 kcal / mol en la barrera de energía de la reacción, y permite que la arilación se produzca a temperatura ambiente. Crédito:Instituto de Ciencias Básicas
Los enlaces carbono-carbono (C-C) forman el esqueleto de todas las moléculas orgánicas. Sin embargo, La creación artificial de enlaces C-C tan ubicuos sigue siendo una tarea complicada. En particular, dado que varias moléculas utilizadas en medicina, la farmacología y la química de los materiales contienen grupos arilo, idear una manera de introducir de manera eficiente y selectiva este grupo químico es un objetivo importante para los químicos orgánicos. En la actualidad, la mayoría de las reacciones de arilación requieren duras condiciones de reacción, incluyendo altas temperaturas y exceso de aditivos.
Científicos del Centro de Funcionalización Catalítica de Hidrocarburos, dentro del Instituto de Ciencias Básicas (IBS, Corea del Sur), ideó un método para introducir selectivamente grupos arilo en enlaces C-H a temperatura ambiente. Publicado en Química de la naturaleza , el estudio también aclara los detalles de esta reacción, que resultó ser diferente a la idea convencional.
En lenguaje sencillo, el procedimiento consta de tres pasos principales. Primeramente, el catalizador de iridio activa el sustrato que contiene C-H. En segundo lugar, el arilsilano ataca el metal, creando una molécula intermedia. El equipo cristalizó dicho intermedio y demostró que oxidar el centro de iridio del intermedio (tercer paso) es beneficioso para lograr una reacción de arilación de baja energía.
El mecanismo de reacción propuesto se verificó con resonancia electroparamagnética, voltametría cíclica y simulaciones por ordenador. "Desarrollar un sistema de oxidación más eficiente y respetuoso con el medio ambiente es nuestro próximo objetivo, "concluye Kwangmin Shin, primer autor del estudio.
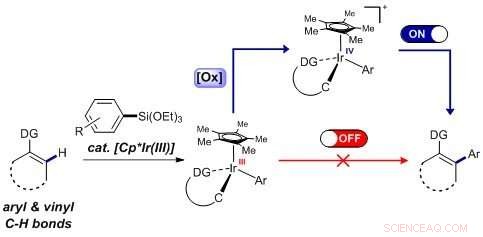
Mecanismo de arilación propuesto por investigadores del SII. La reacción procede a través de una nueva ruta en la que la eliminación reductora tiene lugar más fácilmente después de que el intermedio se oxida selectivamente. Crédito:Instituto de Ciencias Básicas
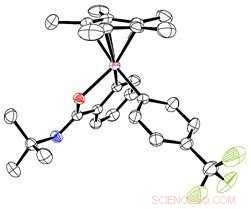
Los científicos del IBS pudieron aislar y cristalizar el intermedio de reacción. Crédito:Instituto de Ciencias Básicas