
Crédito:comunes de Wikipedia
Uno de los mayores desafíos de la biología actual es explicar la estructura de las crestas, las membranas internas de las mitocondrias. Una explicación en este caso es un conjunto de principios para predecir qué forma tomarán las crestas después de las manipulaciones metabólicas básicas del entorno en el que se encuentran las mitocondrias. Por lo tanto, estos principios serán una descripción de la verdadera función de las mitocondrias, algo que hasta ahora solo ha apenas se ha imaginado.
Los avances recientes en técnicas como la microscopía de luz de superresolución de células vivas y la tomografía electrónica han brindado una nueva visión del comportamiento dinámico de las crestas. Ahora se puede construir una arquitectura detallada de todo el volumen mitocondrial a partir de una serie de imágenes inclinadas que se retroproyectan para crear tomogramas 3D. El lunes, discutimos cómo las crestas se transforman y reconfiguran de acuerdo con la abundancia y la salud de varias proteínas de la matriz y la membrana interna. El pretexto para ese análisis fueron las similitudes estructurales y bioquímicas entre las membranas de las mitocondrias, los tilacoides y la mielina que supuestamente ayudan a canalizar los metabolitos en la producción de energía.
En un artículo reciente de Open Biology de The Royal Society , los investigadores explican la biogénesis de las crestas a través de las actividades coordinadas de cuatro vías principales que se conservan evolutivamente desde protistas y levaduras hasta eucariotas superiores como nosotros:formación de dímeros y oligomerización de la ATP sintasa en los bordes de las crestas, ensamblaje del 'sitio de contacto mitocondrial y el sistema organizador de crestas' (MICOS) en las uniones de las crestas, la remodelación de la membrana por una GTPasa relacionada con la dinamina asociada a la membrana interna (Mgm1 en levadura y OPA1 en mamíferos) y el ajuste adecuado de la composición lipídica de la membrana.
Para la primera vía que involucra a la ATP-sintasa, varias cosas son evidentes. Como informamos anteriormente, la dimerización espontánea de la ATP-sintasa en ángulos definidos con precisión y dependientes de la especie en filas ordenadas dicta la geometría de la planta baja. A diferencia de los complejos respiratorios I-IV, que se ensamblan en la membrana límite interna plana, la ATP-sintasa (complejo V) se ensambla completamente en lo profundo de las membranas de las crestas. Si bien varias proteínas de la subunidad ATP-sintasa son prescindibles para la formación adecuada de las crestas, las subunidades Atp20 y Atp21 son estrictamente necesarias.
Un exceso de ADP induce una conformación condensada con grandes espacios intracristalinos hinchados. Por el contrario, bajo condiciones limitantes de ADP, las mitocondrias adoptan la conformación ortodoxa con espacio intracristalino contraído. En la ameba gigante Chaos carolinensis, las mitocondrias normalmente contienen crestas tubulares orientadas al azar. Con la inanición, las crestas agrandadas adoptan una morfología cúbica con un patrón en zigzag. En ratones, los agentes apoptóticos provocan la fusión de crestas individuales con la posterior liberación de citocromo c desde el espacio intracristalino hacia la región límite.
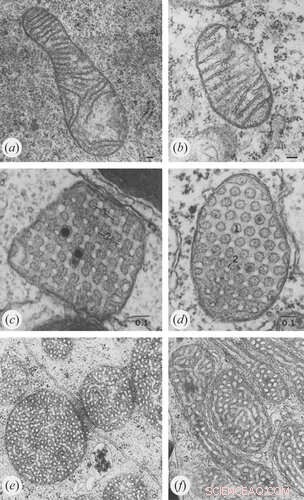
Crédito:Klecker y Westermann, Biología abierta (2021). DOI:10.1098/rsob.210238
Para la segunda vía, el ensamblaje de los sitios de contacto MICOS, la investigación ha determinado que las proteínas críticas, como las de la familia de genes relacionados con MIC60, están presentes desde los ancestros endosimbióticos de las mitocondrias, las α-proteobacterias. Muchos de estos antepasados mitocondriales anteriores ya muestran estructuras de membrana intracitoplasmática diferenciadas. Invariablemente, las especies que han simplificado sus mitocondrias hasta el punto de que las crestas están ausentes carecen correspondientemente de los genes relacionados con MICOS. La reexpresión de homólogos de MIC60 en mutantes de levadura Δmic60 rescata los defectos mitocondriales ultraestructurales.
La tercera vía incluye las GTPasas relacionadas con la dinamina, que coordinan la fusión y la fisión de las membranas interna y externa. En la fisión, estas proteínas se polimeizan en anillos contráctiles que aplican fuerzas constrictivas para apretar las mitocondrias. Ahora se entiende que el resultado depende de las interacciones de estas proteínas, tanto con el complejo MICOS como con las uniones de las crestas, y también con los sistemas de transporte de la membrana interna y externa que se congregan allí. Estos incluyen los complejos translocadores de membrana TIM y TOM.
La cuarta vía comprende los propios fosfolípidos de la membrana mitocondrial. Las mitocondrias albergan la ruta biosintética de cardiolipina y también están involucradas en la síntesis de fosfatidiletanolamina. Junto con la fosfatidilcolina, estos son los tres principales fosfolípidos con los que trabajan las mitocondrias. La mayoría de los componentes básicos de los lípidos mitocondriales se sintetizan en el RE y, por lo tanto, deben importarse mediante mecanismos que implican una aposición cercana al RE. Una vez dentro de la membrana externa, la distribución de lípidos está mediada por proteínas de transporte localizadas en el espacio intermembrana de la familia Ups/PRELI,
Las mitocondrias no crean geometría desde cero, sino que aprovechan y se basan en las formas físicas naturales que ocurren espontáneamente en los lípidos. Si se los deja a su suerte, los lípidos forman estructuras lamelares concéntricas que luego pueden expandirse y aumentarse mediante proteínas específicas. Las mediciones a escala fina ahora han revelado que las crestas individuales son funcionalmente independientes y pueden tener potenciales de membrana significativamente diferentes.
Cristae formation involves a tightly connected interplay of the above four shaping influences. For example, the activities of the MICOS complex and ATP synthase dimerization are both cooperative and antagonistic. MICOS induces negative membrane curvature while the ATP synthase induces positive curvature at cristae tips and rims. New computational models, as currently under development in labs throughout the world, where ratios of these different components can be finely tweaked and adjusted, will greatly aid in defining what controls the form of mitochondria.