
Sooyeon Hwang (sentada), Dong Su (izquierda, de pie, y Shuang Li en el Centro de Nanomateriales Funcionales de Brookhaven Lab, donde utilizaron microscopios electrónicos para ver cómo la estructura cristalina y la naturaleza química de un electrodo de batería hecho de un material de óxido de hierro llamado magnetita evolucionó a medida que se insertaba y extraía litio durante 100 ciclos de carga y descarga. Crédito:Laboratorio Nacional Brookhaven
Debido a su alta densidad de almacenamiento de energía, materiales como óxidos metálicos, sulfuros y los fluoruros son materiales de electrodos prometedores para baterías de iones de litio en vehículos eléctricos y otras tecnologías. Sin embargo, su capacidad se desvanece muy rápidamente. Ahora, Los científicos que estudian un electrodo hecho de un material de óxido de hierro barato y no tóxico llamado magnetita han propuesto un escenario, descrito en la edición en línea del 20 de mayo de Comunicaciones de la naturaleza —Eso explica por qué.
"Magnetita, entre otros materiales de electrodo de tipo conversión (es decir, materiales que se convierten en productos completamente nuevos cuando reaccionan con el litio), pueden almacenar más energía que los materiales de electrodos actuales porque pueden acomodar más iones de litio, "dijo el líder del estudio Dong Su, líder del Grupo de Microscopía Electrónica en el Centro de Nanomateriales Funcionales (CFN), una instalación para usuarios de la Oficina de Ciencias del Departamento de Energía de EE. UU. en el Laboratorio Nacional de Brookhaven. "Sin embargo, la capacidad de estos materiales se degrada muy rápidamente y depende de la densidad de corriente. Por ejemplo, Nuestras pruebas electroquímicas de magnetita revelaron que su capacidad cae muy rápidamente dentro de los primeros 10 ciclos de carga y descarga de alta velocidad ".
Para saber qué hay detrás de esta mala estabilidad en bicicleta, los científicos caracterizaron cómo la estructura cristalina y la naturaleza química de la magnetita evolucionaron cuando la batería completó 100 ciclos. Para estos estudios de caracterización, combinaron microscopía electrónica de transmisión (TEM) en CFN y espectroscopía de absorción de rayos X sincrotrón (XAS) en Advanced Photon Source (APS), una instalación para usuarios de la Oficina de Ciencias del DOE en Argonne National Lab. En TEM, se transmite un haz de electrones a través de una muestra para producir una imagen o un patrón de difracción característico de la estructura del material; En su lugar, XAS utiliza un haz de rayos X para sondear la química del material.
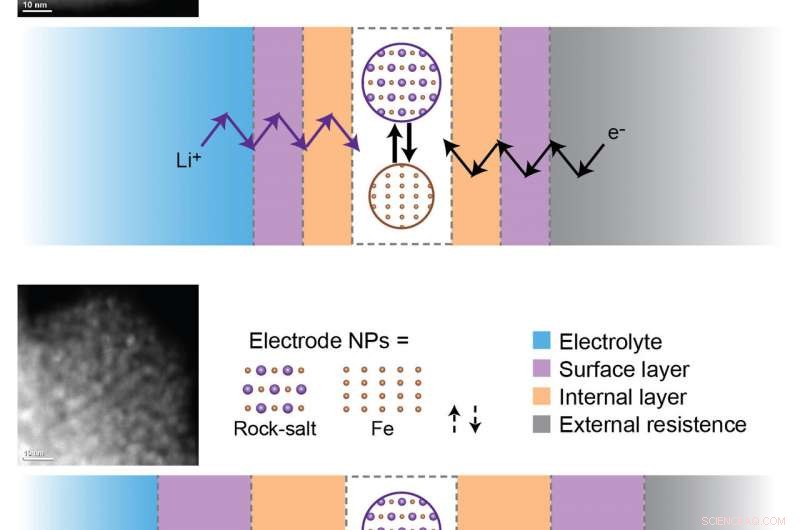
El desvanecimiento de la capacidad de la batería se debe a la formación y engrosamiento de las capas de pasivación internas y superficiales durante los ciclos de carga y descarga. Para que ocurran las reacciones electroquímicas, Los iones de litio (Li +) y los electrones (e-) deben viajar a través de todas estas capas para alcanzar las nanopartículas activas (NP) en el electrodo. Arriba:Muestra de Fe3O4 (óxido de hierro) después de tres ciclos. Abajo:muestra de Fe3O4 después de 100 ciclos. El desarrollo de barreras cinéticas durante los ciclos prolongados limita las reacciones electroquímicas hasta tal punto que no se producen reacciones de reducción-oxidación en los materiales de los electrodos después de 100 ciclos. Crédito:Laboratorio Nacional Brookhaven
Usando estas técnicas, los científicos descubrieron que la magnetita se descompone completamente en nanopartículas de hierro metálico y óxido de litio durante la primera descarga. En el siguiente cargo, esta reacción de conversión no es completamente reversible:quedan residuos de hierro metálico y óxido de litio. Es más, la estructura original de "espinela" de la magnetita evoluciona hacia una estructura de "sal de roca" (la ubicación de los átomos de hierro no es del todo idéntica en las dos estructuras) en el estado cargado. Con ciclos posteriores de carga y descarga, El óxido de hierro de sal de roca interactúa con el litio para formar un compuesto de óxido de litio y nanopartículas de hierro metálico. Debido a que la reacción de conversión no es completamente reversible, estos productos residuales se acumulan. Los científicos también encontraron que el electrolito (el medio químico que permite que los iones de litio fluyan entre los dos electrodos) se descompone en ciclos posteriores.
"Nuestros estudios TEM en tiempo real en vacío ultra alto nos permitieron ver cómo cambia la estructura del óxido de hierro salino a medida que se introduce litio después de los ciclos iniciales, ", dijo Su." Este estudio representa de manera única la litiación in situ de una muestra preciclada. Los estudios in situ previos solo consideraron los ciclos iniciales de carga y descarga. Sin embargo, necesitamos saber qué sucede durante muchos ciclos para diseñar baterías de mayor duración porque la estructura en el electrodo cargado es diferente a la del estado prístino ".
Sobre la base de sus resultados, los científicos propusieron una explicación para el desvanecimiento de la capacidad.
"Dado que el óxido de litio tiene una conductividad electrónica baja, su acumulación crea una barrera para los electrones que van y vienen entre el electrodo positivo y negativo de la batería, "explicó el coautor principal, Sooyeon Hwang, un científico de planta en el Grupo de Microscopía Electrónica CFN. "Llamamos a esta barrera una capa de pasivación interna. De manera similar, La descomposición electrolítica dificulta la conducción iónica al formar una capa de pasivación superficial. Esta acumulación de obstáculos impide que los electrones y los iones de litio alcancen los materiales de los electrodos activos, donde ocurren las reacciones electroquímicas ".
Los científicos observaron que el funcionamiento de la batería a baja corriente puede recuperar parte de esta capacidad al reducir la velocidad de carga para proporcionar suficiente tiempo para el transporte de electrones; sin embargo, se necesitan otras soluciones para solucionar el problema en última instancia. Creen que agregar otros elementos al material del electrodo y cambiar el electrolito podría mejorar la capacidad de desvanecimiento.
"El conocimiento que obtuvimos generalmente se puede aplicar a otros compuestos de conversión, que también enfrentan el mismo problema con las capas de pasivación internas y externas, "dijo el coautor correspondiente Zhongwei Chen, profesor de la Universidad de Waterloo, Canadá. "Esperamos que este estudio pueda ayudar a guiar futuras investigaciones fundamentales sobre estos prometedores materiales de electrodos de tipo conversión".