Existe una lucha constante para reducir las fuentes de energía basadas en carbono y reemplazarlas con alternativas bajas o nulas. El proceso de dividir el agua podría ser la solución.
La producción de hidrógeno es un método simple, seguro y eficaz para producir más energía que la gasolina mediante el simple proceso de dividir el agua. Cosechar energía de esta manera, en lugar de depender en gran medida (o en absoluto) de fuentes de energía basadas en carbono, se está convirtiendo cada vez más en el estándar. Los investigadores han encontrado un método para utilizar sulfuros de metales de transición, como estaño (Sn), cobalto (Co) y hierro (Fe) sobre espuma de níquel, para desarrollar electrocatalizadores de metales no preciosos para su uso en la división del agua de forma rentable y ambientalmente responsable.
Los investigadores han publicado sus resultados en Nano Research Energy .
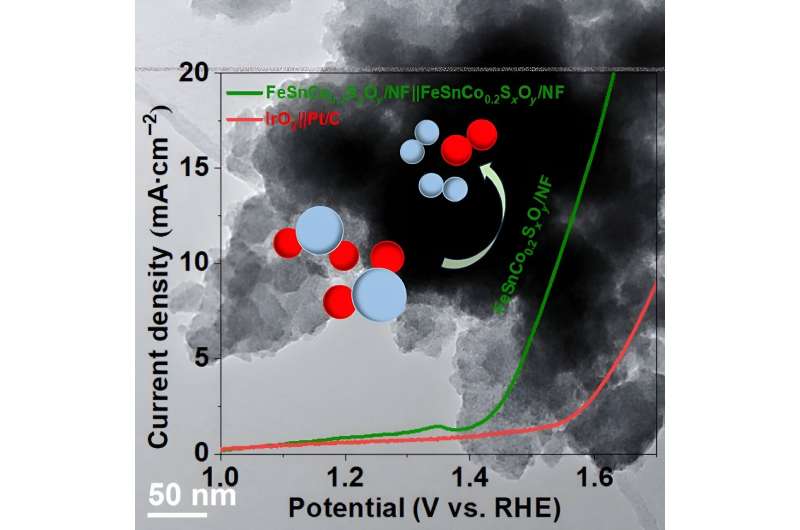
Para tener éxito en esta empresa de reducción de carbono, es necesario estabilizar algunas reacciones para este proceso. La estrella del estudio es el FeSnCo0,2 Sexox Oy /NF, que puede actuar como ánodo y cátodo en el proceso de división del agua a bajo voltaje.
Las dos reacciones que nos preocupan aquí son las reacciones de evolución de oxígeno (OER) y las reacciones de evolución de hidrógeno (HER). REA genera O2 mediante una reacción química del agua. ELLA produce H2 de una reacción de transferencia de dos electrones. El H2 resultante es útil como combustible. Usar ambas reacciones es ideal para crear un electrocatalizador bifuncional. Los electrocatalizadores se pueden definir como catalizadores (o iniciadores de reacciones) que funcionan en las superficies de los electrodos, que son superficies que pueden transportar una corriente eléctrica.
HER ha demostrado ser estable tras 55 horas de uso continuo y también requiere un sobrepotencial menor que el REA. El sobrepotencial es la diferencia en la cantidad de energía necesaria para que funcione un determinado catalizador.
Desafortunadamente, la estabilidad de los REA no está donde necesita estar. Esto se debe en parte al paso adicional involucrado en la transferencia de electrones, pero también a que los electrolitos con los que funcionan suelen ser duros. Si bien los REA se mantienen estables con un uso continuo de alrededor de 70 horas, su actividad disminuye con más contenido de cobalto.
"Es fundamental mejorar la estabilidad REA de los sulfuros de metales de transición para que puedan usarse como catalizadores HER y REA bifuncionales para pilas de combustible de hidrógeno reversibles", afirmó Jingqi Guan, autor e investigador del estudio.
OER también tiene un sobrepotencial mayor que HER. Con una mayor cantidad de energía necesaria para inducir la operación del catalizador, los REA pueden ser más "difíciles". Sin embargo, la combinación de hierro, estaño y cobalto sobre espuma de níquel ofrece cierta mejora en la estabilidad bifuncional y en la actividad HER y OER.
La combinación de estos metales y las interfaces heteroestructurales formadas pueden ajustar la distribución de los electrones a través de la superficie del electrolito. "Heteroestructural" aquí se refiere a un semiconductor que puede tener una composición química alterada según la posición en la que se encuentran los dos químicos. En este caso, es un dúo de sulfuro/oxihidróxido.
La distribución uniforme de los electrones ayuda a aumentar la tasa de transferencia de carga en toda la estructura, lo que luego promueve la transferencia de electrones. Debido a la naturaleza de este semiconductor, aumentar la estabilidad naturalmente mejoraría la actividad y función generales.
En general, estos metales de transición tienen un efecto sinérgico entre sí, especialmente cuando se someten a HER. Este efecto los convierte en candidatos ideales para el principal desafío propuesto por los investigadores:reducir las fuentes de energía basadas en carbono.
Aunque los resultados fueron muy prometedores, siempre se pueden dar pasos en el futuro para perfeccionar un proceso. Encontrar un catalizador que minimice los sobrepotenciales puede reducir el aporte de energía necesario para catalizar la reacción. Además, garantizar que los electrocatalizadores desarrollados sean lo suficientemente duraderos para ser utilizados comercialmente y puedan soportar largas horas de uso continuo sin efectos nocivos es imperativo para el éxito a largo plazo de las interfaces heteroestructurales.
Más información: Siyu Chen et al, Ingeniería de interfaz de electrocatalizador heteroestructural de sulfuro/oxihidróxido de Fe-Sn-Co para la división sinérgica del agua, Nano Research Energy (2023). DOI:10.26599/NRE.2023.9120106
Proporcionado por Tsinghua University Press