Se cree que el envejecimiento de la población y la tendencia a llevar un estilo de vida más sedentario en muchas partes del mundo aumentan drásticamente el número de personas que viven con múltiples enfermedades crónicas. Además, el cambio climático, así como los patrones cambiantes en el uso de la tierra y los viajes, siguen aumentando el riesgo de enfermedades infecciosas que pueden surgir y propagarse a nivel local y global.
Ser capaz de diagnosticar rápidamente la presencia y la evolución de todas estas enfermedades plantea un desafío cada vez mayor para los sistemas de atención médica, desafío que sólo puede resolverse con la ayuda de pruebas diagnósticas efectivas en el lugar de atención (POC, por sus siglas en inglés) más allá del consultorio del médico y sistemas médicos avanzados. instalaciones.
Las pruebas POC aportaron numerosos beneficios a las personas durante la pandemia de COVID-19, pero este enfoque debe aplicarse de manera mucho más amplia y permitir a los médicos y pacientes investigar más profundamente las condiciones patológicas. Las tecnologías de diagnóstico POC actuales solo miden un único biomarcador de enfermedad o, a veces, varios biomarcadores que pertenecen a la misma clase de moléculas, como diferentes ARN, proteínas o anticuerpos.
Sin embargo, medir múltiples biomarcadores de diferentes clases moleculares podría informar de manera más completa sobre el estado en que se encuentra una enfermedad, su gravedad y progresión en el tiempo, e incluso tener en cuenta las diferencias de persona a persona en cómo se desarrolla.
Los biosensores electroquímicos, que convierten una señal química en forma de un biomarcador presente en una pequeña muestra de biofluido, como sangre, saliva u orina, en una señal eléctrica que corresponde en intensidad a la cantidad detectada del biomarcador, podrían proporcionar la respuesta a muchos problemas de diagnóstico POC.
En principio, se pueden combinar múltiples sensores para diferentes moléculas de biomarcadores en conjuntos de sensores multiplexados y, lo que es más importante, la lucha contra el "biofouling", la antes inevitable destrucción de las superficies de los electrodos por moléculas biológicas inespecíficas contenidas en las muestras, se ha vuelto evitable gracias a la ingeniería de revestimientos antiincrustantes finos desarrollados por primera vez en el Instituto Wyss de la Universidad de Harvard.
Ahora, el equipo de investigación del Instituto Wyss, junto con varios institutos colaboradores en Corea, ha avanzado un paso crítico en la detección de diagnóstico electroquímico hacia su aplicación más amplia mediante el desarrollo de un nuevo recubrimiento antiincrustante poroso nanocompuesto que, con un espesor de un micrómetro (el diámetro de una bacteria, que es aproximadamente 100 veces más gruesa que los recubrimientos anteriores.
El mayor espesor del recubrimiento y una red porosa diseñada dentro de él permitieron la incorporación de un número mucho mayor de sondas de detección de biomarcadores en los sensores y, por lo tanto, sensibilidades hasta 17 veces mayores que los mejores sensores anteriores, al mismo tiempo que proporcionaban capacidades antiincrustantes superiores. .
En su estudio de prueba de concepto, los investigadores han construido sensores que combinan la capacidad de detectar objetivos de biomarcadores de ácido nucleico, antígeno y anticuerpo del huésped específicos de COVID-19 en muestras clínicas con alta sensibilidad y especificidad. Sus hallazgos se publican en Nature Communications. .
"Nuestro novedoso recubrimiento de emulsión porosa y espesa aborda directamente los obstáculos críticos que actualmente impiden el uso generalizado de sensores electroquímicos como componentes centrales de diagnósticos POC integrales para muchas afecciones", dijo el último autor y director fundador de Wyss, Donald Ingber, M.D., Ph.D. .
"Sin embargo, ir mucho más allá de eso, también podría abrir nuevas oportunidades para desarrollar dispositivos implantables más seguros y funcionales y otros sistemas de monitoreo de atención médica en múltiples frentes de enfermedades. Superar los problemas de bioincrustación y sensibilidad son desafíos que impactan muchos de estos esfuerzos". /P>
Ingber también es profesor Judah Folkman de biología vascular en la Facultad de Medicina de Harvard y el Hospital Infantil de Boston y profesor Hansjörg Wyss de ingeniería bioinspirada en la Escuela de Ingeniería y Ciencias Aplicadas John A. Paulson de Harvard.
En 2019, el proyecto de sensores electroquímicos del Instituto Wyss publicó su primer artículo histórico que informó sobre el primer recubrimiento antiincrustante con capacidades de biodetección sin precedentes.
En una serie de estudios de seguimiento críticos, el equipo aumentó el potencial de la detección electroquímica al avanzar aún más en la nanoquímica de los recubrimientos para hacer que los electrodos sean aún más sensibles a los biomarcadores, agregar importantes capacidades de multiplexación y desarrollar métodos de fabricación que reducen los costos.
Los biosensores más avanzados que el equipo diseñó en la plataforma eRapid de Wyss tenían un conjunto de características que ya están permitiendo su traducción a algunos entornos clínicos.
Sin embargo, el método de recubrimiento que utilizó el equipo expuso todo el chip del sensor a la solución de nanocompuesto y solo permitió que se formara un recubrimiento relativamente delgado de alrededor de 10 nanómetros en toda la superficie del sensor, lo que limitó la funcionalidad de los sensores de varias maneras.
Por ejemplo, el diámetro delgado del recubrimiento restringió la cantidad máxima de sonda que se podía cargar en él, lo que se vuelve especialmente crítico en sensores multiplexados más grandes que aún necesitan trabajar con volúmenes de muestra pequeños y aún más en los esfuerzos por miniaturizar sensores multiplexados para su uso. en dispositivos de diagnóstico POC portátiles.
"En este nuevo estudio, se nos ocurrió una solución completamente nueva para este problema que resultó en un recubrimiento 100 veces más grueso. Nuestro nuevo enfoque aprovecha un método de impresión por chorro de tinta que nos permite aplicar este recubrimiento grueso de manera muy local a sensores individuales. elementos", dijo el ex científico principal de Wyss, Pawan Jolly, Ph.D., quien jugó un papel decisivo en la evolución de la plataforma eRapid.
"Esto abre nuevas posibilidades:en primer lugar, podemos incluir cantidades mucho mayores de sondas de detección de biomarcadores en el recubrimiento y, en el futuro, los sensores en matrices complejas pueden abordarse individualmente aplicándoles nanocompuestos químicos que están específicamente orientados hacia objetivos específicos. modalidades de biomarcadores."
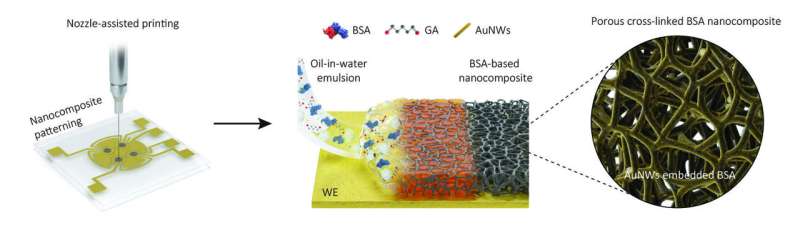
En lugar de sumergir literalmente los electrodos electroquímicos en una solución de recubrimiento, como lo hicieron con su generación anterior de sensores, los investigadores imprimieron una capa de una emulsión densa de aceite en agua a través de una boquilla fina sobre los electrodos. Después de evaporar las pequeñas burbujas de aceite, quedó una capa de 1 micrómetro de espesor en la superficie del electrodo que consistía en moléculas poliméricas reticuladas de la proteína sanguínea albúmina y contenía poros interconectados y nanocables de oro conductores de electrones.
"La red porosa en este recubrimiento nanocompuesto aumenta dramáticamente la superficie que se puede usar para conectar sondas de detección de biomarcadores diseñadas específicamente y que al mismo tiempo es accesible para muestras de fluidos. Como resultado, la sensibilidad de detección aumenta significativamente". explicó el primer autor Jeong-Chan Lee, Ph.D., becario postdoctoral del equipo de Ingber.
"Además, la impresión con boquilla nos permite diseñar la emulsión exclusivamente en el electrodo de trabajo de detección de biomarcadores, manteniendo libre de ella el electrodo de referencia vecino contenido en cada sensor, lo que reduce el ruido eléctrico no específico y mejora la especificidad de nuestras mediciones".
El equipo reutilizó una combinación previamente desarrollada de reactivos de detección para tres biomarcadores relacionados con COVID-19 para modelar una matriz de electrodos sensores utilizando su tecnología de recubrimiento recientemente desarrollada:un sensor habilitado para CRISPR para un ARN del SARS-CoV-2, un sensor específico para un antígeno de la cápside del SARS-CoV-2 y un sensor para un anticuerpo del huésped dirigido al virus.
Probado con una colección de muestras de pacientes, el nuevo sensor produjo sensibilidades de detección mejoradas entre 3,75 y 17 veces en comparación con uno anterior fabricado con los mismos sistemas de detección y el mejor recubrimiento no poroso y mucho más delgado del equipo. También distinguía muestras positivas de negativas con un 100 % de precisión (especificidad).
"Los sensores electroquímicos con este recubrimiento de próxima generación serían ideales para monitorear brotes virales, respuestas a la vacunación y comprender las correlaciones entre varios biomarcadores en el curso de las infecciones virales y, en el futuro, también podrían usarse para otras enfermedades". dijo Lee.
Más información: Jeong-Chan Lee et al, Recubrimiento nanocompuesto poroso y de espesor micrométrico para sensores electroquímicos con excepcionales propiedades antiincrustantes y electroconductoras, Nature Communications (2024). DOI:10.1038/s41467-024-44822-1
Información de la revista: Comunicaciones sobre la naturaleza
Proporcionado por la Universidad de Harvard