
Una imagen de microscopio de barrido en color falso de una matriz de transistores 10-FET. Rojo:elastómero de silicona; Verde:IP; Azul claro:SU8; Oro amarillo; Gris:Silicona. Crédito:Gu et al.
Las células animales pueden utilizar elementos o iones para generar impulsos eléctricos. Estos impulsos luego se transmiten de una célula a otra, viajando a través de redes celulares.
La capacidad de registrar con precisión las señales eléctricas intercambiadas por las células podría ayudar a la investigación y mejorar las prácticas en numerosos campos relacionados con la salud, incluidas la cardiología y la neurología. Sin embargo, la mayoría de las tecnologías existentes están limitadas tanto en su precisión de detección como en su escalabilidad.
Investigadores de la Universidad de California en San Diego desarrollaron recientemente un dispositivo de detección altamente sensible que podría usarse para registrar las señales eléctricas de las células con mayor precisión. Este dispositivo, presentado en un artículo publicado en Nature Nanotechnology , se compone de múltiples sensores, que pueden medir colectivamente la propagación de señales eléctricas intercambiadas por diferentes celdas o dentro de celdas individuales.
El estudio reciente fue dirigido por el Dr. Yue Gu mientras trabajaba en el laboratorio del Prof. Sheng Xu en UC San Diego. Dr. Gu, ahora es asociado postdoctoral en la Universidad de Yale.
"El establecimiento de nuestra estructura 3D, también conocida como arquitectura 'pop-up', se basa en un método único, la técnica de pandeo por compresión que desarrollé durante mis estudios postdoctorales en 2015", dijo el Prof. Xu, uno de los autores de el artículo reciente, dijo a Phys.org. "La técnica de pandeo por compresión aprovecha las técnicas de microfabricación convencionales y versátiles en salas limpias para generar estructuras 3D sofisticadas".
Las estructuras emergentes en 3D utilizadas por el profesor Xu y sus colegas se pueden construir utilizando una amplia gama de materiales que son compatibles con las técnicas de microfabricación. Los materiales de los que están hechos pueden, a su vez, determinar su función, que podría ser la atenuación de ondas electromagnéticas, la vibración mecánica, la detección de presión y tensión, o la detección de señales eléctricas.

Fotografía de una matriz de transistores 128-FET. Crédito:Gu et al.
En su estudio, los investigadores se propusieron construir estas estructuras 3D para que pudieran usarse para registrar con precisión las señales eléctricas generadas e intercambiadas por las células. Su objetivo clave era aprovechar de forma eficaz la versatilidad de la técnica de pandeo por compresión para construir un dispositivo que recogiera registros intracelulares e intercelulares precisos.
"La incorporación de materiales semiconductores y transistores de ingeniería en esta arquitectura emergente amplía la aplicación de la técnica", explicó el profesor Xu. "Nuestra determinación de aplicar esta estructura a las células, específicamente a las células del músculo cardíaco, fue provocada por conversaciones que el Dr. Gu y yo tuvimos con cardiólogos y neurólogos en 2015, quienes se quejaban de las dificultades para registrar señales intracelulares utilizando las herramientas existentes, como como la abrazadera de parche, que es el estándar de oro para registrar señales eléctricas celulares".
Después de enterarse de los desafíos que enfrentaban los investigadores médicos al tratar de recopilar registros precisos de señales eléctricas celulares, el Dr. Xu y el Dr. Gu comenzaron a experimentar con enfoques de ingeniería únicos que podrían simplificar su trabajo. En última instancia, esto condujo al desarrollo de la nueva matriz de sensores presentada en su artículo reciente.
"Otro objetivo de nuestro estudio fue la implementación de sensores intracelulares en tejidos cardíacos diseñados en 3D", dijo el profesor Xu. "Es bien sabido que las propiedades electrofisiológicas de las células varían cuando se encuentran en animales vivos, aisladas de los animales vivos y cultivadas en placas. El registro de las señales in vivo es siempre el paso más significativo y desafiante".
El Prof. Xu y sus colegas fueron los primeros en recopilar registros intracelulares precisos de células dentro del tejido cardíaco diseñado. Por lo tanto, su estudio podría ser un primer paso hacia la recopilación de grabaciones celulares in vivo confiables.
"El potencial de la membrana celular que sesga la terminal de puerta de los transistores individuales da como resultado un cambio en la corriente desde el drenaje hasta la terminal fuente de los transistores", explicó el profesor Xu. "Por lo tanto, las fluctuaciones actuales reflejan los potenciales de membrana momentáneos. Los múltiples transistores en la matriz que desarrollamos pueden registrar simultáneamente señales desde diferentes posiciones de una celda o celdas diferentes".
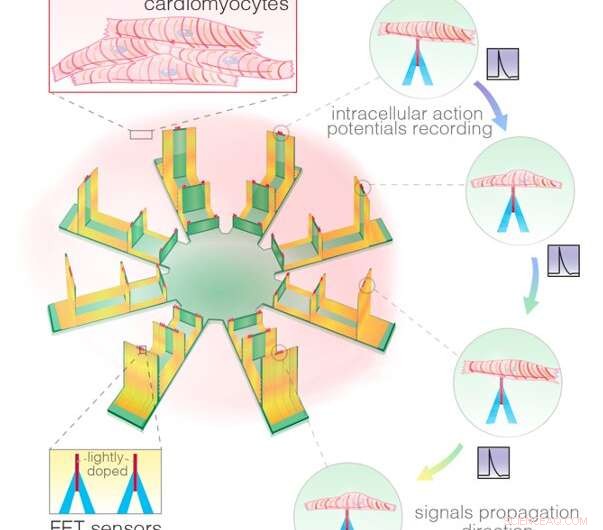
Una imagen esquemática muestra la detección intracelular mediante una matriz de transistores 128-FET y la grabación de las propagaciones de la señal entre las células. Crédito:Gu et al.
Para monitorear los comportamientos de propagación de la señal dentro y entre las células, el dispositivo de los investigadores secuencia las señales captadas por sus muchos transistores. A diferencia de otros métodos propuestos anteriormente para recolectar grabaciones celulares, el nuevo dispositivo es capaz de monitorear múltiples células simultáneamente. Además, sus transistores pueden conservar intactos los potenciales de membrana celular de amplitud completa, sin sufrir atenuaciones o impedancias asociadas con el proceso a través del cual accede a las células.
"Las superficies de transistor funcionalizadas por materiales de bicapa de fosfolípidos también pueden camuflar los transistores inorgánicos para que sean células, lo que facilita en gran medida su inserción en el cuerpo celular", explicó el profesor Xu. "En tales condiciones, la internalización se describe como un proceso de fusión espontáneo, que deja mínima o incluso nula invasividad a la célula".
El dispositivo de detección desarrollado por el profesor Xu y sus colegas también puede monitorear la velocidad de conducción de la señal eléctrica dentro de un cardiomiocito. Esta medida puede ser de vital importancia para el trabajo de los cardiólogos, ya que compararla con la velocidad de conducción entre células vecinas puede ayudar a la detección y comprensión de algunas enfermedades cardíacas, incluida la fibrosis cardíaca.
"Como parte de nuestro estudio, implementamos la matriz de transistores en tejido cardíaco 3D y registramos las señales eléctricas intracelulares de células individuales por primera vez", dijo Xu. "En el proceso, también registramos la conducción de señales eléctricas y calculamos su velocidad".
Hasta ahora, los investigadores han probado principalmente su dispositivo de detección basado en transistores en tejido cardíaco y han obtenido resultados muy prometedores. Sus hallazgos iniciales sugieren que eventualmente podría usarse para recopilar registros precisos de señales eléctricas producidas e intercambiadas por células, tanto en entornos de laboratorio como in vivo, en los cerebros o corazones de animales vivos o pacientes humanos.
"Ahora estamos persiguiendo varios objetivos nuevos", agregó Xu. "La primera es usar nuestros transistores para realizar pruebas in vivo en corazones o cerebros intactos. La segunda es registrar las actividades intracelulares de las neuronas en diferentes ubicaciones neuronales. Finalmente, como algunas células endocrinas también son electrogénicas, lo que significa que sus actividades eléctricas son relacionados con otros eventos fisiológicos, también son de gran interés".
© 2022 Red Ciencia X Los sensores electrónicos 'emergentes' podrían detectar cuando las células cardíacas individuales se comportan mal