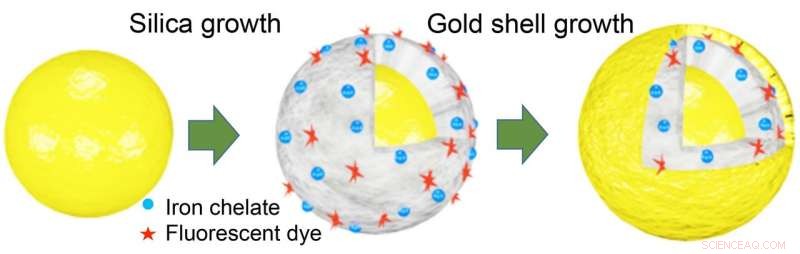
Los científicos del Laboratorio de Nanofotónica de Rice agregaron quelatos de hierro (azul) y tinte fluorescente (rojo) a nanomatryoshkas de oro de múltiples capas para crear partículas que se pueden usar para la terapia y el diagnóstico de enfermedades. Las nanopartículas 'teranósticas' tienen un núcleo de oro (izquierda) que está cubierto por sílice que contiene el hierro y el tinte de diagnóstico, que está cubierto por una capa exterior de oro. Las partículas son aproximadamente 20 veces más pequeñas que un glóbulo rojo, y variando el espesor de las capas, Los científicos de LANP pueden sintonizar las nanomatryoshkas para convertir la luz en calor que mata el cáncer. Crédito:Luke Henderson / Rice University
Los nanocientíficos de la Universidad de Rice han demostrado un método para cargar hierro dentro de nanopartículas para crear agentes de contraste de resonancia magnética que superan a los quelatos de gadolinio. el principal agente de contraste que se enfrenta a un mayor escrutinio debido a posibles problemas de seguridad.
"La posibilidad de eliminar la exposición al gadolinio y obtener una mejora doble en el rendimiento del contraste de la resonancia magnética T1 va a intrigar a los radiólogos, "dijo Naomi Halas de Rice, el investigador principal del proyecto. "Cuando escuchen que hemos hecho esto con hierro, espero que se sorprendan mucho".
Los agentes de contraste son fármacos que mejoran las imágenes de resonancia magnética y las hacen más fáciles de interpretar por los radiólogos. Los radiólogos pueden "ponderar" los resultados de una resonancia magnética y hacer que los tejidos específicos parezcan más brillantes o más oscuros variando las condiciones de la prueba. Se utilizan dos técnicas de ponderación, T1 y T2. Si bien los agentes de contraste a base de hierro se emplean con frecuencia para las exploraciones en T2, Existen pocas alternativas clínicamente disponibles al gadolinio para las pruebas de T1.
"Los quelatos de hierro no son nuevos, "Halas dijo." Se cree que son totalmente imprácticos para el contraste T1, pero este estudio es una ilustración perfecta de lo diferente que pueden comportarse las cosas cuando se diseña a nanoescala ".
Halas y sus colegas de Rice y el MD Anderson Cancer Center de la Universidad de Texas describen sus hallazgos en un artículo disponible en línea en la revista American Chemical Society. ACS Nano . En el estudio, crearon una versión modificada de nanomatryoshkas, nanopartículas concéntricas en capas que toman su nombre de las muñecas de anidación rusas.
Nanomatryoshkas y nanoconchas, otra nanopartícula en capas que Halas inventó en Rice hace más de 20 años, son aproximadamente 20 veces más pequeñas que un glóbulo rojo y están formadas por capas de metal conductor y sílice no conductora. Variando el grosor de las capas, El equipo de Halas sintoniza las partículas para que interactúen con longitudes de onda de luz específicas. Por ejemplo, tanto las nanocapas como las nanomatryoshkas pueden convertir en calor la luz infrarroja cercana que de otro modo sería inofensiva. Esta localizado, El calentamiento intenso se ha utilizado para destruir el cáncer en varios ensayos de nanoconchas, incluido un ensayo en curso para el tratamiento del cáncer de próstata.
El nuevo estudio es el último capítulo en los esfuerzos de Halas para crear nanopartículas activadas por luz con una combinación de características terapéuticas y de diagnóstico. Estas partículas "teranósticas" podrían permitir a los médicos diagnosticar y tratar el cáncer en la misma consulta o visita al hospital.
Luke Henderson, estudiante de posgrado de Rice y autor principal del ACS Nano papel, dijo, "Si los médicos pudieran visualizar las partículas a través de algún tipo de imagen, la terapia podría ser más rápida y eficaz. Por ejemplo, Imagine un escenario en el que se realiza una exploración para verificar el tamaño y la ubicación del tumor, luego se genera calor para tratar el tumor y se realiza otra exploración para verificar que todo el tumor fue destruido ".
Cuando Henderson, un químico, se unió al Laboratorio de Nanofotónica de Halas en 2016, El equipo de Halas ya había demostrado que podía agregar tintes fluorescentes a las nanomatryoshkas para hacerlas visibles en las exploraciones de diagnóstico. También se estaba trabajando en un estudio publicado en 2017 que mostró que los quelatos de gadolinio podrían incrustarse en la capa de sílice para el contraste de resonancia magnética.
Los escáneres de resonancia magnética obtienen imágenes del interior del cuerpo alineando brevemente los núcleos de los átomos de hidrógeno y midiendo cuánto tardan los núcleos en "relajarse" hasta su estado de reposo. Las propiedades de relajación varían según el tejido, y alineando núcleos repetidamente y midiendo los tiempos de relajación, un escáner de resonancia magnética crea una imagen detallada de los órganos del cuerpo, tejidos y estructuras. Los agentes de contraste mejoran la resolución del escaneo al aumentar la tasa de relajación de las partículas.
Los quelatos de gadolinio revolucionaron las pruebas de resonancia magnética cuando se introdujeron a fines de la década de 1980 y se han utilizado más de 400 millones de veces. Aunque el gadolinio es un metal tóxico, El proceso de quelación cubre cada ion de gadolinio con una envoltura orgánica que reduce la exposición y permite que el fármaco pase del cuerpo a través de la micción en unas pocas horas.
En 2013, Los científicos japoneses hicieron el sorprendente descubrimiento de que el gadolinio de los agentes de contraste se había acumulado en el cerebro de algunos pacientes. y estudios posteriores encontraron depósitos similares en huesos y otros órganos. Si bien no se han asociado efectos adversos para la salud con los agentes de contraste de resonancia magnética a base de gadolinio, La FDA exigió a los fabricantes de medicamentos que agreguen advertencias a las guías de medicamentos para ocho agentes de contraste a base de gadolinio ampliamente utilizados en diciembre de 2017.
"En el trabajo anterior con gadolinio, notamos que el diseño de nanomatryoshka mejoraba las relajaciones de los quelatos de gadolinio incrustados, "Dijo Henderson." Al mismo tiempo, escuchábamos más llamadas de la comunidad médica en busca de alternativas al gadolinio, y decidimos probar los quelatos de hierro y ver si obtuvimos el mismo tipo de mejora ".
Los resultados sorprendieron a todos. Henderson no solo pudo aumentar la relajación del hierro, pudo cargar aproximadamente cuatro veces más hierro en cada nanomatryoshka. Eso permitió que las nanomatryoshkas cargadas de hierro funcionaran dos veces más que los quelatos de gadolinio clínicamente disponibles.
Henderson también encontró una forma genérica de cambiar el tipo de metal que se cargaba. Al agregar primero moléculas de quelato descargadas a la sílice, descubrió que podía cargar metal sumergiendo las partículas en un baño de sales metálicas. Al cambiar los metales en el baño, descubrió que podía cargar fácilmente diferentes iones paramagnéticos, incluyendo manganeso, en las nanomatryoshkas.
Después de cargar los iones metálicos en la sílice, la capa final de la nanomatryoshka, la capa exterior de oro, fue añadido. La cáscara, que es vital para plasmónicos, también sirve como barrera para prevenir la lixiviación de iones. Henderson dijo que la barrera del oro también tiene un beneficio secundario para los tintes fluorescentes que agregó para los diagnósticos de modo dual.
"Todos los tintes fluorescentes están sujetos a blanqueamiento fotográfico, lo que significa que se desvanecen con el tiempo y, finalmente, no emitirán una señal medible, "Dijo Henderson." Incluso si los congelas, que ralentiza el blanqueamiento, normalmente no duran más de un par de semanas. Estaba mirando una muestra antigua de nanomatryoshkas que había estado en la nevera durante meses, y descubrí que todavía tenían una fluorescencia bastante buena. Cuando miramos más de cerca esto, encontramos que los tintes eran aproximadamente 23 veces más estables cuando estaban dentro de las nanomatryoshkas ".