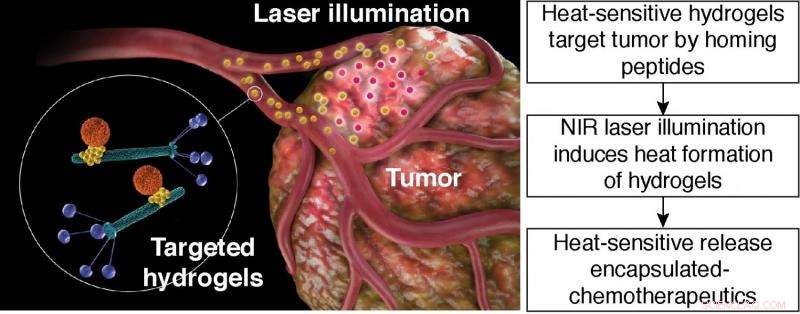
Liberación sensible al calor de quimioterápicos encapsulados. Ilustración esquemática de la terapia fototérmica de hidrogel dirigida. Hidrogel dirigido:partícula naranja, nanoportador a base de liposomas; partícula amarilla, Nanopartícula de oro; varillas verdes, partículas de bacteriófago con ligandos peptídicos que se muestran en la proteína de recubrimiento del fago (azul). Crédito:Hosoya, et al.
(Phys.org) —Las nanopartículas funcionalizadas son una vía de administración de fármacos para la quimioterapia. Sin embargo, Ha demostrado ser difícil conseguir que las nanopartículas se dirijan al sitio del tumor. Un método que los investigadores han utilizado para atacar las células cancerosas es crear hidrogeles hechos de bacteriófagos filamentosos (fagos) y nanopartículas de oro. Pueden incorporarse ligandos de unión a péptidos en la porción de fago del hidrogel que luego se dirigirá a las células de carcinoma conocidas.
Un grupo interdisciplinario de investigadores de varias universidades de Japón, los Estados Unidos., y Alemania han desarrollado una plataforma de hidrogel que puede apuntar a tumores, proporcionar imágenes no invasivas, y liberar un fármaco quimioterápico. Han demostrado su plataforma tanto en estudios in vitro como en modelos de ratón. Adicionalmente, demuestran que su plataforma se puede generalizar a diferentes objetivos y quimioterapéuticos. Su trabajo aparece en el procedimientos de la Academia Nacional de Ciencias .
Hosoya, et al., la plataforma de hidrogel consiste en bacteriófagos, nanopartículas de oro, y vehículos de tamaño nanométrico tales como liposomas o partículas de sílice mesoporosa. En esta configuración, Las partículas de fagos son capaces de reconocer moléculas específicas en las células tumorales. Las nanopartículas de oro sirven como "informadoras" de la distribución del hidrogel. El nanoportador transporta diversos productos químicos o carga farmacéutica. El nanoportador libera carga ante un estímulo específico, como el calor.
En el trabajo actual, Hosoya, et al. demostró por primera vez que los liposomas sensibles al calor (HSL) servirían como un portador formidable sensible al calor. En teoria, a medida que la HSL comienza a derretirse, libera la droga que está incorporada en él. Usando calceína, una molécula fluorescente activa, determinaron que HSL liberó calceína al alcanzar los 40 o C, como se predijo. Cuando el HSL se dejó a temperatura constante (42 o C), liberó toda la calceína en 10 minutos. Hosoya, et al. luego demostró que estas HSL todavía respondían a los cambios de temperatura cuando se incorporaron a la plataforma de hidrogel.
El siguiente paso fue demostrar que los hidrogeles que contienen HSL respondían al calentamiento NIR mientras estaban dentro de una matriz. Los autores utilizaron gel de agarosa como sistema modelo. Descubrieron que el hidrogel que contenía HSL respondía al calentamiento NIR y, a medida que aumentaba la potencia del láser, la temperatura del hidrogel aumentó. Luego determinaron si el calentamiento NIR desencadenaría la liberación de doxorrubicina (dox), un quimioterápico. Pudieron producir un "aumento dependiente de la dosis de fotones reproducible y robusto en la intensidad de la fluorescencia".
Para determinar la distribución de calor en el hidrogel de NIR, utilizaron imágenes de temperatura por resonancia magnética en los hidrogeles que contienen HSL en la plataforma de agarosa. Las imágenes de gradiente térmico confirmaron que el calor centralizado fue producido por el hidrogel a través del láser NIR. Utilizaron hidrogeles que contenían HSL encapsulados en gadolinio para confirmar que la liberación del fármaco se produjo en la ubicación del rayo láser.
Si bien estos resultados muestran que la liberación de fármacos se puede controlar mediante NIR, todavía necesitan probar si el sistema puede apuntar al sitio del cáncer. Para hacer esto, Hosoya, et al incorporaron un ligando que tiene un péptido cíclico bien establecido que se une a CRKL. Las partículas de fago que se unen a CRKL se dirigen a EF43. fgf-4 células de carcinoma mamario. Usando hidrogeles que contienen HSL marcados con rodamina, demostraron que el fago se dirigía a las células del carcinoma, confirmando que aún mantiene sus propiedades aglutinantes incluso cuando se incorpora a la nanoplataforma.
Luego hicieron pruebas in vivo en ratones. Rastrearon la ubicación y los efectos de su plataforma de hidrogel que contiene HSL en ratones que tenían EF43. fgf-4 carcinoma de mama. Los estudios de imágenes de fluorescencia óptica mostraron que el tumor era visible en ratones tratados con el sistema de hidrogel dirigido en comparación con los controles. El análisis de los tumores después de 24 h reveló que las nanopartículas de oro, fago dirigido, y las HSL se localizaron dentro del tumor. Los estudios adicionales para ver si su sistema podría liberar un quimioterapéutico usando NIR en el sitio del tumor también resultaron exitosos. Los autores observaron un crecimiento tumoral reducido en ratones con hidrogeles que contienen HSL con dox, y confirmaron sus resultados utilizando modelos matemáticos.
Finalmente, para probar la versatilidad de su nanoplataforma de hidrogel, Hosoya, et al. incorporó nanopartículas de sílice mesoporosas (MSNP) en el sistema de hidrogel. Las propiedades químicas de MSNP permiten empaquetar diferentes quimioterapéuticos. Probaron si los hidrogeles que contienen MSNP podrían administrar FITC en dos modelos de cáncer diferentes, el mismo modelo de cáncer de mama utilizado anteriormente (EF43. fgf-4 ) y un modelo para el cáncer de próstata. Encontraron una unión dirigida a los dos cánceres y los estudios con dox mostraron una disminución en el tamaño del tumor.
Este trabajo demuestra una plataforma de hidrogel que no cambia las propiedades físicas o químicas de los sistemas nanoportadores conocidos, como los liposomas sensibles al calor o las nanopartículas de sílice mesoporosas. Esta plataforma permite la orientación, parto inducido por calor, y es a la vez versátil y reproducible. Con estudios adicionales, este sistema podría ser general, método robusto para la administración de fármacos dirigida.
© 2016 Phys.org