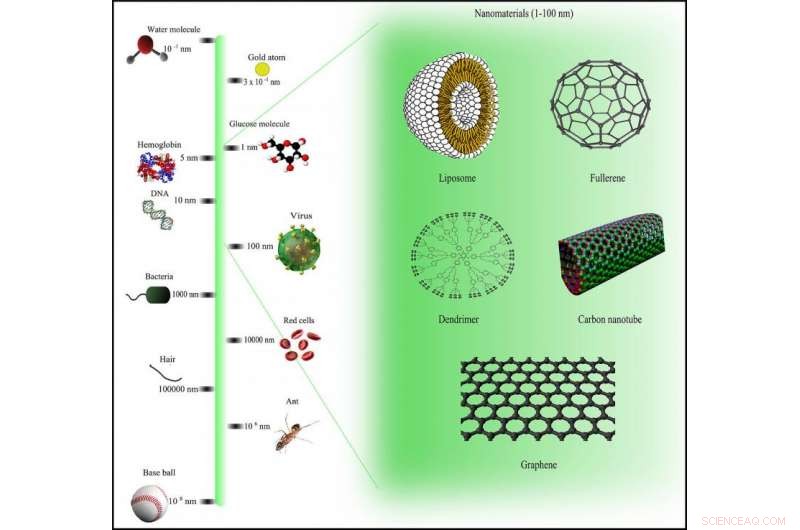
Escala de comparación de nanomateriales a través de Wikimedia Commons bajo licencia CC BY-SA 3.0
Cuando tomas una droga, viaja por tu torrente sanguíneo, disolviendo y dispersando, y finalmente llegar a su área objetivo designada.
Pero debido a que la sangre que contiene el medicamento viaja por todo el cuerpo, solo un pequeño porcentaje de la dosis inicial llega al lugar deseado.
Para medicamentos de venta libre como paracetamol o ibuprofeno, con muy pocos efectos secundarios, esto no importa demasiado.
Pero cuando se trata de medicamentos contra el cáncer, que puede afectar a las células sanas tanto como a las células cancerosas, este proceso puede causar grandes problemas.
En parte porque las drogas se diluyen en su sangre, los pacientes con cáncer necesitan tomar estos medicamentos en dosis particularmente altas, y esto puede causar efectos secundarios muy desagradables.
Pero la profesora Sonia Trigueros, codirector del Programa Oxford Martin de Nanotecnología, se está acercando cada vez más al desarrollo de un sistema de administración de fármacos a nanoescala con el objetivo de apuntar específicamente a las células cancerosas.
Trabajando con un equipo de químicos, ingenieros y físicos, Trigueros se ha embarcado en una ambiciosa misión para abordar el cáncer en el nivel 'nano':menos de 100 nanómetros de ancho. Para el contexto, esto es muy pequeño:un nanómetro es una milésima de milésima de milímetro.
Todavía queda un largo camino por recorrer pero Trigueros está avanzando decente, y ha abordado recientemente un problema importante de trabajar a nivel nano. Y en la conferencia Wired Health de este año, que analizó el futuro de la atención médica, bienestar y genómica:nos habló de su progreso reciente, y sus visiones para el futuro.
A nivel nano
Algunos de nosotros recordaremos la tabla periódica que se muestra en nuestras aulas de ciencias que nos informa sobre las propiedades de cada elemento. Pero trabajando en un nivel nano todo cambia, y los elementos se comportan de manera completamente diferente.
Los elementos tienen propiedades diferentes a nivel nano que a nivel micro, explicó el profesor Trigueros a la audiencia de Wired Health 2015.
Esto plantea grandes problemas para los investigadores que intentan fabricar dispositivos a nanoescala, que puede estar hecho de varios materiales diferentes, incluido el oro, plata y carbono. Todos estos materiales son muy inestables a nivel nano.
"Después de crear las nanoestructuras, solo tiene unos minutos o un par de días para trabajar, ", dijo. Son realmente inestables, especialmente cuando los pones en agua ".
Esto no es ideal considerando que nuestros cuerpos están compuestos principalmente de agua.
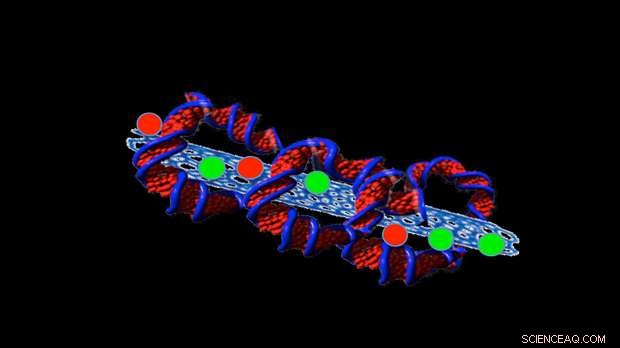
Crédito:Profesora Sonia Trigueros
El trabajo reciente de Trigueros se ha centrado en intentar estabilizar pequeños tubos hechos de carbono, llamados nanotubos de carbono, que contienen medicamentos dentro del tubo para que puedan ser administrados a las células cancerosas.
Ahora ha encontrado una forma de mantenerlos estables durante más de dos años y en temperaturas de hasta 42ºC.
Para hacer esto, ella envuelve el ADN alrededor de las estructuras, como una tortilla envuelve los rellenos de un burrito.
Si bien esto logra el objetivo de mantener estables las nanoestructuras dentro del cuerpo, no sirve de mucho si el ADN no puede desenvolverse para administrar los medicamentos. Pero, según Trigueros, ella ha demostrado que, una vez dentro de una celda, el ADN se desenrolla fácilmente y libera su carga útil.
Entrega de medicamentos verdaderamente dirigida
Entonces, cómo funciona todo? ¿Cómo ingresan los medicamentos a las células cancerosas? Los nanotubos de Trigueros aprovechan las diferencias entre las células cancerosas y las células sanas; en este caso, diferencias en las membranas que los mantienen unidos.
"Las células cancerosas son más permeables que las células normales, por lo que los nanotubos pueden atravesar la membrana celular. Y una vez que están dentro, desenvuelven y entregan droga, "explicó Trigueros.
Aprovechar las diferencias en su permeabilidad es una forma de atacar las células cancerosas, pero Trigueros explica que hay más de una forma de crear un sistema de administración de medicamentos verdaderamente dirigido.
"Podemos adjuntar lo que queramos al ADN, ", dijo." Para que pueda adjuntar una proteína que reconoce las células cancerosas ".
De la teoría a la realidad
Si bien todo esto suena genial en teoría, ¿Funcionará realmente en la realidad?
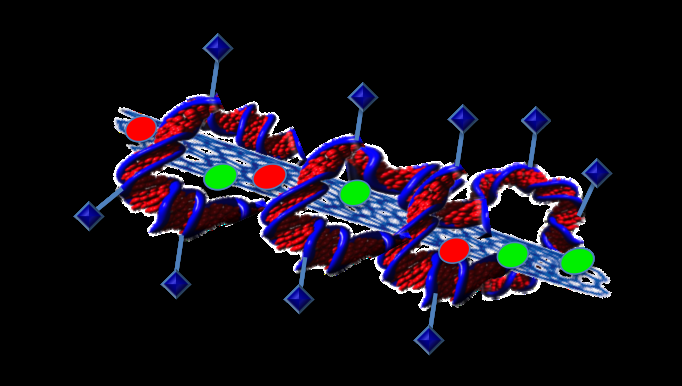
La unión de proteínas al ADN podría crear un sistema de administración de fármacos verdaderamente dirigido. Crédito:Profesora Sonia Trigueros
Trigueros ha comenzado ahora las pruebas preliminares en células de cáncer de pulmón cultivadas en laboratorio, nos dijo durante una entrevista. Y esto ha mostrado una promesa tentativa, ella dice, citando datos no publicados sobre su efectividad para matar estas células en el laboratorio.
Otros son cautelosamente optimistas. "Esta es una perspectiva realmente emocionante, "dice el profesor Duncan Graham, experto en nanotecnología y asesor de Cancer Research UK.
"Una preocupación común con los nanotubos de carbono es la toxicidad, but when coated with DNA this concern could be removed, " el explica, "and it also addresses a fundamental issue, which is that they collect into clusters that become a solid mass and so are unable to leave the body."
In theory, once Trigueros's nanotubes have finished their job they are tiny enough (50 nanometres) to be excreted through urine.
This isn't the first time carbon nanotubes have been used in cancer research:a US research team has used them, por ejemplo, to target and collect images of tumours in mice. But the combination of drug delivery and cancer-specific targeting is what interests Professor Graham.
"Unlike previous work using carbon nanotubes, this approach is set to target the tumour specifically, potentially meaning fewer side effects and a lower dosage. I look forward to seeing this in animal models which is where the real proof of activity lies, " él dijo.
But he's cautious, stressing that Trigueros's work has not yet been peer-reviewed and published.
Próximos pasos
Next Trigueros is aiming towards starting animal trials and, finalmente, she wants to begin clinical trials in patients – that is if everything goes well.
She hopes to focus on how nanostructures could be used to cross the blood-brain barrier – the brain's highly selective 'bouncer' that only lets certain molecules across. This has been notoriously difficult to get past, making targeting cancers in the brain more difficult.
But there is a still a long way to go and a lot of problems to tackle. In the shorter term, we'll be keeping an eager eye on her drug delivery research, as her ideas continue to develop.