MYC es la proteína informe responsable de empeorar la mayoría de los casos de cáncer humano. Los investigadores de UC Riverside han encontrado una manera de controlarlo, ofreciendo esperanza para una nueva era de tratamientos.
En las células sanas, MYC ayuda a guiar el proceso de transcripción, en el que la información genética se convierte del ADN en ARN y, finalmente, en proteínas. "Normalmente, la actividad de MYC está estrictamente controlada. En las células cancerosas, se vuelve hiperactiva y no se regula adecuadamente", dijo el profesor asociado de química de la UCR, Min Xue.
"MYC se parece menos a un alimento para las células cancerosas y más a un esteroide que promueve el rápido crecimiento del cáncer", dijo Xue. "Es por eso que MYC es el culpable del 75% de todos los casos de cáncer humano."
Al principio de este proyecto, el equipo de investigación de la UCR creía que si podían frenar la hiperactividad de MYC, podrían abrir una ventana en la que se podría controlar el cáncer.
Sin embargo, encontrar una manera de controlar MYC fue un desafío porque, a diferencia de la mayoría de las otras proteínas, MYC no tiene estructura. "Es básicamente una masa de aleatoriedad", dijo Xue. "Los procesos de descubrimiento de fármacos convencionales se basan en estructuras bien definidas, y esto no existe para MYC."
Un nuevo artículo en el Journal of the American Chemical Society , del que Xue es el autor principal, describe un compuesto peptídico que se une a MYC y suprime su actividad.
En 2018, los investigadores notaron que cambiar la rigidez y la forma de un péptido mejora su capacidad para interactuar con objetivos proteicos sin estructura como MYC.
"Los péptidos pueden asumir una variedad de formas y posiciones", dijo Xue. "Una vez que los doblas y conectas para formar anillos, no pueden adoptar otras formas posibles, por lo que tienen un bajo nivel de aleatoriedad. Esto ayuda con la unión".
En el artículo, el equipo describe un nuevo péptido que se une directamente a MYC con lo que se llama afinidad submicromolar, que se acerca cada vez más a la fuerza de un anticuerpo. En otras palabras, es una interacción muy fuerte y específica.
"Mejoramos el rendimiento de unión de este péptido con respecto a versiones anteriores en dos órdenes de magnitud", dijo Xue. "Esto lo acerca a nuestros objetivos de desarrollo de fármacos".
Actualmente, los investigadores están utilizando nanopartículas lipídicas para introducir el péptido en las células. Se trata de pequeñas esferas formadas por moléculas grasas y no son ideales para su uso como fármaco. En el futuro, los investigadores están desarrollando una química que mejore la capacidad del péptido principal para ingresar a las células.
Una vez que el péptido esté en la célula, se unirá a MYC, cambiando las propiedades físicas de MYC e impidiendo que realice actividades de transcripción.
El laboratorio de Xue en UC Riverside desarrolla herramientas moleculares para comprender mejor la biología y utiliza ese conocimiento para realizar el descubrimiento de fármacos. Ha estado interesado durante mucho tiempo en la química de los procesos caóticos, lo que lo atrajo al desafío de domesticar MYC.
"MYC representa el caos, básicamente, porque carece de estructura. Eso, y su impacto directo en tantos tipos de cáncer, lo convierten en uno de los santos griales del desarrollo de fármacos contra el cáncer", afirmó Xue. "Estamos muy entusiasmados de que ahora esté a nuestro alcance."
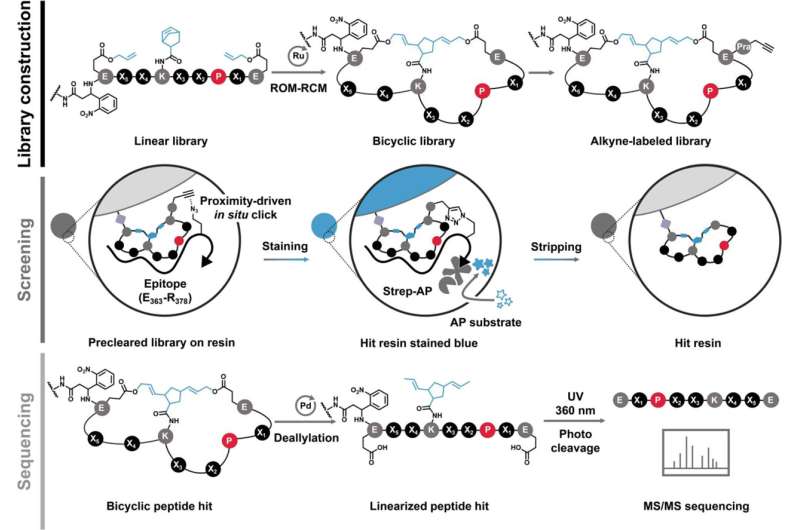
Más información: Zhonghan Li et al, Inhibidores dirigidos a MYC generados a partir de una biblioteca de péptidos bicíclicos estereodiversificados, Revista de la Sociedad Química Estadounidense (2024). DOI:10.1021/jacs.3c09615
Información de la revista: Revista de la Sociedad Química Estadounidense
Proporcionado por la Universidad de California - Riverside