
El estudiante graduado de la Universidad de Rice, Kang-Jie (Harry) Bian, configura moléculas sensibles a la luz para un experimento en el laboratorio del químico Julian West. Bian es el autor principal de un estudio inspirado en procesos naturales para permitir la difuncionalización modular de moléculas de alquenos para el diseño de fármacos y materiales. Crédito:Universidad Rice
Inspirado en su hígado y activado por la luz, un proceso químico desarrollado en los laboratorios de la Universidad de Rice y en China se muestra prometedor para el diseño de fármacos y el desarrollo de materiales únicos.
Los investigadores dirigidos por el químico de Rice Julian West y Xi-Sheng Wang de la Universidad de Ciencia y Tecnología de China, Hefei, informan sobre su exitoso proceso catalítico para agregar simultáneamente dos grupos funcionales distintos a alquenos individuales, moléculas orgánicas extraídas de productos petroquímicos que contienen al menos un doble enlace carbono-carbono combinado con átomos de hidrógeno.
Mejor aún, dicen, es que estos alquenos están "inactivados", es decir, carecen de átomos reactivos cerca del doble enlace, y hasta ahora han resultado difíciles de mejorar.
La vía química detallada en el Journal of the American Chemical Society podría simplificar la creación de una biblioteca de precursores para la industria farmacéutica y mejorar la fabricación de polímeros.
West, cuyo laboratorio diseña procesos de química sintética, dijo que la inspiración inicial provino de una enzima, el citocromo P450, que el hígado usa para eliminar moléculas potencialmente dañinas.
"Estas enzimas son una especie de sierras circulares que trituran las moléculas antes de que puedan causarle problemas", dijo. "Hacen esto a través de un mecanismo interesante llamado rebote radical".
West dijo que P450 encuentra enlaces carbono-hidrógeno y elimina el hidrógeno, dejando un radical centrado en el carbono que incluye un electrón desapareado.
"Ese electrón realmente quiere encontrar un compañero, por lo que el P450 devolverá inmediatamente un átomo de oxígeno (el 'rebote'), oxidando la molécula", dijo. "En el cuerpo, eso ayuda a desactivar estas moléculas para que puedas deshacerte de ellas.
"Este tipo de rebote es poderoso", dijo West. "Y Harry (el autor principal Kang-Jie Bian, un estudiante graduado de Rice) se preguntó si podríamos hacer algo así para transferir diferentes fragmentos a ese radical".
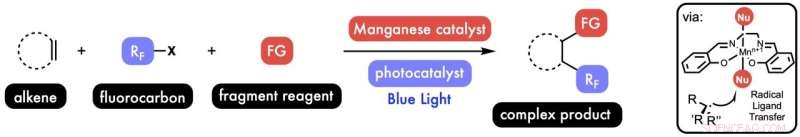
Químicos de la Universidad de Rice desarrollaron un método para agregar dos fragmentos a una molécula de alqueno en un solo proceso. El descubrimiento podría simplificar el diseño de fármacos y materiales. Crédito:West Research Group/Universidad de Rice
Su solución fue permitir lo que ellos llaman transferencia de ligandos radicales, un método general que utiliza manganeso para catalizar el "rebote radical".
West dijo que mientras P450 usa el elemento cercano, el hierro, para catalizar la reacción biológica, experimentos anteriores en el laboratorio de Rice y en otros lugares mostraron que el manganeso tenía potencial.
"El manganeso ayudó a que el proceso fuera más selectivo y un poco más activo, además de mucho más barato y fácil", explicó. "Puede transferir un montón de átomos diferentes, como cloro, nitrógeno y azufre, simplemente cambiando el ingrediente comercial que agrega a la reacción".
Esa reacción representó una funcionalización. ¿Por qué no ir por dos?
West dijo que a Bian también se le ocurrió la idea de agregar un fotocatalizador a la mezcla. "Cuando lo iluminas, se excita y puedes hacer cosas que serían imposibles en el estado fundamental, como activar pequeñas moléculas de fluorocarbono para hacer fragmentos radicales que tienen enlaces carbono-flúor, que son importantes para la ciencia farmacéutica y de materiales". " él dijo. "Ahora podemos unirlos a nuestra molécula de interés".
El resultado final es un proceso suave y modular para agregar dos grupos funcionales a un solo alqueno en un solo paso.
"Primero tenemos el doble enlace carbono-carbono de una molécula de interés, el alqueno", dijo West, resumiendo. "Luego agregamos este valioso fluorocarbono, y luego el catalizador de manganeso nada hacia arriba y realiza esta transferencia de ligando radical para agregar un átomo de cloro, nitrógeno o azufre".
Señaló que la colaboración entre Rice y el laboratorio de Wang fue un resultado natural del traslado de Bian a Rice desde Hefei, donde obtuvo su maestría. "Realmente nos enfocamos en el aspecto del manganeso de este trabajo, y el grupo de Wang no solo aportó experiencia en fotocatálisis, sino que también desarrolló y probó fragmentos de carbono-flúor, y demostró que funcionarían muy bien en este sistema", dijo West.
Dijo que junto con las ciencias farmacéuticas y de materiales, la biología química también podría beneficiarse del proceso, especialmente por su afinidad con pClick, un método descubierto por el químico Han Xiao de Rice para unir drogas u otras sustancias a los anticuerpos.
Los coautores son el estudiante de grado de Rice David Nemoto Jr. y el estudiante de posgrado Shih-Chieh Kao, y Yan He y Yan Li de Hefei. Wang es profesor en Hefei. West es el joven investigador Norman Hackerman-Welch y profesor asistente de química. ¿Tiene prisa por desarrollar fármacos? Aquí está tu CHAT