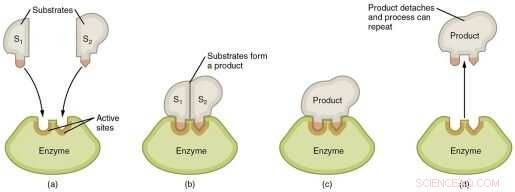
Representación gráfica de los pasos de una reacción enzimática. Crédito:Wikimedia Commons
Las enzimas que se encuentran en los organismos vivos tienen un poder catalítico impresionante. Gracias a las enzimas, las reacciones químicas que sustentan la vida suceden millones de veces más rápido de lo que ocurrirían sin ellas. Las enzimas aceleran las reacciones al ayudar a reducir la energía de activación necesaria para iniciarlas, pero durante más de 70 años, la forma en que las enzimas logran esto ha sido objeto de un intenso debate.
El Dr. Tor Savidge, profesor de patología e inmunología en el Baylor College of Medicine y el Texas Children's Microbiome Center, y sus colegas están cambiando la forma de ver este viejo argumento. En su trabajo publicado en Chemical Science , investigaron las similitudes y diferencias entre los dos mecanismos actualmente en debate al caracterizar las reacciones catalíticas a un nivel molecular detallado.
"En la actualidad, se proponen dos mecanismos de reacción diferentes principales para explicar el poder catalítico enzimático", dijo Savidge. "Uno propone que las enzimas reducen la energía de activación de la reacción a través de la estabilización de los estados de transición (TS) y el otro que lo hacen desestabilizando el estado fundamental (GS) de las enzimas. La idea actual es que estos mecanismos son mutuamente excluyentes".
El primer autor, el Dr. Deliang Chen de la Universidad Normal de Gannan en China, y sus colegas adoptaron un enfoque teórico, teniendo en cuenta los hallazgos anteriores del laboratorio de Savidge que muestran que las interacciones no covalentes de los sustratos y las enzimas con el agua son importantes en términos del mecanismo de la enzima. reacciones.
"En un entorno biológico, debe considerar el agua, que va a interferir con las interacciones atómicas muy complejas que ocurren en el sitio activo de la enzima. Necesitamos considerarlas todas para comprender dónde exactamente necesita tener interacciones electrostáticas que son va a favorecer ese proceso enzimático", dijo Savidge. "Cuando se toma eso en consideración, se puede comprender cómo funcionan estos mecanismos".
Sus análisis llevaron al equipo a proponer algo nuevo:que TS y GS no son tan diferentes después de todo. Utilizan un mecanismo atómico similar para impulsar la reacción enzimática. El mecanismo implica que el agua altera la carga de residuos importantes dentro del sitio catalítico de una manera que favorece la formación de un estado energéticamente favorable que impulsa la reacción enzimática.
"El nuevo punto importante aquí no es cómo se logra esto sino cuándo se logra", dijo Savidge. "Hemos demostrado que en la estabilización de los estados de transición, las cargas que impulsan la reacción se forman antes de que el sustrato ingrese al sitio activo. Mientras que en el estado fundamental de desestabilización esto también ocurre, pero después de que el sustrato ingresa al sitio activo". P>
Los investigadores también propusieron que el mecanismo común entre TS y GS es universal; se puede aplicar a muchas reacciones enzimáticas.
Sus hallazgos tienen implicaciones importantes no solo para ayudar a los investigadores a comprender mejor el poder catalítico de las enzimas, sino también para aplicaciones prácticas de diseño de fármacos.
"Usamos nuestros hallazgos para explorar más profundamente la catálisis enzimática microbiana en diferentes entornos y para diseñar enzimas artificiales", dijo Savidge.
Yibao Li, Xun Li, Xiaolin Fan, de la Universidad Normal de Gannan, y Xuechuan Hong, de la Facultad de Ciencias Farmacéuticas de la Universidad de Wuhan, también contribuyeron a este trabajo. Mapeo de campos eléctricos para ayudar a desentrañar cómo funcionan las enzimas