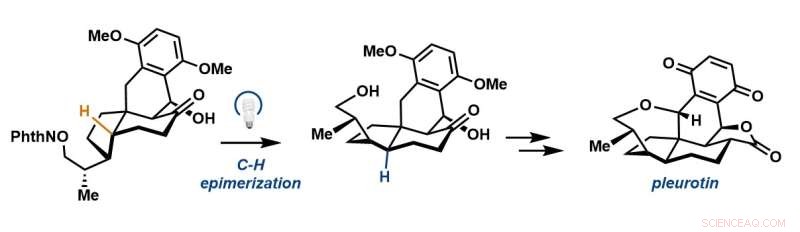
Una epimerización de radicales fotoredox genera el esqueleto tetracíclico de pleurotina. Crédito:Laboratorio Sorensen
Desde la perspectiva de los químicos, la pleurotina es una molécula intrigante.
Existe una fuerte evidencia de propiedades terapéuticas sin explotar como inhibidor de tumores y antibiótico. Tiene una estructura compleja fascinante (¡seis anillos! ¡ocho estereocentros!). Y ha sido difícil de sintetizar a lo largo de las décadas. La última vez que los químicos lograron eso, fue en el año 1988 y necesitaban 26 pasos para hacerlo.
Para el Laboratorio Sorensen de Princeton Chemistry, esas cualidades fueron parte del atractivo para una inversión a largo plazo de tiempo y energía que se ha hecho realidad.
El laboratorio informa de una síntesis concisa de pleurotina mediante la reacción de Diels-Alder y una epimerización radical que convierte un cis-hidrindano en el trans-hidrindano deseado. Su etapa intermedia intermedia se cruza con la síntesis del hito de 1988 hacia el final del proceso, lo que reduce el número total de pasos necesarios para la síntesis en trece.
El proceso del laboratorio podría generar una familia ampliada de candidatos de detección anticancerígenos similares a la pleurotina que, en el futuro, pueden ser útiles para las compañías farmacéuticas que buscan explotar la promesa de la pleurotina como un fármaco de próxima generación.
"La pleurotina es una molécula muy sensible, es muy reactiva. Pero todavía no ha funcionado como fármaco, en parte porque no es muy soluble en agua", dijo el estudiante graduado de tercer año John Hoskin, autor principal del artículo. "Lo ideal sería alterar su estructura:ajustar aquí, cambiar aquí, poner un hidroxi aquí o un fosfato allá, hacer algunas modificaciones muy cuidadosas".
"Y dado que realmente no se puede hacer eso a partir de la pleurotina en sí, nuestro enfoque será incorporar los cambios de una síntesis desde cero, lo que solo es posible debido a la brevedad de la ruta. Luego terminas con el llamado análogos que son muy similares a este producto natural pero que tienen estos cambios estratégicos".
"Una síntesis concisa de pleurotina habilitada por una epimerización C-H no tradicional" se publicó el mes pasado en el Journal of the American Chemical Society por Hoskin y P.I. Erik Sorensen, Profesor Arthur Allan Patchett de Química Orgánica en el Departamento de Química.
"Cuando un químico mira una estructura como esta, no hay estrategias obvias que uno deba tomar para crearla a partir de compuestos simples", dijo Sorensen. Su laboratorio comenzó a trabajar en pleurotin en 2008 solo para encontrarse con una serie de decepciones. Hasta ahora.
"Si tomas pleurotina y dices, quiero hacer química de sitio selectivo en su periferia para que podamos construir nuevas moléculas con propiedades mejoradas, entonces tal vez haya mejores agentes anticancerígenos", agregó. "Entonces, John y yo nos sentimos atraídos por el desafío de desarrollar un enfoque químico para construir ese marco en la menor cantidad de pasos posible".
"Ocho pasos es un número bastante pequeño de pasos para una molécula de esa complejidad", dijo Sorensen. "Esta investigación es testimonio de la habilidad de John como diseñador y ejecutor de síntesis orgánica".
Promesa sin explotar desde 1947
Pleurotin deriva del hongo Pleurotus griseus. Los investigadores describieron por primera vez la molécula en un artículo publicado en 1947 como inhibidora del crecimiento de Staphylococcus aureus, la fuente de infecciones por estafilococos. Eso fue 41 años antes de la síntesis histórica de pleurotina por parte de David Hart, ahora profesor emérito de la Universidad Estatal de Ohio.
Pero debido a la incapacidad de sintetizarlo fácilmente, la pleurotina no se ha investigado en todo su potencial. Fue entonces cuando intervino el Laboratorio Sorensen.
Para reducir los pasos hacia la síntesis, los investigadores utilizaron una táctica comprobada en síntesis orgánica llamada transferencia de átomos de hidrógeno 1,5, en la que un radical reactivo centrado en el oxígeno esencialmente "se estira" y arranca un hidrógeno de un carbono que forma parte de la estructura del pleuroestaño para formar un nuevo radical. Luego, los investigadores usaron ese radical para recibir hidrógeno de un tiol exógeno que permitiría que el estereocentro cambiara a una configuración alternativa o trans.
"Probamos muchas estrategias diferentes y finalmente lo que terminó funcionando fue este paso de inversión para pasar de este cis-hidrindano a trans-hidrindano. Esa es la idea clave", dijo Hoskin. "Al utilizar la funcionalidad inherente a la molécula, este oxígeno, podríamos, como si estuviéramos usando un par de pinzas microscópicas, extraer este hidrógeno y voltear ese carbono para obtener el transhidrindano necesario".
El proceso genera un producto final racémico, haciendo que las versiones izquierda y derecha estén en proporciones iguales. Es probable que solo uno de ellos sea bioactivo. Ahora que la síntesis formal se ha completado de una manera más concisa, dijo Hoskin, el próximo desafío será producir una versión especular de la molécula y sus análogos.
"Esta investigación muestra el poder de una breve síntesis", dijo Hoskin. "Solo lleva una semana recorrer toda la ruta".
Sorensen agregó:"Creo que este trabajo nos coloca en una posición favorable hacia nuestro objetivo más amplio de expandir la clase de agentes anticancerígenos basados en pleurotina". La reversión acelera la creación de una molécula importante:el laboratorio hace que la síntesis de halicondrina B sea más eficiente